- 124.50 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
练习19 二氧化碳制取的研究
自主学习
1.实验室制取二氧化碳气体应该用 ( )
A.煅烧石灰石 B.碳在空气中充分燃烧
C.石灰石和稀盐酸反应 D.石灰石和稀硫酸反应
答案:C
2.检验集气瓶中是否收集满二氧化碳可采用的方法是 ( )
A.加入紫色石蕊试液 B.把燃着的木条放在集气瓶口
C.加入石灰水 D.把燃着的木条放在集气瓶内
答案:B
3.实验室制取二氧化碳一般有五个步骤:①检验装置的气密性;②按要求装配好仪器;③向漏斗中注入酸液;④向广口瓶中放入小块大理石;⑤收集气体.下列操作顺序正确的是 ( )
A.①②③⑤④ B.②①④③⑤ C.①④②③⑤ D.②③④①⑤
答案:B
4.实验室常用_____________跟______________或_____________起反应来制取二氧化碳,化学方程式为__________________.由于二氧化碳的密度比空气大,可用_______________排空气法收集;又由于二氧化碳能溶于水且与水反应,所以通常___________________用排水法收集二氧化碳气体.
答案:稀盐酸 大理石 石灰石
CaCO3+2HCl=CaCl2+ H2O+CO2↑ 向上 不
5.实验室制取二氧化碳需要使用的仪器有_______________(填序号).
a.酒精灯;b.大试管;c. 水槽;d.玻璃片;e.带导管的双孔橡皮塞;f.长颈漏斗; g.铁架台 (带铁圈);h.量筒;i.集气瓶.
答案:a d e f i
6.图6-5是某同学设计的实验室制取CO装置图,请指出图6-5中的错误,并在表6-2中加以改正 表6-2
错误
改正
(1)
(1)
(2)
(2)
(3)
(3)
图6-5
答案:错误;(1)长颈漏斗下端管口在液面上;(2)发生装置中导管太长;(3)集气瓶中导管伸入太短 改正:(1)长颈漏斗下端管口伸入液面以下;(2)发生装置中导管伸入瓶内只需露出橡皮塞少许;(3)导管伸入集气瓶中接近瓶底
能力提高
7.实验室制取O2、CO2两种气体时,可能需要加热的是 ( )
A.制CO2 B.制O2 C.制O2和CO2
答案:B
8.某气体在标准状况下密度为1.98g/L,该气体易溶于水,在实验室收集此气体时可用( )
A.排水集气法 B.向上排空气集气法
C.向下排空气集气法 D.以上方法均可以
答案:B
9.下列物质中能跟盐酸反应生成使澄清石灰水变浑浊的气体的是 ( )
A.CaCO3 B.C C.Na2CO3 D.Zn
答案:AC
10.实验室制取二氧化碳时,选用的反应物最好是 ( )
A.碳酸钠粉末和稀硫酸 B.石灰石和稀硫酸
C.大理石和稀盐酸 D.大理石和浓盐酸
答案:C 实验室制取气体选择试剂必须考虑以下几点:(1)能否产生该气体;(2)原料易得,价格便宜:(3)操作简便,易于收集;(4)产生的气体中尽量少混入杂质.碳酸钠粉末和稀硫酸反应可以生成二氧化碳,但反应速率太大,难以控制.石灰石和稀硫酸反应时,会生成微溶于水的硫酸钙,覆盖在石灰石的表面,阻碍反应继续进行.大理石与盐酸反应可产生二氧化碳气体,且小块大理石与稀盐酸反应速率适中,来源方便,价格便宜,故实验室制取二氧化碳常用它与稀盐酸;但浓盐酸易挥发,使生成的二氧化碳中混有一定量的氯化氢气体.因此本题答案不得而知.
11.铁与稀盐酸反应产生氯化亚铁(FeCl)和氢气.在天平两边的托盘上各放有一个盛足量稀盐酸的烧杯,把天平调节平衡.然后向其中一个烧杯中加入5.3g碳酸钠,向另一个烧杯中加入铁片,若要使反应后天平保持平衡,加入铁片的质量是 ( )
A.5.6 g B.5.3 g C.3.215 g D.3.1 g
答案:C 向两烧杯中分别加入的Na2CO3和Fe都能与盐酸反应放出气体.加人物质的质量与放出气体的质量之差为烧杯中溶液增加的质量.若两个烧杯中溶液增加的质量相等,则反应后天平平衡.本题可利用这一思路进行计算求出结果.
12.写出以石灰石为原料用两种不同的方法生成CO2的化学方程式:
(1)_________________________________________________________________________;
(2)_________________________________________________________________________.
答案:(1)CaCO3+2HCl= CaCl2+ H2O+CO2 ↑
(2) CaCO3CaO+CO2↑.
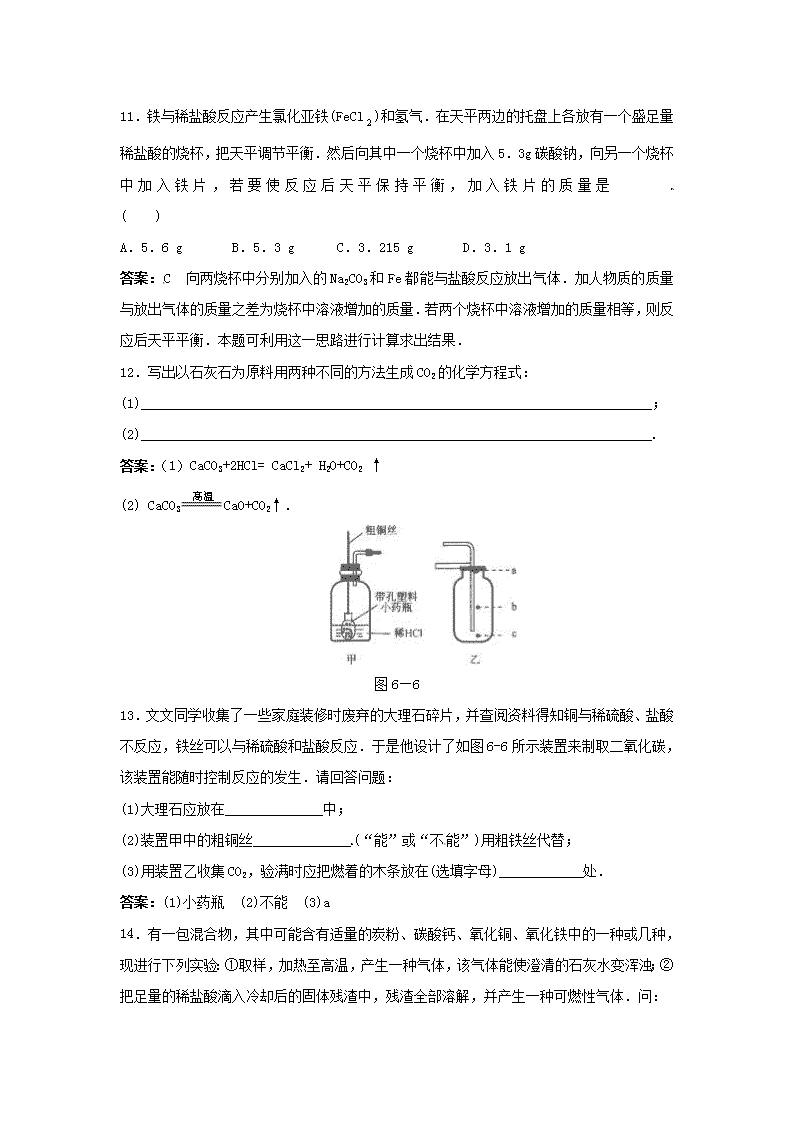
图6—6
13.文文同学收集了一些家庭装修时废弃的大理石碎片,并查阅资料得知铜与稀硫酸、盐酸不反应,铁丝可以与稀硫酸和盐酸反应.于是他设计了如图6-6所示装置来制取二氧化碳,该装置能随时控制反应的发生.请回答问题:
(1)大理石应放在______________中;
(2)装置甲中的粗铜丝______________(“能”或“不能”)用粗铁丝代替;
(3)用装置乙收集CO2,验满时应把燃着的木条放在(选填字母)____________处.
答案:(1)小药瓶 (2)不能 (3)a
14.有一包混合物,其中可能含有适量的炭粉、碳酸钙、氧化铜、氧化铁中的一种或几种,现进行下列实验:①取样,加热至高温,产生一种气体,该气体能使澄清的石灰水变浑浊;②把足量的稀盐酸滴入冷却后的固体残渣中,残渣全部溶解,并产生一种可燃性气体.问:
(1)混合物中一定不含有______________;
(2)混合物中一定含有______________、______________,在实验过程中肯定发生反应的化学方程式______________;
(3)混合物中可能含有的物质是______________,为证明它是否存在,你认为可采取的方法是____________________________.
答案:(1)氧化铜 (2)氧化铁、炭粉 3C+2Fe2O34Fe+3CO2 ↑ (3)碳酸钙取少量的样品于试管中加稀盐酸,并将产生的气体通入澄清的石灰水中
(4)取样滴加足量稀盐酸,检验其中是否含碳酸根离子.
15.小明在实验室里学习制取CO2(见图6-7),他的具体操作步骤如下:
(1)组装仪器后进行装置的气密性检查,见图(a).请你帮助他判断,该装置是否漏气?
_________________________________.
(2)他从稀硫酸和稀盐酸中选择一种酸,与石灰石反应制取CO2想一想他不用另外一种酸的理由_________________________________________________.
(3)小明想用图(b)装置制取二氧化碳,你认为是否理想______________,原因是___________________________.
(4)请你告诉他收集满二氧化碳的集气瓶,应该______________(填“正”或“倒”)放在桌面.
(5)小明将气体发生装置稍作改动如图(c),该装置与(a)中发生装置相比,优点是__________________________________________,图中小试管的作用是__________________________________________.
(6)请帮助小明检验c装置的气密性(简述过程)_______________________________________
______________________________________________________________________________.
答案:(1)不漏气 (2)反应中产生微溶于水的硫酸钙附着在大理石的周围,阻止反应继续进行,得到的二氧化碳很少 (3)不理想 因为二氧化碳溶于水 (4)正 (5)可以控制反应随时发生和停止液封
(6)将止水夹夹紧,从长颈漏斗中注入水浸没漏斗下端管口后,若漏斗内液面不再下降,则装置不漏气.
在图c中,由于长颈漏斗使锥形瓶内外相通.因此,不能按常规检查气密性的方法操作,操作时应形成密封气压.小试管的作用可从防止CO2气体散逸上考虑.
16.已知氢气是最轻的气体单质,难溶于水.图6—8所示的装置(正立放置),既用作排水法收集氧气或氢气,又能用作排空气法收集氢气或二氧化碳,试分别简要加以说明,并指明气体流入和流出的方向.
(1)排水法收集氧气:_____________________________________________________________;
(2)排水法收集氢气:_____________________________________________________________;
(3)排空气法收集氢气:___________________________________________________________;
图6—7
(4)排空气法收集二氧化碳:_______________________________________________________.
答案:(1)集气瓶应先装满水,因为氧气不易溶于水,且密度比水小,故气体应从b通入,水从a排出 (2)集气瓶应先装满水,因为氢气难溶于水,且密度比水小,故气体应从b通入,水从a排出 (3)因为氢气密度比空气小,故气体应从b通入,空气从a排出
(4)因为二氧化碳密度比空气大,故气体应从a通入,空气从b排出
图6—8
17.托盘天平两边各放一只装有稀盐酸的烧杯(盐酸足量)使天平保持平衡.在左边烧杯中加入5g碳酸钙,使其充分反应.应向右边烧杯中投入多少克镁粉,充分反应后天平仍然保持平衡?(已知:Mg+2HCl=MgCl2+ H2
答案:3.05克
18.在Na2S、Na2SO3和Na2SO4的混合物中氧的质量分数为22%,则钠元素的质量分数为多少?
答案:28.4% 从Na2S、Na2SO3和Na2SO4
的组成上找出Na和S的原子个数比相同,亦即三种物质中Na与S元素的质量比相同,因而三种物质的化合物中Na与S元素的质量比为23×2:32,再根据混合物中O的质量分数求出Na和S的质量分数,从而求得Na的质量分数.
中考链接
19.(2010,黄冈)在实验室开放日里,我与小娜、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着四瓶无标签的试剂,分别是两瓶固体和两瓶液体,我们决定对“固体与液体之间的反应”进行一系列探究.
(1)小娜同学从一瓶固体和一瓶液体中各取少量试剂于试管中进行混合,立即产生了一种五色气体.对气体是何物质,同学们进行了大胆的猜想.小佳同学的猜想可能是
①_____________________________;②_____________________________;……
(2)我想设计一个实验证明小佳同学猜想①是正确的,实验设计如表6-3(请填写).
表6-3
实验步骤
现象及结论
图6-9
(3)小华想用图6-9给定的收集装置收集一瓶小佳同学猜想②中的气体,则气体由_______________(填a或b)端进入.
(4)小丽同学从另外两瓶试剂中各取少量试剂于试管中,发现混合后,固体发生了变化,但无气泡放出.同学们对加入试管中的固体和液体从不同的反应类型、物质类别等方面进行了大胆的猜想:
猜想一:________________________________________________________________________;
猜想二;________________________________________________________________________;
……
答案:(1)①CO2 ②H2 [或O2等]
(2)如①是CO2 [或H2,或O2等],填表如表D6-1
表D6-1
实验步骤
现象及结论
将气体通入澄清石灰水中[将试管口堵一会儿,点燃此气体,或将带火星的木条插入试管中等]
石灰水变浑浊,则证明是二氧化碳.[或能燃烧,产生淡蓝色火焰,或听到爆鸣声,则证明是氢气,或木条复燃,证明是氧气等]
(3)②中如果是氢气填a(如是氧气或二氧化碳填b)
(4)猜想一:金屑与盐溶液发生置换反应;猜想二:金属氧化物与酸溶液反应,猜想三:喊与酸溶液发生复分解反应;猜想四,氧化物(如CaO)与水发生化合反应;猜想五:可溶于水的固体物质;猜想六:……
执行标准:GBl413—99
主要成分:碳酸钙
含钙量:每片含钙0.75g,每瓶50片,重40g(中外合资××公司出品)
20.(2010,厦门)某钙片的标签如表6-4,且知此钙成 表6-4
分中只有碳酸钙含有钙元素.
(1)请通过计算说明此标签中的含钙量是错误的.
(2)为测定其真实的含钙量,小东每次取10片钙片放入已称量的含足量盐酸的烧杯中,发生化学反应:CaCO3+2HCl====CaCl2+H2O+CO2↑,充分反应后再称取烧杯和剩余物的总质量,小东做了三次实验,数据如表6-5所示:
表6-5
物质的质量
第1次
第2次
第3次
第4次
反应前:烧杯+盐酸/g
22
22
22
22
10片钙片/g
8
8
8
8
反应后:烧怀+剩余物/g
26.7
26.5
26.5
26.7
①请列式计算每片此钙片含碳酸钙的质量.
②请列式计算每片此钙片的含钙量,并建议厂家如何修改标签.
答案: (1)本品若为纯碳酸钙,其含钙量为碳酸钙含钙质量分数40%,每片含钙量为0.32g,因此本品每片不可能含钙0.75g.
(2)①设:10片钙片含碳酸钙的质量为x,x=7.5g,每片此钙片含碳酸钙0.75g
②每片此钙片的含钙量:0.75g×40%=0.3g建议:将含钙量“每片含钙0.75g”改为“每片含钙0.3 g”.