- 196.50 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
空气中氧气含量测定的探究
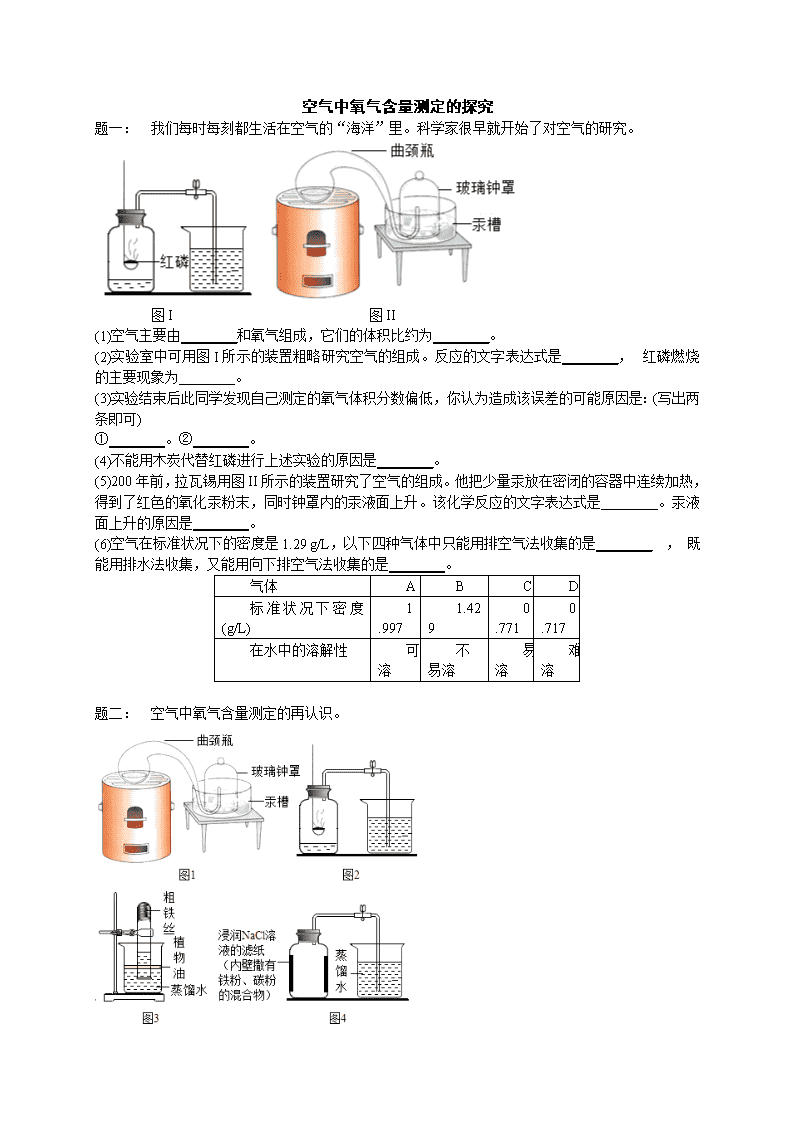
题一: 我们每时每刻都生活在空气的“海洋”里。科学家很早就开始了对空气的研究。
图I 图II
(1)空气主要由________和氧气组成,它们的体积比约为________。
(2)实验室中可用图I所示的装置粗略研究空气的组成。反应的文字表达式是________, 红磷燃烧的主要现象为________。
(3)实验结束后此同学发现自己测定的氧气体积分数偏低,你认为造成该误差的可能原因是:(写出两条即可)
①________。②________。
(4)不能用木炭代替红磷进行上述实验的原因是________。
(5)200年前,拉瓦锡用图II所示的装置研究了空气的组成。他把少量汞放在密闭的容器中连续加热,得到了红色的氧化汞粉末,同时钟罩内的汞液面上升。该化学反应的文字表达式是________。汞液面上升的原因是________。
(6)空气在标准状况下的密度是1.29 g/L,以下四种气体中只能用排空气法收集的是________ , 既能用排水法收集,又能用向下排空气法收集的是________。
气体
A
B
C
D
标准状况下密度(g/L)
1.997
1.429
0.771
0.717
在水中的溶解性
可溶
不易溶
易溶
难溶
题二: 空气中氧气含量测定的再认识。
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1)。
(1)该实验中选择使用汞的优点有_____。
A. 实验过程中没有污染
B. 在汞槽中起到液封的作用
C. 生成的化合物加热分解又能得到汞和氧气
D 能将密闭装置内空气中的氧气几乎耗尽
(2)【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),
写出红磷燃烧的化学方程式________,其反应类型为________。
兴趣小组用该方法测出的氧气含量常常远低于21%。
(3)【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行猜想】①________;
②________,装置内氧气有剩余;
(4)【实验与交流】在老师的指导下,小明分别用过量的红磷(着火点240℃)和白磷(着火点40℃)进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%。请从燃烧条件的角度回答产生上述结果的主要原因。________。
(5)【实验探究1】小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量。于是进行了实验(装置如图3)。通过7天测得的数据计算出空气中氧气的含量为19.13%。
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点。________(填字母)。
a.装置内残留的氧气更少
b.反应更彻底,实验结果更准确
c.铁丝生锈比红磷燃烧反应更快
(6)【实验探究2】为了加快反应速率,小明通过查闻资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。8分钟后测得的数据如下表:
实验前的体积
实验后的体积
集气瓶内空气
烧杯内蒸馏水
烧杯内剩余蒸馏水
131mL
90.0mL
63.6mL
请计算出空气中氧气含量________(计算结果保留一位小数)。
(7)【结论与反思】通过上述实验探究,选择________(填字母)进行实验,可较为快速地完成实验并减小实验误差。
a.红磷 b.白磷 c.铁粉、炭粉、氯化钠、蒸馏水
(8)【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿主要成分为Cu2(OH)2CO3]。若将图3装置中的粗铁丝换成足量的铜丝进
行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由。________、理由________(填字母)。
a.空气中CO2含量只有约0.03%,铜不能将装置内的氧气几乎耗尽
b.铜丝反应比铁丝快
c.反应更彻底
题一: 在测定空气中氧气含量的实验中,小强采用了下图所示装置:在由注射器和具支试管组成的密闭系统中留有25mL空气,给装有铜粉的具支试管加热,同时缓慢推拉注射器活塞,待注射器活塞稳定后,观察密闭系统内空气体积变化。
(1)在实验加热过程中,具支试管上的小气球作用是________ 。
(2)写出该实验中反应的化学方程式________ 。
(3)小强测得实验结果如下:
反应前装置内气体总体积
反应后装置内气体总体积
25 mL
22 mL
由此数据可以推算出他测定的空气中氧气的体积分数________ 21%(填“>”、“=”、 “<”)。造成该实验出现误差的原因可能是________ 。(填序号)①没有推拉注射器活塞;②读数时没有冷却至室温;③加入铜丝量太少;④加入铜丝量太多。
(4)通过上面的实验,你学到的测量空气中氧气含量的方法是________ 。
题一: 如图是某同学设计的测定空气中氧气含量的实验装置。在具支试管中铺上一层玻璃棉,用于保护反应管;注射器提前连接好,装入100mL水。实验时,将橡皮塞取下,取一定量的白磷放入具支试管底部的玻璃棉上,塞紧橡皮塞(并用拇指压住),在试管底部稍微加热,白磷燃烧。
回答下列问题:
(1)待反应结束,装置完全冷却后,注射器内的水进入具支试管的体积约为试管容积的________ 。若进水量偏小,可能的原因是________ 。
(2)整个实验过程中,活塞的运动方向为________ 。
(3)你认为该实验设计的优点是________。
题二: 为了探究某脱氧剂的成分(由两种单质组成)及利用该脱氧剂测定空气中氧气含量,兴趣小组进行了如下实验:
Ⅰ探究脱氧剂成分
(1)【实验观察】脱氧剂为灰黑色粉末,若在空气中放置一段时间,有红棕色固体生成。 【实验猜想】根据颜色变化,猜想该脱氧剂中含有________(填化学式)。
(2)【验证猜想】方法为:________。 【实验探究】新取一定量的脱氧剂,将已验证的成分分离。取剩余固体与少量CuO混合,置于图1所示装置中加热。一会儿观察到黑色固体变红色,同时澄清石灰水变浑浊。
(3)【实验结论】该脱氧剂中还含有________(填化学式)。写出澄清石灰水变浑浊的化学方程式:________。
测定空气中氧气含量
使用图2装置进行实验。实验前应先进行的操作是________。
(4)【实验过程】
步骤1:在注射器中放入足量脱氧剂粉末(体积为2mL),封闭。
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹。
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化。
【数据处理】
①实验中需要记录的数据是________。
②上述实验测定过程至少需要重复两次,其目的是________。计算得氧气约占空气体积的_____。
(5)【实验对比】
实验室常通过燃烧红磷法测定空气中氧气的含量(装置如图3)。步骤如下:
①用弹簧夹夹紧橡皮管;
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧瓶塞。
③________。
④观察并记录水面的变化情况。
多次实验发现,集气瓶内上升的水面始终小于瓶内原有空气体积的。
(6)【拓展研究】查阅资料得知,当空气中氧气的体积分数降至约为7%以下时,红磷不再燃烧。由此可知,燃烧红磷法测定结果不够准确的原因的是________。
【实验评价】与燃烧红磷法相比,脱氧剂法测定空气中氧气含量的优点是________。
题一: 注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用。某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动: [查阅资料]白磷的温度达到40℃就可以在空气中燃烧,而红磷的要达到240℃才可以在空气中燃烧,两种物质的燃烧产物五氧化二磷是固体,会刺激人体呼吸道,能与空气中的水蒸气反应,生成有毒的偏磷酸
[设计实验]设计了如图的装置进行探究活动。
[步骤与现象]
①测量试管的容积为50mL;
②检查装置的气密性良好;
③
装药品,将注射器活塞调整到合适位置,连接好仪器;
④用弹簧夹夹紧胶皮管,加热粗铜丝,观察现象;
⑤燃烧结束,试管冷却到室温后打开弹簧夹,观察注射器活塞的移动情况。
[反思与交流]
(1)实验中利用了铜丝的________性。
(2)兴趣小组同学测量试管容积的方法可能是________。
(3)步骤③中注射器活塞至少应调到________ mL处(填整数)。
(4)白磷在空气中燃烧的表达式________,步骤④中观察到的颜色变化是:红色变________色;
(5)小华同学认为步骤⑤在保证活塞自由移动的前提下,观察活塞位置时,最好将试管和注射器整体横放,小华同学的理由是________。
参考答案
题一: (1)氮气;4:1;(2)磷+氧气五氧化二磷;剧烈燃烧,放出大量热,产生大量白烟;(3)装置未冷却就打开止水夹(或塞子没塞紧、装置漏气);红磷量不足 ;(4)木炭与氧气反应生成的二氧化碳为气体,不会造成压力差 而红磷与氧气反应生成的产物是固体,会造成压力差 ;(5)汞+氧气 氧化汞;氧气与汞发生反应导致钟罩内气压降低;(6)AC;D
解析:(1)空气主要由氮气和氧气组成,它们的体积比约为4:1。
(2)实验室中用图I所示的装置粗略研究空气的组成。反应的文字表达式是磷+氧气五氧化二磷, 红磷燃烧的主要现象为剧烈燃烧,放出大量热,产生大量白烟。
(3)实验结束后发现自己测定的氧气体积分数偏低,造成该误差的可能原因是(写出两条即可):①红磷量不足 ②装置未冷却就打开止水夹(或塞子没塞紧、装置漏气)。
(4)不能用木炭代替红磷进行上述实验的原因是红磷与氧气反应生成的产物是固体,会造成压力差;木炭与氧气反应生成的二氧化碳为气体,不会造成压力差。
(5)200年前,拉瓦锡用图II所示的装置研究了空气的组成。他把少量汞放在密闭的容器中连续加热,得到了红色的氧化汞粉末,同时钟罩内的汞液面上升。该化学反应的文字表达式是:汞+氧气氧化汞。汞液面上升的原因是氧气与汞发生反应导致钟罩内气压降低。(6)易溶于水的气体只能用排空气法收集,AC气体都能溶于水,只能用排空气法收集;D气体难溶于水,密度小于空气,既能用排水法收集,又能用向下排空气法收集。
题二: 【经典赏析】BCD;【实验回顾】4P+5O2 2P2O5;化合反应; 【进行猜想】实验中装置漏气 红磷不足;【实验与交流】白磷的着火点比红磷的着火点低;【交流与反思】ab;【实验探究2】20.2%;【结论与反思】bc;【拓展延伸】不能;a。
解析:【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1)。该实验中选择使用汞的优点有在汞槽中起到液封作用;生成的化合物加热分解又能得到汞和氧气;能将密闭装置内空气中的氧气集合耗尽,故选BCD;【实验回顾】磷和氧气在点燃的条件下生成五氧化二磷,反应的化学方程式为:4P+5O2 2P2O5;其反应类型为:化合反应;【进行猜想】实验中装置漏气;所取的红磷不足(或实验前没有夹弹簧夹、实验装置可能未冷却就打开弹簧夹等);【实验与交流】小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%,请从燃烧条件的角度回答产生上述结果的主要原因白磷的着火点比红磷的着火点低;【交流与反思】铁丝在水、氧气的条件下很容易生锈,与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点及原因:装置内残留的氧气更少,实验结果更准确;【实验探究2】烧杯内蒸馏水减少的体积为氧气的体积=90mL﹣63.6mL=26.4mL空气中氧气含量= ≈20.2%。
题三: 缓冲压力或防止活塞冲出或防止试管炸裂或防止橡皮塞冲出;2Cu+O22CuO;<;①②③;利用化学反应,在不引入新的气体杂质的前提下,将氧气转化为固体,从而达到测定空气中氧气含量的目的
解析:(1)装置加热后,内部空气压强加大,在具支试管上的小气球,其作用是为缓冲压力或防止活塞冲出或防止试管炸裂或防止橡皮塞冲出;(2)铜与氧气共热,化学方程式为:2Cu+O22CuO;(3)反应前装置内气体总体积25mL,反应后装置内气体总体积22mL,则反应掉氧气体积分数为:[(25-22)/25]×100%=12%<21%,原因可能是①没有推拉注射器活塞;②读数时没有冷却至室温;③加入铜丝量太少;(4)利用化学反应,在不引入新的气体杂质的前提下,将氧气转化为固体物质,从而达到测定空气中氧气含量的目的。
题一: (1)五分之一;白磷不足量(或气密性不好、未定装置完全冷却即观察进水体积等);(2)先向左移动,后向右移动;(3)反应始终在一个密闭的容器中进行,误差较小,现象比较明显(答案合理即可)。
解析:(1)观察到注射器中的水进入具支试管内的水量约占试管容积的五分之一;若进水量偏小,可能的原因是白磷不足量或气密性不好、未等装置完全冷却即观察进水体积等;(2)白磷燃烧要放出热量,导致装置内气压变大,活塞向左移动,当温度降低时,装置内压强减小,活塞向右移动;(3)此设计具有以下优点:减少实验误差,节省燃料,不污染环境,便于读数。
题二: (1)Fe
(2)用磁铁吸引或加入盐酸有气泡
(3)C;Ca(OH)2+CO2=CaCO3↓+H2O;检查装置的气密性
(4)注射器原来的空气的体积、反应后注射器活塞进入后显示剩余气体的体积;使测量的结果更准确
(5)燃烧结束,冷却至室温
(6)氧气含量太少时,可燃物无法燃烧;不受氧气含量多少的影响,使结果更准确
解析:(1)通过实验分析可知:根据颜色变化,猜想该脱氧剂中含有Fe,因为若在空气中放置一段时间,有红棕色固体生成;(2)铁粉的检验方法是:用磁铁吸引或加入盐酸有气泡;(3)新取一定量的脱氧剂,将已验证的成分分离。取剩余固体与少量CuO混合,置于图1所示装置中加热;一会儿观察到黑色固体变红色,同时澄清石灰水变浑浊,说明还有碳,二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;故答案为:Fe;用磁铁吸引或加入盐酸有气泡;C;Ca(OH)2+CO2=CaCO3↓+H2O;(4)【数据处理】使用图2装置进行实验。实验前应先进行的操作是:检查装置的气密性;实验中需要记录的数据是:注射器原来的空气的体积、反应后注射器活塞进入后显示剩余气体的体积;上述实验测定过程至少需要重复两次,其目的是:使测量的结果更准确;故答案为:检查装置的气密性;注射器原来的空气的体积、反应后注射器活塞进入后显示剩余气体的体积;使测量的结果更准确;(5)【实验对比】本实验成功的关键是:装置要严密;红磷要足量;燃烧结束,冷却的室温,再打开止水夹;故答案为:燃烧结束,冷却的室温;(6)【拓展研究】【实验评价】由实验探究可知,燃烧红磷法测定结果不够准确的原因的是:氧气含量太少时,可燃物无法燃烧;与燃烧红磷法相比,脱氧剂法测定空气中氧气含量的优点是:不受氧气含量多少的影响,使结果更准确;故答案为:氧气含量太少时,可燃物无法燃烧;不受氧气含量多少的影响,使结果更准确。
题三: (1)导热;(2)将试管注满水,用量筒量出这些水的体积;(3)10;(4)4P+5O2 2P2O5;黑;(5)减少活塞自重对气体体积的影响
解析:(1)根据实验装置,在试管外部加热铜丝,是为了引燃白磷,铜有良好的导热性。故答案为:导热性;(2)测量试管容积的常用方法是,将试管装满水,然后测量水的体积。故答案为:将试管注满水,用量筒量出这些水的体积;(3)因为试管的容积为50mL,把试管5等分,每一等分为10mL,活塞最少应调至在10mL处。故答案为:10;(4)
白磷在空气中燃烧时,磷与氧气反应生成五氧化二磷。该反应的化学方程式为:4P+5O2 2P2O5 。 铜丝被加热生成黑色氧化铜,步骤④中观察到的颜色变化是:红色变黑色;(5)因为活塞本身也有重量,将试管和注射器整体横放,可以减少活塞自重对气体体积的影响。故答案为:减少活塞自重对气体体积的影响。