- 567.00 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
要题加练二 溶解度曲线
姓名:________ 班级:________ 限时:______分钟
1.a、b两种固体物质的溶解度曲线如图所示。下列说法不正确的是( )
A.将t1 ℃时的a、b的饱和溶液升温,溶质质量分数都变大
B.t2℃时,两种物质的饱和溶液中溶质质量分数a>b
C.使b物质结晶的最好方法是蒸发溶剂
D.将t2℃时a、b的饱和溶液分别降温至t1℃时,两溶液的溶质质量分数相等
2.甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
A.20 ℃时,甲物质的溶解度是40
B.升温可使乙物质的饱和溶液析出固体
C.甲物质的溶解度大于乙物质的溶解度
D.40 ℃时,将甲、乙两物质饱和溶液分别降温到20 ℃,二者都变为不饱和溶液
3.如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线。下列说法错误的是( )
A.t1 ℃时,三种物质中B的溶解度最大
8
B.t1 ℃时,将等质量的A、C不饱和溶液分别用添加溶质的方法形成饱和溶液,所加的溶质质量相等
C.可用降低温度的方法使t2 ℃时C的饱和溶液变为不饱和溶液
D.t2 ℃时,三种物质的饱和溶液中,溶质质量分数最大的是A
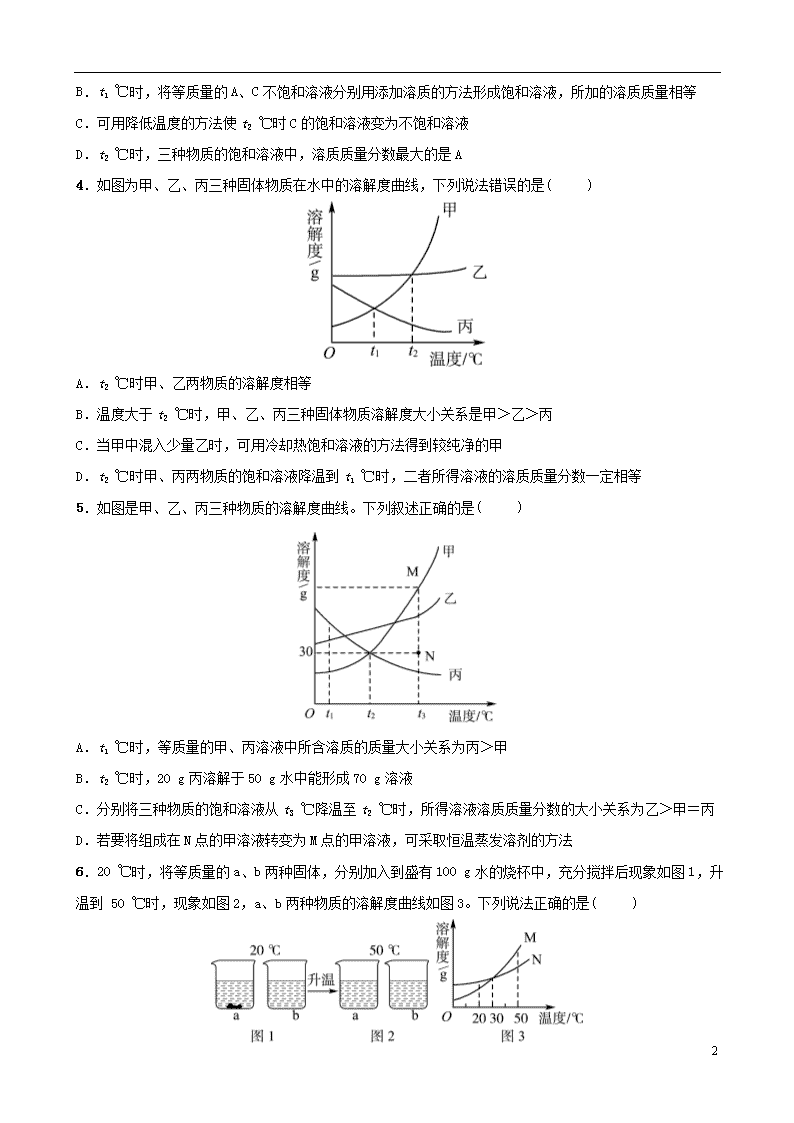
4.如图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是( )
A.t2 ℃时甲、乙两物质的溶解度相等
B.温度大于t2 ℃时,甲、乙、丙三种固体物质溶解度大小关系是甲>乙>丙
C.当甲中混入少量乙时,可用冷却热饱和溶液的方法得到较纯净的甲
D.t2 ℃时甲、丙两物质的饱和溶液降温到t1 ℃时,二者所得溶液的溶质质量分数一定相等
5.如图是甲、乙、丙三种物质的溶解度曲线。下列叙述正确的是( )
A.t1 ℃时,等质量的甲、丙溶液中所含溶质的质量大小关系为丙>甲
B.t2 ℃时,20 g丙溶解于50 g水中能形成70 g溶液
C.分别将三种物质的饱和溶液从t3 ℃降温至t2 ℃时,所得溶液溶质质量分数的大小关系为乙>甲=丙
D.若要将组成在N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
6.20 ℃时,将等质量的a、b两种固体,分别加入到盛有100 g水的烧杯中,充分搅拌后现象如图1,升温到 50 ℃时,现象如图2,a、b两种物质的溶解度曲线如图3。下列说法正确的是( )
8
A.图3中M表示b的溶解度曲线
B.图1溶液中溶质的质量分数a大于b
C.图2中a、b溶液一定是不饱和溶液
D.30 ℃时a、b溶液溶质质量分数不相等
7.如图表示甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )
A.t2 ℃时,甲、乙溶液中溶质质量分数一定相等
B.乙中含有少量甲,可采用降温结晶的方法提纯乙
C.t3 ℃时,甲、乙、丙三种物质的饱和溶液降温到t1 ℃,所得溶液中溶质质量分数的大小关系为乙>丙>甲
D.t2 ℃时,100 g甲的饱和溶液中加入400 g水,得到10%的甲溶液
8.两个烧杯中分别盛装X、Y的饱和溶液,两支试管中分别装有NaOH和NH4NO3固体,向两支试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( )
A.Y的溶解度曲线为b曲线
B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2 ℃降温到t1 ℃,溶质的质量分数变大
8
D.t3 ℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
9.如图为KNO3的溶解度曲线,a、b在溶解度曲线上。
(1)a点对应的溶液是________(填“饱和”或“不饱和”)溶液。
(2)a点对应的溶液的质量分数是___________________(只列计算式)。
(3)将a点对应的溶液升温到70 ℃,其质量分数________(填写“变大”“变小”或“不变”)。
(4)欲使KNO3溶液的状态从b点转化为c点,可采取的措施是____________。
10.如图是A、B、C三种物质的溶解度曲线,请根据此图回答下列问题:
(1)________℃时,物质A和C的溶解度相等。
(2)等质量的A、B、C三种物质的饱和溶液分别从t2 ℃降温至t1 ℃,溶液质量没有发生改变的是______。
(3)接近饱和的C溶液,在保持溶质质量分数不变的情况下转变为饱和溶液,可采取的方法是____________。
(4)t1 ℃时,B物质溶液中溶质的质量分数可能为________。
A.20% B.25%
C.28.7% D.30%
11.已知氯化钠、碳酸钠在不同温度时的溶解度如下:
温度/℃
0
10
20
30
40
溶解度/g
氯化钠
35
35.5
36
36.5
37
碳酸钠
6
10
18
36.5
50
8
(1)依据表中数据,绘制出氯化钠和碳酸钠的溶解度曲线(如图),图中能表示碳酸钠溶解度曲线的是______(填“A”或“B”)。
(2)图中两溶解度曲线相交于M点,此点表示的意义是____________________________________________。
(3)40 ℃时,把50 g A物质放入100 g水中,充分搅拌,所得溶液是________溶液(填“饱和”或“不饱和”)。
(4)生活在盐湖(主要成分是NaCl和Na2CO3)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”。请你答出“冬天捞碱”的道理____________________________________________________________________
__________________________________________________________________。
12.已知A、B、C三种物质的溶解度曲线如图所示。
(1)在阴影区域部分,处于不饱和状态的是______(填“A”“B”或“C”)。
(2)若在饱和A溶液中含有少量的C,提纯A的方法为________结晶,过滤。
(3)P点表示的含义为______________________________________。
(4)在t1 ℃下,B、C的饱和溶液升温至t2 ℃,所得溶液溶质的质量分数大小关系为_____________________________________________________________。
13.图中A、B、C分别表示三种不同的固体物质,其溶解度曲线如图所示。请回答下列问题:
(1)这三种物质的溶液中,适用于海水晒盐原理进行结晶提纯的是______。
8
(2)在t2 ℃时,将质量均为25 g的上述三种物质分别加入到100 g水中,不能形成饱和溶液的是________,此时A溶液的溶质质量分数为__________。
(3)在t2 ℃时,将足量的三种物质的饱和溶液各蒸发10 g水后再冷却到t2 ℃,它们析出晶体的质量分别为m(A)、m(B)和m(C),则三者的大小关系是________________________________。
(4)将t2 ℃的这三种物质的饱和溶液分别降温至t1 ℃,所得溶液中溶质的质量分数分别是w(A)、w(B)和w(C),则三者的大小关系是________________________________。
14.R是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验。
(1)t1 ℃时,氯化铵的溶解度为________g。
(2)①的溶液中溶质质量分数为__________。
(3)根据以上信息可推出R是________________________(写名称或化学式均可)。
(4)关于图2中烧杯内的物质,以下几种说法正确的有________。
A.①②③中,只有③中上层清液是饱和溶液
B.③中的固体溶解,可采用加水或升温的方法
C.①和②的溶液中,溶质质量相等
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小
15.图1是三种常见物质的溶解度曲线。请回答以下问题。
8
(1)由图1可知,30 ℃时硝酸钾的溶解度是________g。
(2)图1所示三种物质中溶解度随温度升高而减小的物质是____________(填名称)。
(3)若氯化钠固体中混有少量硝酸钾,提纯氯化钠的方法是____________(填“降温结晶”或“蒸发结晶”)。
(4)现有40 ℃时等质量的硝酸钾、氯化钠饱和溶液,加热蒸发等质量的水后恢复至40 ℃,剩余溶液的质量关系大小为硝酸钾______(填“>”“=”或“<”)氯化钠。
(5)若a、b、c分别代表上述三种物质,图2是在室温下,烧杯中a物质的溶液、试管①中b物质的溶液和试管②中c物质的溶液的状态。当从室温升至60 ℃时,发现烧杯中a物质没有明显变化,试管①中b物质全部溶解,试管②中有c物质析出,写出a、b、c三种物质的化学式:a____________,b______________,c__________________。
参考答案
8
1.A 2.B 3.B 4.D 5.D 6.C 7.C 8.D
9.(1)饱和 (2)×100%
(3)不变 (4)增加溶剂
10.(1)t1 (2)C (3)升高温度
(4)AB
11.(1)A (2)在30 ℃时,氯化钠和碳酸钠的溶解度相等
(3)饱和
(4)碳酸钠的溶解度随温度的降低减小明显
12.(1)B (2)降温 (3)t1 ℃时,B、C物质的溶解度相等
(4)B>C
13.(1)B (2)AB 20% (3)m(C)<m(B)<m(A)
(4)w(B)>w(A)>w(C)
14.(1)40 (2)25% (3)硝酸钾(或KNO3) (4)BC
15.(1)45 (2)氢氧化钙 (3)蒸发结晶 (4)< (5)NaCl KNO3 Ca(OH)2
8