- 104.50 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
水溶液中的离子平衡(一)
★ 备注:以下选择题均为双选
1、25℃时,某浓度的NH4Cl溶液pH = 4,下列叙述正确的是 ( )
A.溶液中的 c(OH-) = 1×10-10 mol·L-1
B.溶液中的c(NH4+)>c(Cl-)>c(H+)>c(OH-)
C.溶液中的c(H+) + c(NH4+) = c(Cl-) + c(OH-)
D.溶液中的c(NH3·H2O) = c(NH4+)
2.对于常温下pH=3的乙酸溶液,下列说法正确的是 ( )
A.与等体积、pH=3的盐酸比较,跟足量锌粒反应产生的H2更多
B.加水稀释到原体积的10倍后溶液pH变为4
C.加入少量乙酸钠固体,溶液pH升高
D.加水稀释后,溶液中c(H+)和c(OH-)都减小
3.在一定条件下Na2CO3溶液存在水解平衡:CO32-+H2OHCO3-+OH-。下列说法正
确的是 ( )
A.Na2CO3溶液中:2c(Na+)= c(CO32-)+ c(HCO3-)+ c(H2CO3)
B.加入NaOH固体,溶液中c(Na +)和c(CO32-)都增大
C.稀释Na2CO3溶液,溶液中的离子浓度都减少
D.升高温度,Na2CO3溶液pH增大
4、对于常温下pH为12的氢氧化钠溶液,叙述正确的是 ( )
A.将此溶液稀释106倍,溶液的pH=6
B.与等体积等浓度的氯化铵溶液混合后所得溶液呈中性
C.与pH=2的CH3COOH溶液任意比混合: c(H+) + c(Na+) =c(OH-) + c(CH3COO-)
D.与0.01 mol·L-1 的CH3COOH溶液等体积混合所得溶液中:
c (Na+)>c(CH3COO-)>c(OH-)>c(H+)
5. 下列关于pH=12的Na2CO3溶液说法正确的是 ( )
A. 升高溶液温度,溶液pH增大 B. c(Na+) +c(H+)=c(CO32-)+ c(HCO3-)+ c(OH-)
C. 溶液中c(OH-)>c(HCO3-)> c(H+) D. 2c(Na+)=c(CO32-)+ c(HCO3-)+ c(H2CO3)
6.HA为一元弱酸,在0.1 mol·L-1NaA溶液中,下列说法正确的是:( )
A.室温下,该溶液的pH=7 B.适当加热该溶液,溶液的PH值升高
①
pH
V(HCl)/mL
10
20
7
②
③
C.c(Na+)> c(A-)> c(H+)> c(OH-) D.c(Na+)+ c(H+)= c(A-)+ c(OH-)
7.常温下,用0.1000 mol/L HCl溶液滴定20.00 mL 0.1000 mol/L NH3•H2O溶液,滴定曲线如下图。下列说法正确的是 ( )
A.①溶液:c(C1—)>c(NH4+)>c(OH—)>c(H+)
B.②溶液:c(NH4+) = c(C1—)>c(OH—) = c(H+) C.③溶液:c(OH—)>c(H+)
D.滴定过程中可能出现:c(NH3•H2O)>c(NH4+)>c(OH—)>c(Cl—)>c(H+)
8.常温下,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液②NaOH溶液③CH3COONa溶液,下列说法中正确的是(忽略混合前后溶液体积变化) ( )
A.溶液的pH值:②>③>① B.水电离出的c(OH-):③>①=②
C.①和③等体积混合后的溶液:c(CH3COOH)+ c(CH3COO-)=0.1mol/L
D.②和③等体积混合后的溶液:c(Na+)=c(CH3COOH)+c(CH3COO-)
9.常温下,100ml 蒸馏水中加入0.1mol CH3COONa ,下列说法正确的是 ( )
A、该溶液中存在: c(Na+) + c(H+)=c(OH—)+c(CH3COO—)
B、加入酚酞后加热,溶液颜色变浅
C、若在该溶液再通入0.1mol HCl,存在: c(Na+)>c(CH3COO—)> c(H+)
D、若在该溶液中再投入0.1mol NaCl,存在: c(Na+)=c(Cl—)+c(CH3COO—)+c(CH3COOH)
10.下列各溶液中,微粒的物质的量浓度关系正确的是
A.常温下,将pH=2的盐酸和pH=12的氨水等体积混合后:
c(NH4+)>c(Cl-)> c(OH-)>c(H+)
B.0.1 mol·L-1 Na2CO3溶液:c(Na+)=2c(HCO)+2c(CO32¯)+2c(H2CO3)
C.0.1 mol·L-1 NH4Cl溶液:c(NH)=c( Cl-)
D.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
11.下列各溶液的叙述中不正确的是
pH
a
b
c
Ⅰ
Ⅱ
溶液体积
A.等pH的硫酸与醋酸稀释后pH的变化如右图所示,
则曲线Ⅱ表示的是醋酸的稀释图像
B.溶有等物质的量的NaClO、NaHCO3的溶液中:
c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
C.若NH4HCO3溶液、NH4HSO4溶液中c(NH4+)相等,则:
c(NH4HSO4)﹥c(NH4HCO3)
D.已知某温度下Ksp(CH3COOAg) = 2.8×10-3,浓度均为0.1 mol·L-1的AgNO3溶液和CH3COONa溶液等体积混合一定能产生CH3COOAg沉淀
12.下列叙述正确的是 ( )
A.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
B.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-)+c(CH3COOH)=2c(Na+)
C.常温下,向NH4Cl溶液中加入氨水至溶液的pH=7,此时溶液中c(NH4+)>c(C1-)
D.0.1mol·L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(OH-)>c(H+)
13、常温下,下列溶液中的微粒浓度关系正确的是( )
A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO)>c(CO)>c(H2CO3)
C.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)=c(NH)>c(OH-)=c(H+)
D.0.1 mol·L-1CH3COONa溶液中:c(OH-)=c(CH3COOH)+c(H+)
14. 常温时,下列各溶液中,离子的物质的量浓度关系正确的是( )
A.饱和碳酸钠溶液中:c(Na+)= 2c(CO32-)+ 2c(HCO3-)+2c(H2CO3)
B.pH=2的醋酸中:c(H+)=0.02mol•L-1
C.0.1 mol•L-1氯化铵溶液中: c(Cl-)> c(NH4+) >c(H+)> c(OH-)
D.pH=12的NaOH溶液与等体积0.01 mol·L-1氯化铵溶液混合后所得溶液中:c(Na+) = c(NH)
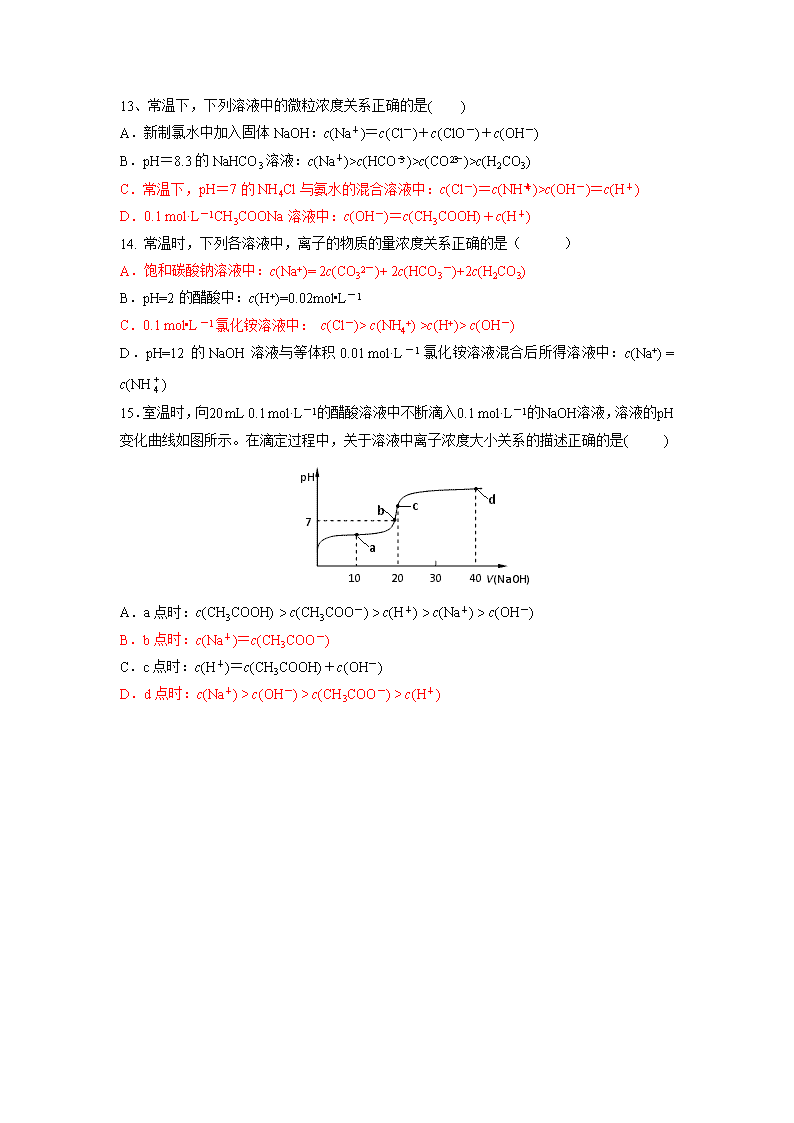
15.室温时,向20 mL 0.1 mol·L-1的醋酸溶液中不断滴入0.1 mol·L-1的NaOH溶液,溶液的pH
变化曲线如图所示。在滴定过程中,关于溶液中离子浓度大小关系的描述正确的是( )
40
V(NaOH) (mL)
pH
30
20
10
7
b
d
c
a
A.a点时:c(CH3COOH) > c(CH3COO-) > c(H+) > c(Na+) > c(OH-)
B.b点时:c(Na+)=c(CH3COO-)
C.c点时:c(H+)=c(CH3COOH)+c(OH-)
D.d点时:c(Na+) > c(OH-) > c(CH3COO-) > c(H+)
水溶液中的离子平衡(二)
★ 备注:以下选择题均为双选
1.现有常温下的四份溶液:①0.01 mol·L-1 CH3COOH;②0.01 mol·L-1 HCl;③pH=12的氨水;④pH=12的NaOH溶液。下列说法正确的是( )
A.①中水的电离程度最小,③中水的电离程度最大
B.将②、③混合,若有pH=7,则消耗溶液的体积:②>③
C.将①、④混合,若有c(CH3COO-)>c(H+),则混合液一定呈碱性
D.将四份溶液分别稀释100倍后,溶液的pH:③>④,①>②
2.下列有关电解质溶液中微粒的关系不正确的是( )
A.25℃时,pH=4的氯化铵溶液中:c(NH4+)>c(Cl-)>c(H+)>c(OH-)
B.25℃时,pH=3的氯化铵溶液中: c(OH-)=1.0×10-11mol·L-1
C.将pH=5的醋酸溶液稀释后,恢复至原温度,pH和Kw均增大
D.向NH4HSO4溶液中加入等物质的量的NaOH形成的溶液中:
c(Na+) = c(SO42-) >c(NH4+) >c(H+) > c(OH-)
3.50℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
A.pH=4的醋酸中:c(H+)=4.0 mol·L-1
B.饱和小苏打溶液中:c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3)
C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+ c(OH-)
D. pH=12的纯碱溶液中:c(OH-)=1.0×10-2 mol·L-1
4.有关下列溶液的叙述正确的是( )
A.醋酸与醋酸钠的混合溶液中:c(CH3COO-) + c(OH-) = c(Na+) + c(H+)
B.1 mol·L-1Na2CO3溶液中:c(OH-) = c((H+) + c(HCO3-) + c(H2CO3)
C.0.1 mol·L-1的硫酸铵溶液中: c(SO42-) >c(NH4+)>c(H+)> c(OH-)
D.将1molKCl、1molNaHS溶于水配成1L混合溶液中:
n(K+) = n(S2-)+n(HS-)+n(H2S) = 1mol
5.下列叙述正确的是( )
A.相同温度下,中和pH=1的盐酸和醋酸各20.0mL,需要0.100 mol·L-1NaOH都是20.0mL
B.0.1mol·L-1Na2CO3中加入少量NaOH固体后振荡,c(Na+)和c(CO32-)都增大
C.常温下,向AgCl悬浊液中加入少量NaCl固体后振荡,Ksp(AgCl)增大
D.相同浓度的CH3COOH和 CH3COONa溶液等体积混合后,则:
c(CH3COO-)+ c(CH3COOH) = 2c(Na+)
6.在25℃时,将0.2molCH3COONa晶体和0.1molHCl气体同时溶解于同一烧杯的水中,制
得1L溶液,若此溶液中c(CH3COO—)>c(Cl—),则下列判断不正确的是( )
A.该溶液的pH大于7
B.c(CH3COOH)+c(CH3COO—)=0.20mol·L—1
C.c(CH3COOH)②>③
13.下列各溶液中,微粒的物质的量浓度关系正确的是
A.对于0.1mol/L的Na2CO3溶液:2c(CO)+2c(H2CO3)+2c(HCO)=c(Na+)
B.向0.1 mol·L-1 CH3COOH溶液滴入少量NaOH,促进CH3COOH电离,溶液pH降低
C.对于Na2SO3溶液,若升高温度,溶液的pH降低
D.常温下,将pH=2的盐酸和pH=12的氨水等体积混合后:
c(NH4+)>c(Cl-)> c(OH-)>c(H+)
相关文档
- 高考化学一轮复习 专题 过氧化钠的2021-05-134页
- 2019人教版高考物理一轮优练题12及2021-05-136页
- 2019届高考数学一轮复习 第3讲 平2021-05-133页
- 高考物理第一轮复习 曲线运动 提高2021-05-136页
- (浙江专版)2020高考语文一轮复习 专2021-05-137页
- 2020版高考化学一轮复习 全国卷热2021-05-134页
- 2013高考英语一轮复习方略 素能提2021-05-136页
- 高考地理一轮复习考点练习卷地球的2021-05-133页
- 2020版高考地理一轮总复习 第十二2021-05-136页
- 高考化学一轮复习真题考点集训气体2021-05-1311页