- 784.50 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
知识梳理:要描述一个电子的运动状态,应从四个方面来描述_____、______、______、______
第n能层有___个能级,每能层有__个轨道,
每个轨道最多容纳__个电子
能层
1
2
3
4
5
6
7
能层符号
能级符号
轨道数
各能级、能层最多容纳电子数
所含电子自旋方向
(2007海南·25)A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为 ;
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为 ,C的元素符号为 ;
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为 ,其基态原子的电子排布式为 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为 ,其基态原子的电子排布式为 。
(09年福建理综·30)[化学——物质结构与性质](13分)
Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
回答下列问题:
(1)Z2+ 的核外电子排布式是 。
(2)在[Z(NH3)4]2+离子中,Z2+的空间轨道受NH3分子提供的 形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
a.稳定性:甲>乙,沸点:甲>乙
b.稳定性:甲>乙,沸点:甲>乙
c.稳定性:甲<乙,沸点:甲<乙
d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)
(5)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为 。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 。
知识梳理:Abn型分子中孤电子对数目=_______________________
比较分子中键角大小的方法_______________________________
1.(09年海南化学·19.3)下列说法中错误的是:
A.SO2、SO3都是极性分子
B.在NH4+ 和[Cu(NH3)4]2+中都存在配位键
C.元素电负性越大的原子,吸引电子的能力越强
D.原子晶体中原子以共价键结合,具有键能大熔点高硬度大的特性
.(2007海南·23)用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是( )
A.直线形;三角锥形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
3.(08年海南化学·22)在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是
A.sp,范德华力 B.sp2,范德华力C.sp2,氢键 D.sp3,氢键
4.(08年宁夏理综·35)X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键 ____________________________________________________ 。
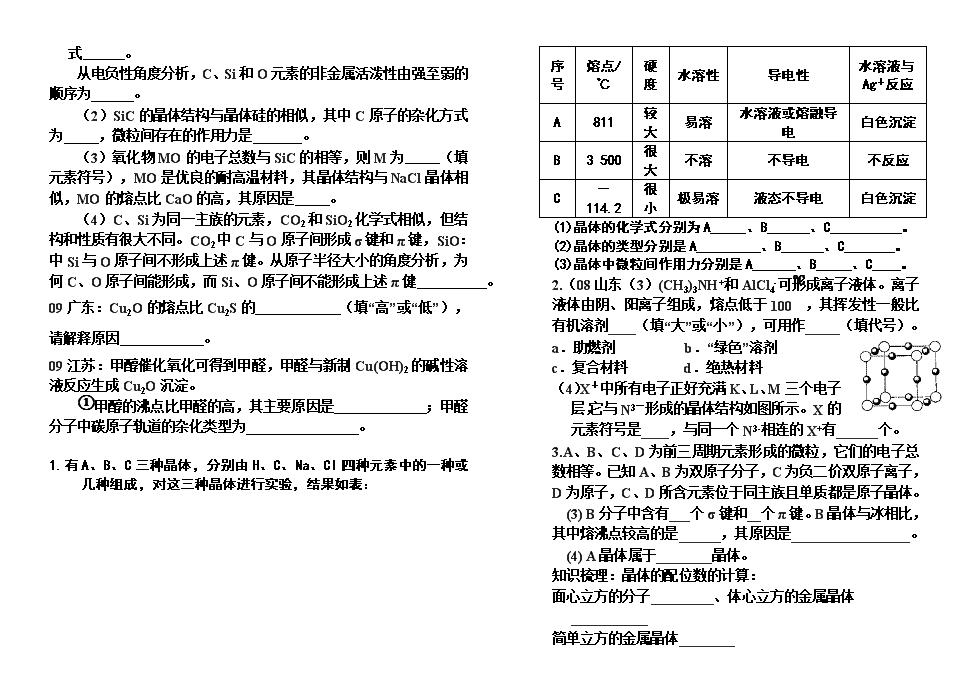
(08年广东化学·27。(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如下图所示,请改正图中错误: 。
(3)用镁粉、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因: 。
氧化物
NaF
MgF2
SiF4
熔点/K
1266
1534
183
(4)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
解释表中氟化物熔点差异的原因: _____ __________ 。
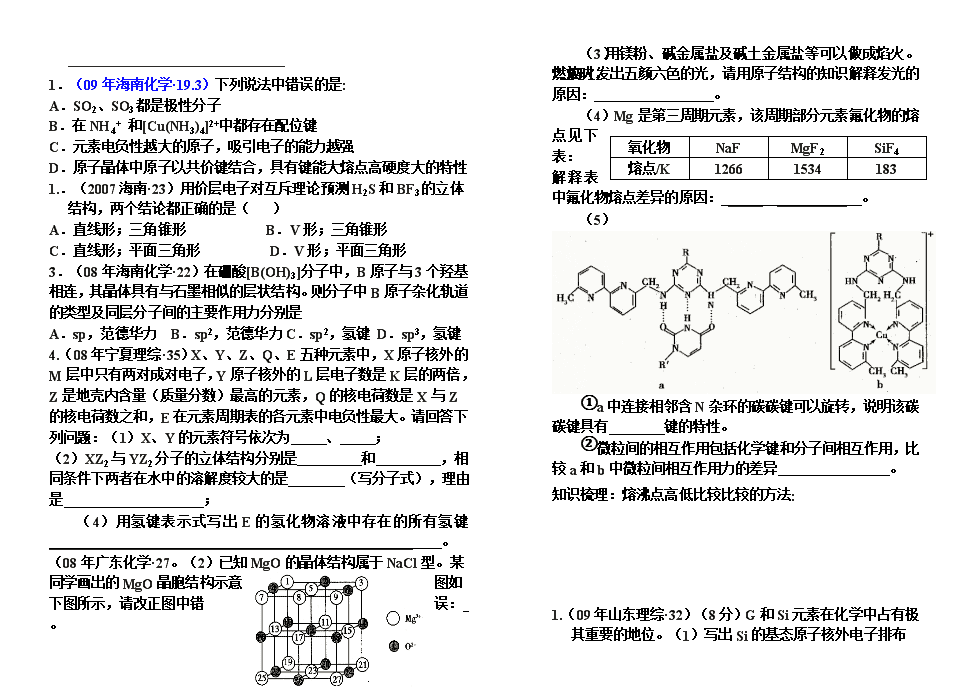
(5)
①a中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有 键的特性。
②微粒间的相互作用包括化学键和分子间相互作用,比较a和b中微粒间相互作用力的差异 。
知识梳理:熔沸点高低比较比较的方法:
1.
(09年山东理综·32)(8分)G和Si元素在化学中占有极其重要的地位。(1)写出Si的基态原子核外电子排布式 。
从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为 。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为 ,微粒间存在的作用力是 。
(3)氧化物MO的电子总数与SiC的相等,则M为 (填元素符号),MO是优良的耐高温材料,其晶体结构与NaCl晶体相似,MO的熔点比CaO的高,其原因是 。
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO:中Si与O原子间不形成上述π健。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π健 。
09广东:Cu2O的熔点比Cu2S的 (填“高”或“低”),请解释原因 。
09江苏:甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是 ;甲醛分子中碳原子轨道的杂化类型为 。
1.有A、B、C三种晶体,分别由H、C、Na、Cl四种元素中的一种或几种组成,对这三种晶体进行实验,结果如表:
序号
熔点/℃
硬度
水溶性
导电性
水溶液与Ag+反应
A
811
较大
易溶
水溶液或熔融导电
白色沉淀
B
3 500
很大
不溶
不导电
不反应
C
-114.2
很小
极易溶
液态不导电
白色沉淀
(1)晶体的化学式分别为A_____、B______、C__________。
(2)晶体的类型分别是A_________、B______、C_______。
(3)晶体中微粒间作用力分别是A______、B_____、C____。
2.(08山东(3)(CH3)3NH+和AlCl4-可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂____(填“大”或“小”),可用作_____(填代号)。
a.助燃剂 b.“绿色”溶剂
c.复合材料 d.绝热材料
(4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是____,与同一个N3-相连的X+有______个。
3.A、B、C、D为前三周期元素形成的微粒,它们的电子总数相等。已知A、B为双原子分子,C为负二价双原子离子,D为原子,C、D所含元素位于同主族且单质都是原子晶体。
(3) B分子中含有___个σ键和__个π键。B晶体与冰相比,其中熔沸点较高的是______,其原因是_________________。
(4) A晶体属于________晶体。
知识梳理:晶体的配位数的计算:
面心立方的分子_________、体心立方的金属晶体___________
简单立方的金属晶体________
1.(12分)最近,由镁、镍和碳三种元素组成的化合物引起了科学家的注意。
(1)写出镍原子基态的电子排布式 。
(2)已知一氧化碳与N2是等电子体,写结构式 ,
(3)四羰基镍【Ni(CO)4】为无色挥发性剧毒液体。熔点-25℃。沸点43℃。不溶于水,易溶于乙醇、乙醚、苯、四氯化碳等有机溶剂,呈四面体构型。四羰基镍的晶体类型是 ,镍原子和羰基之间的作用力为 。
图中:碳原子用小球,镍原子用大球,
镁原子用大球
(4)据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积(ccp)如图,试写出该晶体的化学式 。晶体中每个镁原子周围距离最近的镍原子有 个。
2.下列图象是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断NaCl晶体结构的图象是
晶体(晶胞)密度的计算
计算公式
——————————————————
1.XY晶体的单元结构如下图所示,晶体中距离最近的X+与Y-的核间距离为a cm,已知阿伏加德罗常数为NA mol-1,其密度为ρ g·cm-3,则XY的摩尔质量可表示为________ g·mol-1。
设该晶体的摩尔质量为M g·mol-1,晶体密度为ρ·cm-3,阿伏加德罗常数为NA则晶体中两个距离最近的X中心间的距离为__________ 。
晶体结构
1.下图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。
(1)其中代表金刚石的是(填编号字母,下同)________,金刚石中每个碳原子与________个碳原子最接近且距离相等。金刚石属于________晶体;
(2)其中代表石墨是________,其中每个正六边形占有的碳原子数平均为________个;
(3)代表干冰的是________,它属于________晶体,每个CO2分子与________个CO2分子紧邻;
(4)上述三种物质熔点由高到低的排列顺序为________。
2.下列各项所述的数字不是6的是
A.在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数
B.在金刚石晶体中,最小的环上的碳原子个数
C.在二氧化硅晶体中,最小的环上的原子个数
D.在石墨晶体的片层结构中,最小的环上的碳原子个数
3.下面有关离子晶体的叙述中,不正确的是
A.1mol氯化钠中有NA个NaCl分子
B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个
C.氯化铯晶体中,每个CS+周围紧邻8个Cl-
D.平均每个NaCl晶胞中有4个Na+、4个Cl-
(08年江苏化学·21A)(12分)
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)B的氢化物的分子空间构型是 。其中心原子采取 杂化。
(3)一种由B、C组成的化合物与AC2互为等电子体,其化学式为 。
(4)E的核外电子排布式是 ,ECl3形成的配合物的化学式为 。
08江苏:答案:(12分) (1)C<O<N (2)三角锥形 sp3(3) N2O
(4)1s22s22p63s23p63d54s1(或[Ar] 3d54s1) [Cr(NH3)4(H2O)2]Cl3
解析:A:化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,推知C为氧元素,D为镁元素,AC2为非极性分应为二氧化碳,A为碳元素。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高,推出B氮元素,NH3分子空间构型是三角锥形,氮原子sp3杂化,E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界,E为铬元素,二氧化碳分子应满足8电子稳定态。
(08年广东化学·27)答案:(10分)(物质结构选做题)
(1)增大离子浓度,从而增大熔融盐的导电性
(2)⑧应为黑色
(3)原子核外电子按一定轨道顺序排列,轨道离核越远,能量越高。燃烧时,电子获得能量,从能量较低的轨道跃迁到能量较高的另一条轨道。跃迁到新轨道的电子处在一种不稳定的状态,它随即就会跳回原来的地能量轨道,并向外界释放能量(光能)
(4)NaF与MgF2为离子晶体,SiF4为分子晶体,所以NaF与MgF2远比SiF4熔点要高。又因为Mg2+的半径小于Na+的半径,所以MgF2的离子键强度大于NaF的离子键强度,故MaF2的熔点大于NaF。
(5)①σ键 ②a中存在氢键和范德华力,b中存在配位键
解析:(1) 以MgCl2为原料用熔融盐电解法制备Mg时,常加入NaCl、KCl、或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有:增大离子浓度,从而增大熔融盐的导电性。
(2) 请更正图中错误:⑧应为黑色。
(3) 请用原子结构的知识解释发光的原因:原子核外电子按一定轨道顺序排列,轨道离核越远,能量越高。燃烧时,电子获得能量,从内侧轨道跃迁到外侧的另一条轨道。跃迁到新轨道的电子处在一种不稳定的状态,它随即就会跳回原来轨道,并向外界释放能量(光能)。
(4) 解释表中氟化物熔点差异的原因:NaF与MgF2为离子晶体,SiF4为分子晶体,所以NaF与MgF2远比SiF4熔点要高。又因为Mg2+的半径小于Na+的半径,所以MgF2的离子键强度大于NaF的离子键强度,故MaF2的熔点大于NaF。
(5) ①a中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有:σ键的特性。
②微粒间的相互作用包括化学键和分子间相互作用,比较a和b中微粒间相互作用的差异:a中微粒间的相互作用为氢键,b中微粒间的相互作用为配位共价键。
09山东答案:(1)1s22s2sp63s23p2 O>C>Si(2)sp3 共价键(3)Mg Mg2+半径比Ca2+小,MgO的晶格能大(4)C的原子半径较小,C、O原子能充分接近,p—p轨道肩并肩重叠程度较大,形成较稳定的π键。而Si原子半径较大,Si、O原子间距离较大,p—p轨道肩并肩重叠程度较小,不能形成稳定的π键
相关文档
- 高考选修33热学计算题训练2021-05-1312页
- 历史选修一改革全国卷高考题整理A2021-05-137页
- 高考地理一轮复习作业选修旅游地理2021-05-135页
- 2020-2021年高考生物一轮复习知识2021-05-136页
- 2019高考生物二轮专题跟踪训练5基2021-05-136页
- 优化方案2011高考英语一轮复习 uni2021-05-136页
- 高考生物总复习 专题 微生物的培养2021-05-138页
- 新课标高考有机专题复习选修5羧酸2021-05-136页
- 2014年版高考生物选修专题目综合测2021-05-1310页
- 新课标高考生物二轮复习专题一细胞2021-05-137页