- 752.50 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2011年普通高等学校招生全国统一考试理科综合能力测试
(全国2卷化学部分)
6.等浓度的下列稀溶液:①乙酸、②苯酚、③碳酸、④乙醇,它们的pH由小到大排列正确的是
A.④②③① B.③①②④ C.①②③④ D.①③②④
【解析】选D。依据酸性强弱的大小顺序:乙酸>碳酸>苯酚>乙醇,知D项正确。
7.下列叙述错误的是
A.用金属钠可区分乙醇和乙醚
B.用高锰酸钾酸性溶液可区分己烷和3--己烯
C.用水可区分苯和溴苯
D.用新制的银氨溶液可区分甲酸甲酯和乙醛
【解析】选D。钠和乙醇反应有气泡产生,而钠和乙醚不反应,A正确;3--己烯可以使高锰酸钾酸性溶液褪色,而己烷不能,B正确;苯的密度比水小,而溴苯的密度比水大,用水可以区分,C正确;甲酸甲酯分子结构中也含有醛基,故用新制的银氨溶液不能区分甲酸甲酯和乙醛,D错误。
8.在容积可变的密闭容器中,2molN2和8molH2在一定条件下发生反应,达到平衡时,H2的转化率为25%,则平衡时氮气的体积分数接近于
A. 5% B.10% C.15% D.20%
【解析】选C。依据三行式,平衡时N2、H2、NH3,的物质的量分别为4/3、6、4/3, N2的物质的量分数约等于15%,故氮气的体积分数接近于15%,故C项正确。
9.室温时,将浓度和体积分别为c1、V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是
A. 若pH>7,则一定是c1V1=c2V2
B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-) +c(OH-)
C.当pH=7时,若V1=V2,一定是c2>c1
D.若V1=V2,c1=c2,则c(CH3COO-) +c(CH3COOH)=c(Na+)
【解析】选A。当NaOH和CH3COOH按照等物质的量反应时,形成的是强碱弱酸盐,显碱性,pH>7,而NaOH过量时,其pH也大于7,A错误;由电荷守恒关系式可知,B正确;当pH=7时,CH3COOH的物质的量大于NaOH的物质的量,若V1=V2,一定是c2>c1,C正确;若V1=V2,c1=c2,则NaOH和CH3COOH恰好中和,依据物料守恒,知D正确。
10.用石墨作电极电解CuSO4溶液。通电一段时间后,欲使电解质溶液恢复到起始状态,应向溶液中加入适量的
A.CuSO4 B.H2O C.CuO D.CuSO4·H2O
【解析】选C。依据电解方程式2CuSO4+2H2O2Cu+O2↑+2H2SO4,欲使电解质溶液恢复到起始状态,应向溶液中加入适量的CuO。
11.将足量的CO2通入下列各溶液中,所含离子还能大量共存的是
A.K+、SiO32-、Cl-、NO3- B.H+、NH4+、Al3+、SO42-
C.Na+、S2-、OH-、SO42- D.Na+、C6H5O-、CH3COO-、HCO3-
【解析】选B。CO2通入溶液中相当于存在碳酸,碳酸的酸性大于硅酸,A中的SiO32-不能大量共存;C中的OH-不共存;D中的C6H5O-会和CO2反应形成苯酚,故只有B中离子还能大量共存。
12.NA为阿伏加德罗常数,下列叙述错误的是
A.18 g H2O中含有的质子数为10NA
B.12 g金刚石中含有的共价键数为4 NA
C.46 g NO2和N2O4混合气体中含有的原子总数为3 NA
D.1 mol Na与足量的O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
【解析】选B。一个H2O分子中含有10个质子,故18 g H2O中含有的质子数为10NA,A正确;金刚石的结构为正四面体构型,每个碳原子可以和另外的4个碳原子形成共价键,属于每个碳原子的共价键为2个,故12 g金刚石中含有的共价键数应为2 NA,B错误;46 g NO2和N2O4混合气体中,不管46 g NO2 还是46 g N2O4,其物质的量分别是1mol、0.5mol,所含有的原子总数都为3 NA,C正确;1 mol Na与足量的O2反应,钠必然消耗完全,其转移的电子的物质的量为1mol,数目为NA,D正确。
13.某含铬(Cr2O72-)废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀经干燥后得到n mol FeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是
A.消耗硫酸亚铁的物质的量为n(2-x)
B.处理废水中的Cr2O72-的物质的量为nx/2
C.反应中发生转移的电子数为3nxmol
D.在FeO·FeyCrxO3中,3x=y
【解析】选D。依据铬、铁元素反应前后的价态以及化合物的化学式中正负化合价的代数和为0的原则,易知FeO·FeyCrxO3中的x、y的值相等且等于1,故D项错误;A、B、C项正确。
27.(15分)(注意:在试卷上作答无效)
下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:①反应能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:,F中E元素的质量分数为60%。
回答问题:⑴①中反应的化学方程式为 ;
⑵化合物I的电子式为 ,它的空间结构是 ;
⑶1.6 g G溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需的铜粉的质量(写出离子方程式和计算过程);
⑷C与过量NaOH溶液反应的离子方程式为 ,反应后溶于与过量化合物I反应的离子方程式为 。
⑸E在I中燃烧观察到的现象是 。
【解析】依据题目信息C、B是单质,G、H是二元化合物,且反应曾应用于铁轨的焊接,知C为Al、G为Fe2O3、B为Fe、H为Al2O3;由于I是一种常见的温室气体,知其为CO2,而Mg能在CO2中燃烧,且MgO中Mg元素的质量分数为60% ,知E为Mg,F为MgO,D为碳单质,A为氧气。
【答案】⑴ 4Al+ 2Fe2O34Fe+ 2Al2O3
⑵ 直线型
⑶ n(Fe2O3)=0.01 mol,n(Fe3+)=0.02 mol,依据离子方程式2Fe3++Cu=2 Fe2++ Cu2+ ,则n(Cu )= 0.01 mol,m(Cu )=0.64 g.。
⑷ 2 Al + 2OH- + 2 H2O=2AlO2- + 3H2↑ AlO2- + CO2 + 2H2O = Al(OH)3↓+ HCO3-
⑸ 剧烈燃烧,放出热量,生成黑色固体和白色固体。
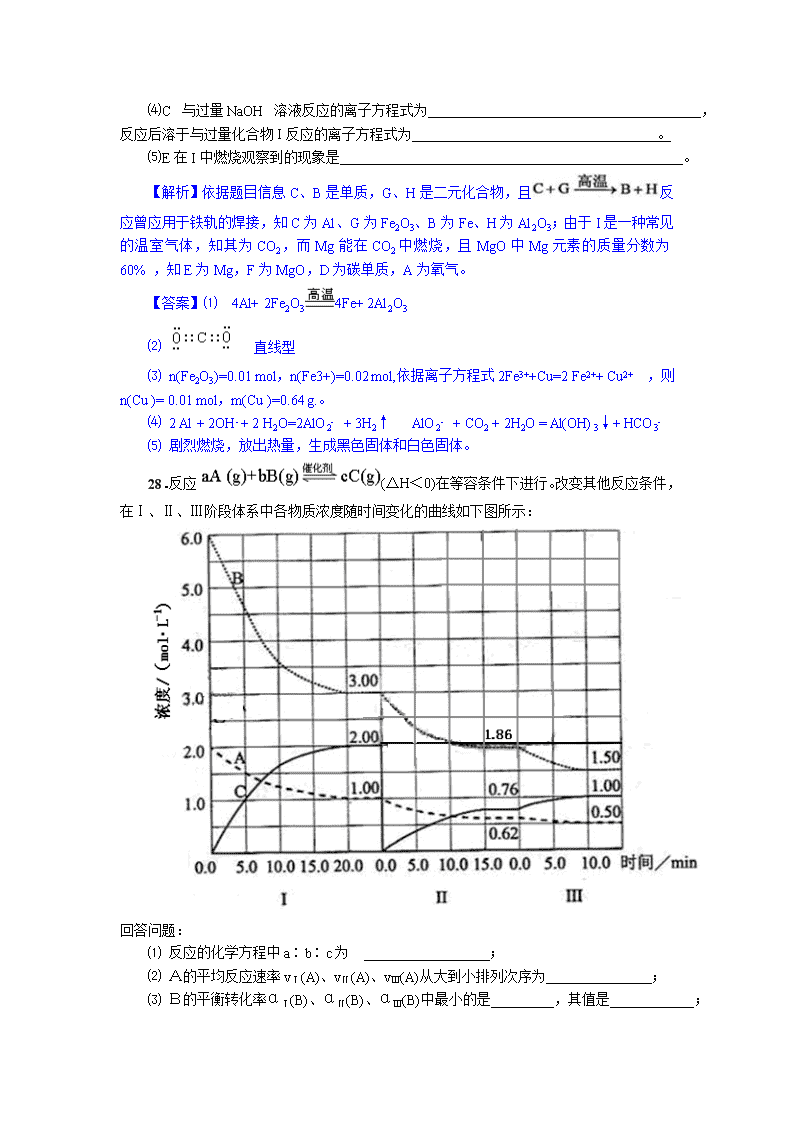
28.反应(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
回答问题:
⑴ 反应的化学方程中a∶b∶c为 ;
⑵ A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为 ;
⑶ B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是 ,其值是 ;
⑷ 由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是 ;
⑸ 比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低;T2 T3(填“<”“>”“=”)判断的理由是 。
⑹ 达到第三次平衡后,将容器的体积扩大一倍,假定10 min后达到新的平衡,请在下图中用曲线表示第Ⅳ阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C)。
【解析】⑴ 依据图示第一次达到平衡时,A、B、C三种物质的物质的量的变化分别为1mol、3 mol、2 mol,故a∶b∶c=1∶3∶2。
⑵ vⅠ(A)=(2.0-1.00)mol·L-1/20.0min=0.05 mol·L-1·min-1、vⅡ(A)=(1.00-0.62)/15.0 min=0.025 mol·L-1·min-1、vⅢ(A)=( 0.62-0.50) mol·L-1/10 min=0.012 mol·L-1·min-1。故大小顺序为vⅠ(A) >vⅡ(A) >vⅢ(A)。
⑶ 由图可知αⅠ(B)=0.5、αⅡ(B)=1.14/3.00=0.38、αⅢ(B)=0.36/1.86=0.19,则B的平衡转化率最小的是αⅢ(B),其值为0.19。
⑷ 第一次平衡后,A、B的浓度从平衡点开始降低,而C的物质的量浓度突然变为0,则平衡向右移动,此时采取的措施是将C从平衡混合物中液化分离出去。
⑸ 因为生成物的浓度增大,反应向正方向进行,该反应为放热反应,故恒容下的措施应为降低温度,故T2﹥T3 。
⑹容积加倍,体系压强减小,平衡向逆反应方向移动,作图要点:①容积加倍的瞬间,各组分浓度都变为原来的1/2;②A 、B的新平衡浓度比原来的1/2要大,而C的浓度比原浓度的1/2要小。
【答案】(1)1:3:2 (2)vⅠ(A) >vⅡ(A) >vⅢ(A)
(3) αⅢ(B) 0.19 (4)向右移动 将C从平衡混合物中液化分离出去(5)> 由于平衡正向移动,且反应放热,在恒容条件下只能降低温度,故T2> T3
(6)第Ⅳ阶段体系中各物质的浓度随时间变化的趋势如下图所示:
29.请回答下列实验室中制取气体的有关问题。
⑴ 下图是用KMnO4与浓盐酸反应制取适量氯气的简易装置。
装置B、C、D的作用分别是:
B ;
C ;
D 。
⑵ 在实验室欲制取适量的NO气体。
①下图中最适宜完成该实验的简易装置是 (填序号);
② 根据所选的装置完成下表(不需要的可以不填):
应加入的物质
所起的作用
A
B
C
D
③简单描述应观察到的现象 。
【解析】⑴ 气体制备一般包括四部分:发生装置、除杂净化装置、收集装置、尾气处理装置。由于题中提到该装置是制取适量氯气的简易装置,所以B的作用是除去Cl2中混有的杂质气体HCl;C的作用是用排液法收集氯气;D的作用是吸收多余的氯气。
⑵ ① 由于NO易与空气中的氧气反应,但难溶于水,故应用排水法收集,则最适宜完成该实验的简易装置是Ⅰ。
② 制取NO用铜和稀硝酸,用排水法收集NO,最后为防止污染环境,用NaOH溶液吸收。
③ 现象包括看到的、听到的、闻到的、触摸到的。A处试管内有气泡产生,铜片减少,溶液变蓝,试管上部有红棕色的气体生成,一段时间后B中液体排出后可以收集到无色气体。
【答案】(1)除去Cl2中混有的杂质气体HCl 用排液法收集氯气 吸收多余的氯气
(2) ① I
②
应加入的物质
所起的作用
A
铜和稀硝酸
反应物
B
水
防止NO被氧化
C
NaOH溶液
防止产生的NO氧化污染环境
D
③ A处试管内有气泡产生,铜片减少,溶液变蓝,试管上部有红棕色的气体生成,一段时间后B中液体排出后可以收集到无色气体。
30.金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
请回答下列问题:
⑴ 环戊二烯分子中最多有 个原子共面;
⑵ 金刚烷的分子式为 ,其分子中的CH2基团有 个;
⑶下面是以环戊烷为原料制备环戊二烯的合成路线:其中,反应①的产物名称是 ,反应②的反应试剂和反应条件是 ,反应③的反应类型是 ;
⑷ 已知烯烃能发生如下的反应:
请写出下列反应产物的结构简式:
⑸ A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经酸性高锰酸钾溶液氧化得羧基],写出A所有可能的结构简式(不考虑立体异构):
。
【解析】⑴ 依据乙烯分子6原子共平面的特点,环戊二烯分子中最多有9个原子共面。
⑵ 依据金刚烷的结构,其分子式为C10H16,其分子中的CH2基团6个。
⑶ 反应①的产物名称是1—氯环戊烷;反应②发生消去反应,其反应试剂为NaOH的醇溶液,反应条件是加热。
⑷ 由题目信息可知,双键碳上连有H原子的,经过反应后双键断裂可以生成醛基,则其反应产物的结构简式为。
⑸ 二聚环戊二烯的分子式为C10H12,其不饱和度为5,又A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸,则A的分子必有苯环(4个不饱和度),另外还要有一个碳碳双键,则A所有可能的结构简式为:
【答案】(1)9(2)C10 H16 6(3)1—氯环戊烷 NaOH的醇溶液,加热 消去反应
(4)
(5)