- 104.00 KB
- 2021-05-14 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
配位键高考题汇编
1.(92全国)气态氯化铝(Al2Cl6)是具有配位键的化合物,分子中原子间成键的关系如下图所示.请将图中,你认为是配位键的斜线上加上箭头。
【答案】
(2013宁德市质量检查)①AlCl3在NaCl、KCl融熔盐中能形成Al2Cl7-,其结构如图所示。其中Al原子的杂化轨道类型为 ,配位键数目为 。
【答案】sp3 2
(2010福建卷)(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
[CrCln(H2O)6-n]x++xR-H→Rx[CrCln(H2O)6-n]+xH+
交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。
将含0.0015 mol [CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1 NaOH溶液25.00 ml,可知该配离子的化学式为 。
【答案】[CrCl(H2O)5]2+
【解析】(3)根据提供数据,该配离子通过离子交换树脂后生成的n(H+)=0.1200mol/L×0.025L=0.003mol,则1:x=0.0015:0.003,解得x=2。则该配离子的化学式为[CrCl(H2O)5]2+。
(2011江苏卷)(4)元素W(Cu)的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是 ,它可与浓盐酸发生非氧化还原反应,生成配合物HnWCl3,反应的化学方程式为 。
【答案】CuCl CuCl+2HCl=H2CuCl3 (或CuCl+2HCl=H2[CuCl3])
(2012海南卷)(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是 ,反应的化学方应程式为 。
【答案】H2O2为氧化剂,氨与Cu2+形成配离子,两者相互促进使反应进行。 Cu+H2O2+4NH3=[Cu(NH3)4]2++2OH-
(2012江苏卷)(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为 。
【答案】
(2012山东卷)(3)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=______。CO与N2结构相似,CO分子内σ建于π键个数之比为________。
【答案】4 1:2
(2013山东卷)(4)若BCl3与XYn 通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤对电子的原子是 。
【答案】X
(2013江苏)(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
【答案】16
(2013新课标卷Ⅱ)(4)A-、B+和C3+三种离子组成的化合物B3CA6(K3FeF6),其中化学键的类型有_____;该化合物中存在一个复杂离子,该离子的化学式为_______,配位体是____。(A为F,B为K,C为Fe)
【答案】离子键、配位键 [FeF6]3-;
(2014福建卷·31)(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1mo NH4BF4含有 mol配位键。
【答案】2
(2014四川卷8)(2)R2+的水合离子中,提供孤电子对的原子是 ② 。
(4)将R单质的粉末加入XH3的浓溶液中,通入Y2,充分反应后溶液呈深蓝色,该反应的离子方程式是 。(R为Cu、X为N,Y为O2)
【答案】(2)O(4)2Cu+8NH3·H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O
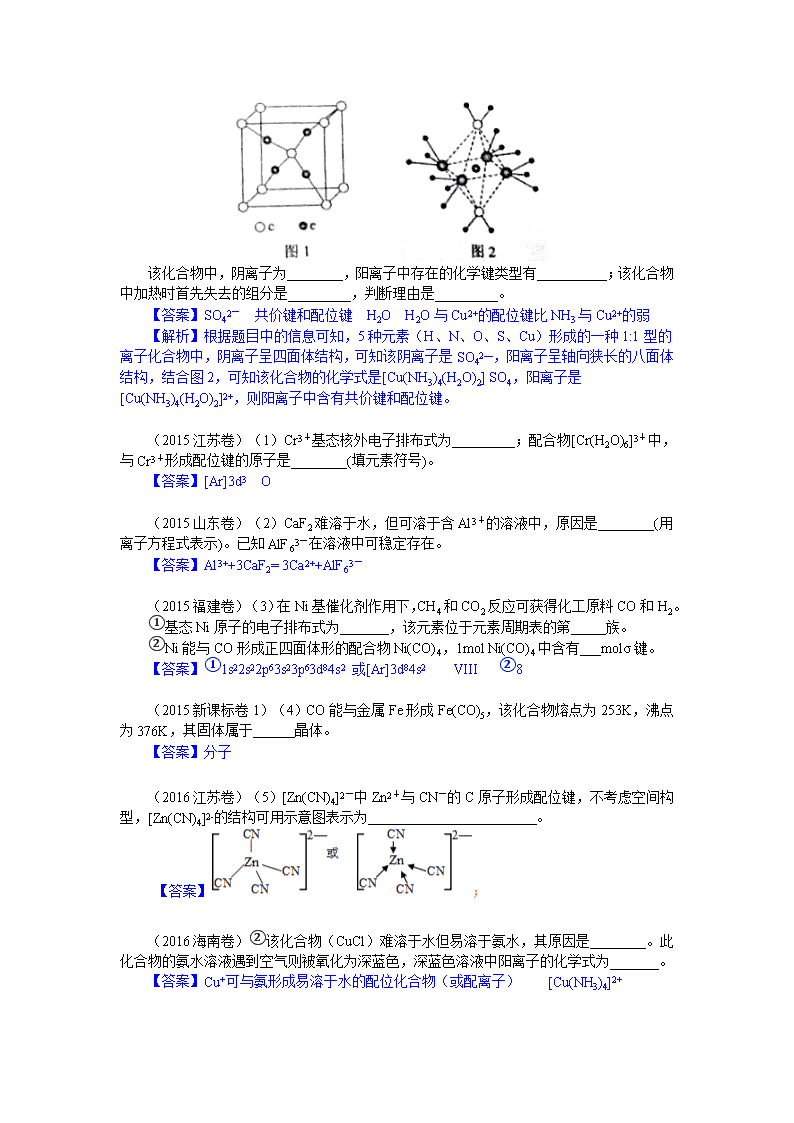
(2014·全国卷II,T37)(5)这5种元素(H、N、O、S、Cu)形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。
该化合物中,阴离子为________,阳离子中存在的化学键类型有__________;该化合物中加热时首先失去的组分是_________,判断理由是_________。
【答案】SO42- 共价键和配位键 H2O H2O与Cu2+的配位键比NH3与Cu2+的弱
【解析】根据题目中的信息可知,5种元素(H、N、O、S、Cu)形成的一种1:1型的离子化合物中,阴离子呈四面体结构,可知该阴离子是SO42—,阳离子呈轴向狭长的八面体结构,结合图2,可知该化合物的化学式是[Cu(NH3)4(H2O)2] SO4,阳离子是[Cu(NH3)4(H2O)2]2+,则阳离子中含有共价键和配位键。
(2015江苏卷)(1)Cr3+基态核外电子排布式为_________;配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是________(填元素符号)。
【答案】[Ar]3d3 O
(2015山东卷)(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是________(用离子方程式表示)。已知AlF63-在溶液中可稳定存在。
【答案】Al3++3CaF2= 3Ca2++AlF63-
(2015福建卷)(3)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni原子的电子排布式为_______,该元素位于元素周期表的第_____族。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有___molσ键。
【答案】①1s22s22p63s23p63d84s2 或[Ar]3d84s2 VIII ②8
(2015新课标卷1)(4)CO能与金属Fe形成Fe(CO)5,该化合物熔点为253K,沸点为376K,其固体属于 晶体。
【答案】分子
(2016江苏卷)(5)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为 。
【答案】;
(2016海南卷)②该化合物(CuCl)难溶于水但易溶于氨水,其原因是________。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______。
【答案】Cu+可与氨形成易溶于水的配位化合物(或配离子) [Cu(NH3)4]2+