- 3.64 MB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第
3
讲
氧化还原反应
1.本质和特征
考点一 氧化还原反应基本概念
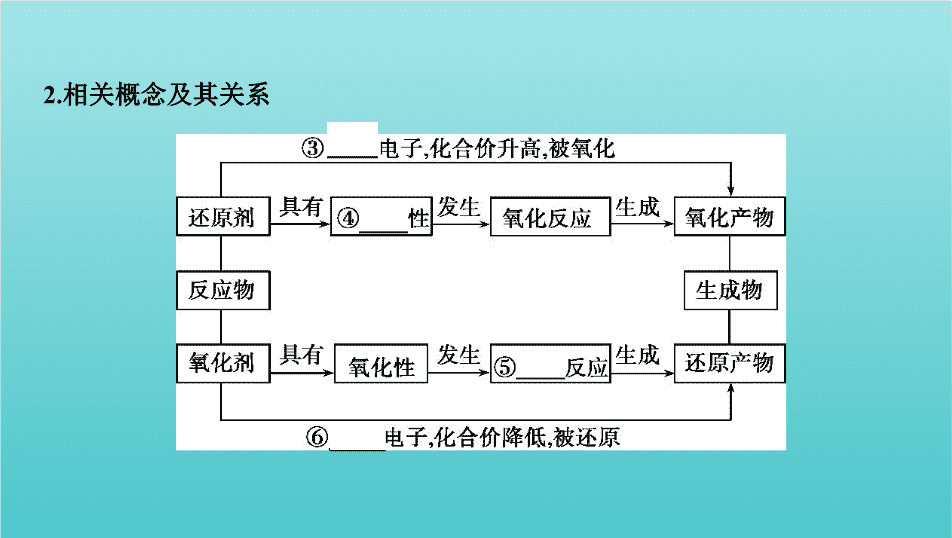
2.相关概念及其关系
[简记]“失升氧,得降还,若说剂,正相反”。
例如:反应MnO
2
+4HCl(浓)
MnCl
2
+Cl
2
↑+2H
2
O中氧化剂是⑦
MnO
2
,
还原剂是HCl,氧化产物是⑧
Cl
2
,生成1 mol Cl
2
时转移电子数目为
⑨
1.204
×
10
24
。
及时提醒
①有单质参与的化合反应、有单质生成的分解反应是氧化还原
反应。
②有单质参加或生成的化学反应,不一定是氧化还原反应,如3O
2
2O
3
。
③所有的置换反应都是氧化还原反应;所有的复分解反应都不是氧化还原
反应。
④元素由化合态变为游离态时,该元素不一定被还原。如:Cu
2+
→Cu时,铜元
素被还原,Cl
-
→Cl
2
时,氯元素被氧化。
3.氧化性和还原性
(1)氧化性是指物质
得电子
的性质(或能力);还原性是指物质
失电子
的性质(或能力)。
(2)元素价态与氧化性、还原性的关系
最高价态——只有
氧化性
,如Fe
3+
、H
2
SO
4
、KMnO
4
等;最低价态——
只有
还原性
,如金属单质、Cl
-
、S
2-
等;中间价态——既有
氧化性
,
又有
还原性
,如Fe
2+
、S、Cl
2
等。
4.氧化还原反应中电子转移的表示方法
(1)双线桥法
如Cu与稀硝酸反应中电子转移的方向和数目:
及时提醒
a.箭头指向反应前、后有元素化合价变化的同种元素的原子,且
需注明“得(到)”或“失(去)”。
b.箭头的方向不代表电子转移的方向,仅表示电子转移前后的变化。
c.失去电子的总数等于得到电子的总数。
(2)单线桥法
请标出Cu与稀硝酸反应中电子转移的方向和数目:
及时提醒
a.箭头从失电子元素的原子指向得电子元素的原子。
b.不标“得到”或“失去”,只标明电子转移的总数。
c.线桥只出现在反应物中。
5.氧化剂和还原剂
(1)常见的氧化剂
包括某些活泼的非金属单质、含有高价态元素的化合物、某些氧化物和过
氧化物等。如:
及时提醒 ①O
2
、O
3
在水溶液中的还原产物,酸性条件下是H
2
O,中性、碱性
条件下是OH
-
;而当还原产物为固态时是O
2-
或
。
②浓硝酸的还原产物是NO
2
,稀HNO
3
的还原产物是NO。
(2)常见的还原剂
包括活泼的金属单质、某些活泼的非金属单质、元素处于低价态时的物质
(化合物、低价金属阳离子、非金属阴离子、氢化物等)。如:
(3)既可作氧化剂,又可作还原剂的物质或微粒
1.
易错易混辨析(正确的画“√”,错误的画“
✕
”)。
(1)元素由化合态变成游离态时,可能被氧化,也可能被还原
(
√
)
(2)金属单质只有还原性,非金属单质只有氧化性
(
✕
)
(3)氧化还原反应中的反应物不是氧化剂就是还原剂
(
✕
)
(4)氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原
(
✕
)
(5)在反应2CuFeS
2
+O
2
Cu
2
S+2FeS+SO
2
中,SO
2
既是氧化产物,又是还原产
物
(
√
)
(6)Al原子比Na原子最外层电子数多,故还原性:Al>Na
(
✕
)
(7)1 mol Cl
2
参加反应时一定得到2 mol电子
(
✕
)
2.
【深度思考】
下面是氧化还原反应与四种基本反应类型间的关系图示,请完成填空。
(1)一定属于氧化还原反应的是
反应。
(2)一定不属于氧化还原反应的是
反应。
(3)有单质参加的化合反应或有单质生成的分解反应
(填“一定”或
“不一定”)属于氧化还原反应。
答案
(1)置换 (2)复分解
(3)一定
1.
下列我国古代的技术应用中,不涉及氧化还原反应的是
(
A
)
题组一 氧化还原反应的概念及判断
答案
A A项,贝壳的主要成分是碳酸钙,煅烧时碳酸钙发生分解反应生成
氧化钙和二氧化碳,不是氧化还原反应。
2.
(2019河南洛阳一调)下列工业生产的过程中,未涉及氧化还原反应的是
(
D
)
A.粗铜精炼 B.海水提镁 C.工业制铝 D.海水制粗盐
答案
D 海水经风吹日晒,蒸发溶剂,浓缩、结晶得到粗盐,整个过程没有元
素化合价改变,不涉及氧化还原反应,选项D正确。
3.
在下列反应中,HCl作还原剂的是
,HCl作氧化剂的是
,
HCl为还原产物的是
。
①KOH+HCl
KCl+H
2
O
②2KMnO
4
+16HCl(浓)
2KCl+2MnCl
2
+5Cl
2
↑+8H
2
O
③Cl
2
+H
2
O
HCl+HClO
④2NaCl+H
2
SO
4
(浓)
Na
2
SO
4
+2HCl↑
⑤Fe+2HCl
FeCl
2
+H
2
↑
答案
② ⑤ ③
题后悟道
(1)同一种物质在反应中是作氧化剂还是作还原剂,取决于另一种反应物的性
质。如H
2
O
2
与氧化性强的KMnO
4
反应时作还原剂;与还原性较强的FeCl
2
、Na
2
SO
3
反应时作氧化剂。
(2)同一种氧化剂(或还原剂)所对应的还原产物(或氧化产物)不是一成不变的,而是决定于还原剂(或氧化剂)的性质、反应条件、反应物的浓度、反应介质的酸碱性等多种因素。如KMnO
4
在酸性溶液中的还原产物一般是Mn
2+
;在中性或碱性溶液中的还原产物一般是锰的较高价态的化合物,如MnO
2
、K
2
MnO
4
等。HNO
3
、H
2
SO
4
的还原产物不仅与它们的浓度有关,还与还原剂的还
原性强弱有关。
题组二 电子转移的表示方法
4.
判断下列反应中电子转移方向、数目表示的正误。
(1)
(
✕
)
(2)
(
✕
)
(3)
(
✕
)
(4)
(
√
)
(5)
(
√
)
(6)
(
✕
)
题后悟道
正确表示电子转移的关键——正确标出元素化合价
基本方法是先标出熟悉元素的化合价,再根据化合物中各元素正、负化合价
的代数和为零的原则求解其他元素的化合价。常见元素的化合价可以借助
化合价口诀来记忆:一价氢、氯、钾、钠、银;二价氧、钙、钡、镁、锌;三
铝、四硅、五价磷;二三铁、二四碳、二三四五氮常见;二四六硫锰齐(七)全;
铜汞二价最常见;单质零价永不变;金属无负价。
一些特殊物质中元素的化合价:
5.
根据下列反应,可以判断有关物质的氧化性由强到弱的顺序正确的是(
B
)
①Cl
2
+2KI
2KCl+I
2
②2FeCl
2
+Cl
2
2FeCl
3
③2FeCl
3
+2HI
2FeCl
2
+2HCl+I
2
④H
2
S+I
2
S↓+2HI
A.H
2
S>I
2
>Fe
3+
>Cl
2
B.Cl
2
>Fe
3+
>I
2
>S
C.Fe
3+
>Cl
2
>H
2
S>I
2
D.Cl
2
>I
2
>Fe
3+
>H
2
题组三 氧化性、还原性强弱判断及应用
答案
B 由反应①可知氧化性:Cl
2
>I
2
,由反应②可知氧化性:Cl
2
>Fe
3+
,由反应
③可知氧化性:Fe
3+
>I
2
,由反应④可知氧化性:I
2
>S,则氧化性:Cl
2
>Fe
3+
>I
2
>S。
6.
(2019河南安阳月考)已知常温下在溶液中可发生如下两个离子反应:Ce
4+
+
Fe
2+
Fe
3+
+Ce
3+
、Sn
2+
+2Fe
3+
2Fe
2+
+Sn
4+
,由此可以确定Fe
2+
、Ce
3+
、Sn
2+
三种离子的还原性由强到弱的顺序是
(
A
)
A.Sn
2+
、Fe
2+
、Ce
3+
B.Sn
2+
、Ce
3+
、Fe
2+
C.Ce
3+
、Fe
2+
、Sn
2+
D.Fe
2+
、Sn
2+
、Ce
3+
答案
A 根据反应Ce
4+
+Fe
2+
Fe
3+
+Ce
3+
,可以判断出还原性:Fe
2+
>Ce
3+
;根
据反应Sn
2+
+2Fe
3+
2Fe
2+
+Sn
4+
,可以判断出还原性:Sn
2+
>Fe
2+
,所以还原性由
强到弱的顺序是Sn
2+
>Fe
2+
>Ce
3+
。故本题选A。
7.
已知I
-
、Fe
2+
、SO
2
、Cl
-
、H
2
O
2
均有还原性,它们在酸性溶液中还原性的强
弱顺序为SO
2
>I
-
>H
2
O
2
>Fe
2+
>Cl
-
,则下列反应不能发生的是
(
C
)
A.2Fe
3+
+SO
2
+2H
2
O
2Fe
2+
+S
+4H
+
B.I
2
+SO
2
+2H
2
O
H
2
SO
4
+2HI
C.H
2
O
2
+H
2
SO
4
SO
2
↑+O
2
↑+2H
2
O
D.2Fe
3+
+2I
-
2Fe
2+
+I
2
答案
C 根据氧化还原反应的规律可知,氧化性:氧化剂>氧化产物;还原性:
还原剂>还原产物。强氧化剂与强还原剂发生反应产生具有弱氧化性和弱还
原性的物质。若A反应可以发生,则还原性:SO
2
>Fe
2+
,正确;若B反应可以发生,
则还原性:SO
2
>I
-
,正确;若C反应可以发生,则还原性:H
2
O
2
>SO
2
,错误;若D反应
可以发生,则还原性:I
-
>Fe
2+
,正确。
题后悟道
(1)氧化性、还原性强弱比较的方法
氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
(2)利用元素周期律、金属活动性顺序、电化学原理均可判断氧化性、还原
性强弱。
(3)物质的氧化性、还原性受温度、浓度、酸碱性等因素影响
。
考点二 氧化还原反应的规律及应用
一、守恒规律
(1)氧化还原反应中,氧化剂和还原剂得失电子守恒。
(2)应用
①直接计算反应物与产物或与转移电子的数量关系。如用铜电极电解Na
2
SO
4
溶液,其阳、阴极产物及转移电子关系式为Cu
2+
~2e
-
~H
2
~2OH
-
。
②配平氧化还原反应方程式。
(3)解题流程:
1.
在酸性条件下,可发生如下反应:Cl
+2M
3+
+4H
2
O
M
2
+Cl
-
+8H
+
,M
2
中M的化合价是
(
C
)
A.+4 B.+5 C.+6 D.+7
答案
C 根据离子方程式中,反应前后电荷守恒,可得6-1=8-
n
-1,解得
n
=2,
M
2
中M的化合价为+6价,故C正确。
2.
Na
2
S
x
在碱性溶液中可被NaClO氧化为Na
2
SO
4
,而NaClO被还原为NaCl,若反
应中Na
2
S
x
与NaClO的物质的量之比为1∶16,则
x
的值为
(
D
)
A.2 B.3 C.4 D.5
答案
D Na
2
x
Na
2
O
4
,Na
O
Na
根据得失电子守恒可得:[6-(-
)]
×
x
=16
×
2,解得
x
=5。
二、转化规律
(1)价态归中规律
①含义:含不同价态的同种元素的物质间发生氧化还原反应时,该元素价态的
变化遵循“高价+低价
中间价”,而不会出现交叉现象。
例如,H
2
S与浓硫酸的反应:
( √ )
(
✕
)
②应用:根据化合价判断氧化还原反应体系中的氧化剂、还原剂和氧化产
物、还原产物及电子转移的数目,判断同种元素不同价态的物质之间反应的
可能性。
(2)歧化规律
同一元素发生氧化还原反应生成不同价态的物质时,该元素的价态变化一定
遵循“中间价态
高价态+低价态”,不会出现“一边倒”的现象,即生成
物中该元素的价态不能都比中间价态高或都比中间价态低。
如:
3.
(2019山东临沂三调)已知Cu
+
在酸性条件下能发生下列反应:Cu
+
Cu+
Cu
2+
(未配平),NH
4
CuSO
3
与足量的10 mol·L
-1
H
2
SO
4
溶液混合微热,产生下列现
象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断
下列说法一定合理的是
(
B
)
A.反应中硫酸作氧化剂
B.该反应显示硫酸具有酸性
C.刺激性气味的气体是氨气
D.NH
4
CuSO
3
中铜元素全部被氧化
答案
B 根据题意可知,分别发生反应:2Cu
+
Cu+Cu
2+
,S
+2H
+
H
2
O+SO
2
↑。反应中硫酸只显示酸性,A错误;NH
4
CuSO
3
中S元素化合价没有发
生变化,生成SO
2
,显示硫酸的酸性,B正确;根据反应S
+2H
+
H
2
O+SO
2
↑,
刺激性气味的气体是SO
2
,C错误;根据2Cu
+
Cu+Cu
2+
,可知Cu元素既被氧
化又被还原,D错误。
4.
已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关
系(未配平):
①G
Q+NaCl
②Q+H
2
O
X+H
2
③Y+NaOH
G+Q+H
2
O
④Z+NaOH
Q+X+H
2
O
这五种化合物中Cl元素化合价由高到低的顺序是
(
C
)
A.G、Y、Q、Z、X B.X、Z、Q、G、Y
C.X、Z、Q、Y、G D.G、Q、Y、Z、X
答案
C 由①得出Q中Cl元素化合价高于G;由②得出X中Cl元素化合价高
于Q;由③得出Y中Cl元素化合价介于G、Q之间;由④得出Z中Cl元素化合价
介于Q、X之间,故选C。
三、强者优先规律
在浓度相差不大的溶液中:
(1)同时含有几种还原剂时
将按照还原性由强到弱的顺序依次反
应。如在FeBr
2
溶液中通入少量Cl
2
时,因为还原性:Fe
2+
>Br
-
,所以Fe
2+
先与Cl
2
反
应。
(2)同时含有几种氧化剂时
将按照氧化性由强到弱的顺序依次反
应。如在含有Fe
3+
、Cu
2+
的溶液中加入Fe粉,因为氧化性:Fe
3+
>Cu
2+
,所以Fe粉
先与Fe
3+
反应,然后与Cu
2+
反应。
5.
已知酸性K
2
Cr
2
O
7
溶液可与FeSO
4
溶液反应生成Fe
3+
和Cr
3+
。现将硫酸酸化的
K
2
Cr
2
O
7
溶液与FeSO
4
溶液混合,充分反应后再向所得溶液中加入KI溶液,混合
溶液中Fe
3+
的物质的量随加入的KI的物质的量的变化关系如图所示,下列说
法中不正确的是
( )
A.图中AB段的氧化剂为K
2
Cr
2
O
7
B.图中BC段发生的反应为2Fe
3+
+2I
-
2Fe
2+
+I
2
C.开始加入的K
2
Cr
2
O
7
的物质的量为0.25 mol
D.K
2
Cr
2
O
7
与FeSO
4
反应的物质的量之比为1∶3
答案
D A项,开始时
n
(Fe
3+
)不变,说明Fe
3+
没有参加反应,则AB段应为K
2
Cr
2
O
7
和KI的反应,正确;B项,BC段
n
(Fe
3+
)逐渐减小,说明Fe
3+
和KI发生氧化还原反
应:2Fe
3+
+2I
-
2Fe
2+
+I
2
,正确;C项,由图像可知,在酸性条件下,整个反应过程
中,K
2
Cr
2
O
7
将Fe
2+
氧化为Fe
3+
,Fe
3+
又被I
-
还原为Fe
2+
,相当于K
2
Cr
2
O
7
只与I
-
发生氧
化还原反应:Cr
2
+6I
-
+14H
+
2Cr
3+
+3I
2
+7H
2
O,则
n
(Cr
2
)=
n
(I
-
)=
×
1.5
mol=0.25 mol,正确;D项,6Fe
2+
+Cr
2
+14H
+
6Fe
3+
+2Cr
3+
+7H
2
O,K
2
Cr
2
O
7
与
FeSO
4
反应的物质的量之比为1∶6,错误。
6.
已知:2Fe
2+
+Br
2
2Fe
3+
+2Br
-
,2Fe
3+
+2I
-
2Fe
2+
+I
2
。向FeI
2
、FeBr
2
的混合
溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。下列有关
说法中,不正确的是
(
)
A.还原性:I
-
>Fe
2+
>Br
-
B.原混合溶液中FeBr
2
的物质的量为3 mol
C.当通入1 mol Cl
2
时,溶液中发生的反应为2Fe
2+
+Cl
2
2Fe
3+
+2Cl
-
D.原溶液中
n
(Fe
2+
)∶
n
(I
-
)∶
n
(Br
-
)=2∶1∶3
答案
C 由已知反应可知还原性:I
-
>Fe
2+
>Br
-
,则通入氯气后,I
-
最先反应,Br
-
最后反应。分析图像可知,原溶液中I
-
、Br
-
、Fe
2+
的物质的量分别为2 mol、6
mol、4 mol,所以原溶液中FeBr
2
的物质的量为3 mol;当通入1 mol Cl
2
时,发生
的反应为Cl
2
+2I
-
I
2
+2Cl
-
。
考点三 氧化还原反应方程式的配平与书写
分析近几年的高考化学试题发现,主观题中新情景下陌生氧化还原反应方程式的书写与配平是最常见的考查方式。除了已知反应物和生成物,利用氧化还原反应方程式的配平方法书写方程式外,有时还会出现缺项方程式的配平。该类氧化还原反应方程式一般结合实际情景或化工流程中物质的转化判定所缺物质,同时结合离子反应进行考查,题目综合性强,难度较大。备考过程中要结合实例,确定解题流程,分类突破。
类型一 直接型氧化还原反应方程式的配平
典例1
配平下列反应的化学方程式:
MnO(OH)
2
+I
-
+H
+
Mn
2+
+I
2
+H
2
O
[流程应用]
答案
MnO(OH)
2
+2I
-
+4H
+
Mn
2+
+I
2
+3H
2
O
1.
(1)
HCl(浓)+
MnO
2
Cl
2
↑+
MnCl
2
+
H
2
O
(2)
FeS
2
+
O
2
Fe
2
O
3
+
SO
2
(3)
KI+
KIO
3
+
H
2
SO
4
I
2
+
K
2
SO
4
+
H
2
O
(4)
Mn
+
H
+
+
Cl
-
Mn
2+
+
Cl
2
↑+
H
2
O
(5)
Mn
+
Fe
2+
+
H
+
Mn
2+
+
Fe
3+
+
H
2
O
(6)
P+
CuSO
4
+
H
2
O
Cu+
H
3
PO
4
+
H
2
SO
4
(7)
I
2
+
NaOH
NaI+
NaIO
3
+
H
2
O
(8)
S+
KOH
K
2
S+
K
2
SO
3
+
H
2
O
(9)
P
4
+
KOH+
H
2
O
KH
2
PO
2
+
PH
3
(10)
(NH
4
)
2
Cr
2
O
7
N
2
↑+
Cr
2
O
3
+
H
2
O
答案
(1)4 1 1 1 2
(2)4 11 2 8
(3)5 1 3 3 3 3
(4)2 16 10 2 5 8
(5)1 5 8 1 5 4
(6)2 5 8 5 2 5
(7)3 6 5 1 3
(8)3 6 2 1 3
(9)1 3 3 3 1
(10)1 1 1 4
类型二 缺项型氧化还原反应方程式的配平
缺项方程式是指某些反应物或生成物的化学式没有写出来,一般为水、
酸(H
+
)或碱(OH
-
),其配平流程为:
典例2
完成以下氧化还原反应的离子方程式:
( )Mn
+( )C
2
+
( )Mn
2+
+( )CO
2
↑+
。
[流程应用]
答案
2Mn
+5C
2
+16H
+
2Mn
2+
+10CO
2
↑+8H
2
O
及时提醒
补项原则
条件
补项原则
酸性条件下
缺H或多O补H
+
,少O补H
2
O
碱性条件下
缺H或多O补H
2
O,少O补OH
-
2.
(1)
ClO
-
+
Fe(OH)
3
+
Cl
-
+
Fe
+
H
2
O
(2)
Mn
+
H
2
O
2
+
Mn
2+
+
O
2
↑+
H
2
O
(3)
Mn
+
N
+
Mn
2+
+
N
+
H
2
O
(4)
S
2-
+
S
+
S↓+
H
2
O
(5)某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有Al
2
O
3
、
C、N
2
、AlN、CO。请将AlN之外的反应物与生成物分别填入以下空格内,
并配平。
答案
(1)3 2 4OH
-
3 2 5
(2)2 5 6H
+
2 5 8
(3)2 5 6H
+
2 5 3
(4)2 1 6H
+
3 3
(5)Al
2
O
3
+3C+N
2
2AlN+3CO
类型三 信息型氧化还原反应方程式的书写
信息型氧化还原反应方程式是指用文字描述的方式,叙述一个化学反应的过程,需要从文字信息中找出反应物、生成物,进而分析反应中电子得失情况,其流程为:
典例3
+6价Cr的化合物毒性较大,常用NaHSO
3
将废液中的Cr
2
还原成Cr
3+
,
该反应的离子方程式为
。
[流程应用]
答案
Cr
2
+3HS
+5H
+
2Cr
3+
+3S
+4H
2
O
3.
(1)向盛有H
2
O
2
溶液的试管中加入几滴酸化的FeCl
2
溶液,溶液变成棕黄色,发
生反应的离子方程式为
。
(2)已知Fe
3
S
4
能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况
下的密度为1.518 g·L
-1
),写出该反应的离子方程式:
。
(3)一定条件下,向FeSO
4
溶液中滴加碱性NaBH
4
溶液,溶液中B
(B元素的化
合价为+3价)与Fe
2+
反应生成纳米铁粉、H
2
和B(OH
,其离子方程式为
。
答案
(1)2Fe
2+
+H
2
O
2
+2H
+
2Fe
3+
+2H
2
O
(2)Fe
3
S
4
+6H
+
3H
2
S↑+3Fe
2+
+S
(3)2Fe
2+
+B
+4OH
-
2Fe+2H
2
↑+B(OH
4.
(1)ClO
2
与碘化钾在稀硫酸中反应的离子方程式为
。
(2)NaBH
4
与H
2
O反应生成NaBO
2
和H
2
。该反应的化学方程式是
。
(3)MnO
2
可与KOH和KClO
3
在高温下反应,生成K
2
MnO
4
,反应的化学方程式为
。
答案
(1)2ClO
2
+10I
-
+8H
+
5I
2
+4H
2
O+2Cl
-
(2)NaBH
4
+2H
2
O
NaBO
2
+4H
2
↑
(3)3MnO
2
+KClO
3
+6KOH
3K
2
MnO
4
+KCl+3H
2
O↑
方法技巧
氧化还原反应方程式的配平技巧
1.全变从左边配:氧化剂、还原剂中某元素化合价全变的,一般从左边反应物
着手配平。
2.自变从右边配:自身氧化还原反应(包括分解反应、歧化反应)一般从右边
着手配平。
3.缺项配平法:先将得、失电子数配平,再观察两边电荷。若反应物一侧缺正
电荷,一般加H+,生成物一边加水;若反应物一侧缺负电荷,一般加OH-,生成物
一边加水,然后将两边电荷数配平。
4.当化学方程式中有多个缺项时,应根据化合价的变化找准氧化剂、还原
剂、氧化产物、还原产物。
考点四 竞争型离子反应和氧化还原反应
如果溶液中存在多种离子,则相互之间发生的反应可能有多种,此时溶液中可
能发生“平行反应”,也可能发生“竞争反应”。“平行反应”是指离子之
间同时反应互不影响,而“竞争反应”是指各个反应要按照一定的顺序完
成。常见类型:
(1)一种氧化剂(还原剂)与多种还原剂(氧化剂)反应,如把Cl
2
通入含有I
-
、Br
-
、
Fe
2+
的溶液中,按照还原能力由强到弱的顺序,I
-
优先反应,其次是Fe
2+
,最后是Br
-
。
(2)一种酸(碱)与多种碱性(酸性)物质反应,如把盐酸逐滴加入含有NaOH、
Na
2
CO
3
、NaHCO
3
的混合溶液中,按照碱性由强到弱的顺序NaOH优先反应,
其次是Na
2
CO
3
,最后是NaHCO
3
。
(3)若某一溶液中同时存在几种能与所加试剂形成类型相似的沉淀的离子,则
溶解度(严格地说应为溶度积)小的物质先沉淀。如向AlCl
3
、FeCl
3
的混合溶
液中逐滴加入氢氧化钠溶液,应优先生成Fe(OH)
3
沉淀,而不是Al(OH)
3
沉淀。
(4)互相促进水解的反应与复分解反应
如果既符合发生互相促进水解反应的条件,又符合直接发生复分解反应的条
件,究竟发生哪个反应,要具体情况具体分析。
典例1
在复杂的体系中,确定化学反应发生的先后顺序有利于解决问题,下
列物质参与反应的先后顺序正确的是
(
C
)
A.含等物质的量的FeBr
2
、FeI
2
的溶液中,缓慢通入氯气:I
-
、Br
-
、Fe
2+
B.含等物质的量的Fe
3+
、Cu
2+
、H
+
的溶液中加入锌粉:Cu
2+
、Fe
3+
、H
+
C.含等物质的量的Al
、OH
-
、C
的溶液中,逐滴加入盐酸:OH
-
、Al
、
C
D.含等物质的量的Ba(OH)
2
、KOH的溶液中,缓慢通入CO
2
:KOH、Ba(OH)
2
题后悟道
(1)常用离子还原性:S
2-
>S
>I
-
>Fe
2+
>Br
-
>Cl
-
;
(2)常见离子的氧化性:Fe
3+
>Cu
2+
>H
+
>Fe
2+
>Zn
2+
;
(3)常见酸根离子结合H
+
能力:OH
-
>Al
>C
>HC
>CH
3
COO
-
[酸根离子对
应酸的酸性越弱,则酸根离子结合质子(H
+
)的能力越强]。
典例2
向NH
4
Cl、AlCl
3
、MgCl
2
的混合溶液中逐滴加入NaOH溶液至过量,
按反应的先后顺序,写出有关反应的离子方程式:{已知25 ℃时,
K
sp
[Mg(OH)
2
]
=5.61
×
10
-12
,
K
sp
[Al(OH)
3
]=1.3
×
10
-33
}
(1)
,
(2)
,
(3)
,
(4)
。
答案
(1)Al
3+
+3OH
-
Al(OH)
3
↓
(2)Mg
2+
+2OH
-
Mg(OH)
2
↓
(3)N
+OH
-
NH
3
·H
2
O
(4)Al(OH)
3
+OH
-
Al
+2H
2
O
题后悟道
弱碱阳离子对应碱的碱性越弱,该阳离子结合OH
-
的能力越强,如结合OH
-
能
力:Fe
3+
>Al
3+
>Mg
2+
>N
。
1.
往含Fe
3+
、H
+
、N
的混合液中加入少量S
,充分反应后,下列表示该反应
的离子方程式正确的是
(
C
)
A.2Fe
3+
+S
+H
2
O
2Fe
2+
+S
+2H
+
B.2H
+
+S
H
2
O+SO
2
↑
C.2H
+
+2N
+3S
3S
+2NO↑+H
2
O
D.2Fe
3+
+3S
+3H
2
O
2Fe(OH)
3
↓+3SO
2
↑
答案
C 氧化还原反应优先于非氧化还原反应,因此B、D不正确。如果
S
先与Fe
3+
反应,则生成的Fe
2+
又会与H
+
、N
反应,所以S
应先与H
+
、
N
反应,故选C。
2.
将足量Cl
2
缓缓通入含0.02 mol H
2
SO
3
和0.02 mol HBr的混合溶液中。在此
过程中溶液的pH与Cl
2
通入量的关系示意图是(溶液体积变化忽略不计,且不
考虑Cl
2
与水反应)
(
A
)
答案
A 因H
2
SO
3
的还原性强于HBr的还原性,故Cl
2
先氧化H
2
SO
3
:H
2
SO
3
+Cl
2
+H
2
O
H
2
SO
4
+2HCl,生成的H
2
SO
4
和HCl是强酸,故溶液的pH减小;当H
2
SO
3
完全反应后,发生反应Cl
2
+2HBr
Br
2
+2HCl,溶液的pH不再改变。
3.
已知室温下,Al(OH)
3
的
K
sp
或溶解度远大于Fe(OH)
3
。向浓度均为0.1 mol·L
-1
的Fe(NO
3
)
3
和Al(NO
3
)
3
的混合溶液中,逐滴加入NaOH溶液。下列示意图表示
生成Al(OH)
3
的物质的量与加入NaOH溶液的体积的关系,合理的是
(
C
)
答案
C 因为
K
sp
[Al(OH)
3
]
≫
K
sp
[Fe(OH)
3
],当向浓度均为0.1 mol·L
-1
的含Fe
3+
、
Al
3+
的混合溶液中逐滴加入NaOH溶液时,开始阶段只有Fe(OH)
3
沉淀产生,Fe
3+
沉淀完全后生成Al(OH)
3
沉淀,随着NaOH溶液的加入,最终生成的Al(OH)
3
沉淀
又全部溶解,故C正确。
1.
(2019课标Ⅰ,27节选)硫酸铁铵[NH
4
Fe(SO
4
)
2
·
x
H
2
O]是一种重要铁盐。为充
分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流
程如下:
真题演练
·
模拟预测
回答下列问题:
(3)步骤③中选用足量的H
2
O
2
,理由是
。分
批加入H
2
O
2
,同时为了
,溶液要保持pH小于0.5。
答案
(3)将Fe
2+
全部氧化为Fe
3+
;不引入杂质 防止Fe
3+
水解
解析
(3)步骤③利用H
2
O
2
的强氧化性将Fe
2+
全部氧化为Fe
3+
。为防止Fe
3+
水
解,需控制溶液的pH小于0.5。
2.
(2018课标Ⅰ,27改编)焦亚硫酸钠(Na
2
S
2
O
5
)可用作食品的抗氧化剂。在测定
某葡萄酒中Na
2
S
2
O
5
残留量时,用碘标准溶液进行滴定,该反应的离子方程式
为
。
答案
S
2
+2I
2
+3H
2
O
2S
+4I
-
+6H
+
3.
(不定项)(2020山东高考模拟)已知Pb
3
O
4
与HNO
3
溶液发生反应Ⅰ:Pb
3
O
4
+4H
+
PbO
2
+2Pb
2+
+2H
2
O;PbO
2
与酸化的MnSO
4
溶液发生反应Ⅱ:5PbO
2
+2Mn
2+
+
4H
+
+5S
2Mn
+5PbSO
4
+2H
2
O。下列推断正确的是
(
AD
)
A.由反应Ⅰ可知,Pb
3
O
4
中Pb(Ⅱ)和Pb(Ⅳ)含量之比为2∶1
B.由反应Ⅰ、Ⅱ可知,氧化性:HNO
3
>PbO
2
>Mn
C.Pb可与稀硝酸发生反应:3Pb+16HNO
3
3Pb(NO
3
)
4
+4NO↑+8H
2
O
D.Pb
3
O
4
可与盐酸发生反应:Pb
3
O
4
+8HCl
3PbCl
2
+4H
2
O+Cl
2
↑
答案
AD 反应Ⅰ中HNO
3
未将Pb
2+
氧化,可证明氧化性:HNO
3
Mn
,又因氧化性:Mn
>Cl
2
,故Pb
3
O
4
可
与盐酸发生氧化还原反应,故D正确。
相关文档
- 2019-2020学年湖北省荆州中学高一12021-07-027页
- 化学卷·2018届山东省济南一中高二2021-07-0235页
- 2019届一轮复习人教版第六章第22讲2021-07-0219页
- 云南省丘北二中2018-2019学年高二92021-07-0217页
- 安徽省阜阳市大田中学2018-2019学2021-07-025页
- 2020高考化学高频热点1化学与传统2021-07-026页
- 高一化学同步测试(A)第一节 无机非金2021-07-025页
- 2021高考化学一轮复习课练4离子反2021-07-0217页
- 云南省保山市龙陵县一中2019-20202021-07-0213页
- 2021届新高考选考化学一轮复习人教2021-07-0210页