- 255.50 KB
- 2021-07-03 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
卤素的性质及X-的检验
练习时间:40分钟,总分100分
一、 选择题:
1.溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单质反应生成相应的卤化物,跟水反应的方程式为IBr+H2O===HBr+HIO。下列有关IBr的叙述中,不正确的是( )
A.IBr是双原子分子 B.在很多反应中,IBr是强氧化剂
C.和NaOH溶液反应生成NaBr和NaIO D.和水反应时,既是氧化剂又是还原剂
2.下列关于卤素的叙述正确的是( )
①卤素的钾盐中,最易被氧化的是氟化钾
②溴中溶有少量氯气,可以用加入溴化钠再用汽油萃取的方法提纯
③溴化银具有感光性,碘化银不具有感光性
④氟气跟氯化钠水溶液反应,一定有氟化氢和氧气生成
⑤氯气跟水反应时,水既不是氧化剂也不是还原剂
A.①③④ B.②③⑤ C.②④⑤ D.①③
3.下列叙述中正确的是( )
A.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2
B.用硝酸酸化的硝酸银溶液能一次鉴别NaCl、NaBr、KI三种失去标签的溶液
C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-
D.某浅黄色的溴水,加入CCl4振荡静置后,上层显橙红色
4.鉴别NaCl、NaBr、NaI可以选用的试剂是( )
①碘水、淀粉溶液 ②氯水、CCl4 ③溴水、苯 ④稀硝酸、AgNO3溶液 ⑤氯水、苯 ⑥FeCl3溶液、CCl4
A.①②④ B.②③⑥ C.②④⑤ D.④⑤⑥
5.某学生做如下实验:第一步,在淀粉KI溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列对实验原理的解释和所得结论错误的是( )
A.第一步反应的离子方程式ClO-+2I-+2H+===I2+Cl-+H2O
B.淀粉KI溶液变蓝是因为I-被氧化为I2,I2使淀粉变蓝色
C.蓝色逐渐消失的原因是Na2SO3溶液具有漂白性
D.微粒的氧化性由强到弱的顺序是ClO->I2>SO
6.(2014·江苏,13)在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是( )
4
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-
C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
D.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
7.(2015·北京理综,11)某消毒液的主要成分为NaClO,还含有一定量的NaOH。下列用来解释事实的方程式中,不合理的是(已知:饱和NaClO溶液的pH约为11)( )
A.该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-===ClO-+Cl-+H2O
B.该消毒液的pH约为12:ClO-+H2OHClO+OH-
C.该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒Cl2:2H++Cl-+ClO-===Cl2↑+H2O
D.该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ClO-===HClO+CH3COO-
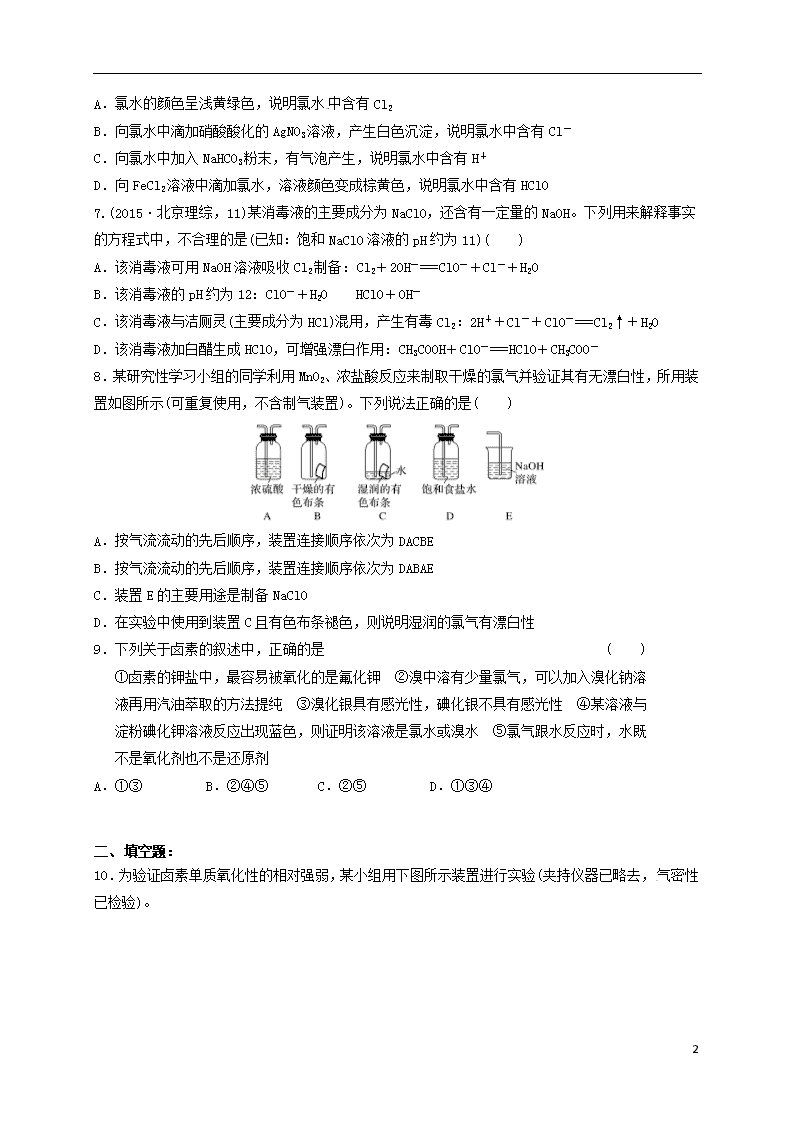
8.某研究性学习小组的同学利用MnO2、浓盐酸反应来制取干燥的氯气并验证其有无漂白性,所用装置如图所示(可重复使用,不含制气装置)。下列说法正确的是( )
A.按气流流动的先后顺序,装置连接顺序依次为DACBE
B.按气流流动的先后顺序,装置连接顺序依次为DABAE
C.装置E的主要用途是制备NaClO
D.在实验中使用到装置C且有色布条褪色,则说明湿润的氯气有漂白性
9.下列关于卤素的叙述中,正确的是 ( )
①卤素的钾盐中,最容易被氧化的是氟化钾 ②溴中溶有少量氯气,可以加入溴化钠溶
液再用汽油萃取的方法提纯 ③溴化银具有感光性,碘化银不具有感光性 ④某溶液与
淀粉碘化钾溶液反应出现蓝色,则证明该溶液是氯水或溴水 ⑤氯气跟水反应时,水既
不是氧化剂也不是还原剂
A.①③ B.②④⑤ C.②⑤ D.①③④
一、 填空题:
10.为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
4
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是____________________________________________。
(2)验证氯气的氧化性强于碘的实验现象是________________________________________
________________________________________________________________________。
(3)B中溶液发生反应的离子方程式是___________________________________________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是______________________________
________________________________________________________________________。
(5)过程Ⅲ实验的目的是_________________________________________________________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下____________________,得电子能力逐渐减弱。
11.实验探究是体验知识的产生或形成过程的基本途径。下面是某同学探究实验报告的一部分,请填空:
实验名称:氯、溴、碘的氧化性强弱比较
实验药品:NaCl溶液、KBr溶液、KI溶液、氯水、溴水、四氯化碳
实验步骤
实验结论
①NaCl溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色
氧化性从强到弱的顺序:氯、溴、碘
②KBr溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色
③KI溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色
(1)完成该实验需用到的仪器是________________________________________________;
(2)CCl4在实验中所起的作用是____________________________________________
________________________________________________________________________;
4
(3)在实验②中四氯化碳层颜色变化过程为_______________________________________
________________________________________________________________________;
(4)该同学的实验缺陷是____________________________________________________,
改进的办法是________________________________________________________________
________________________________________________________________________。
4