- 1021.00 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
高考总复习
第4讲 铜及其化合物 金属资源
[考纲要求]
1.掌握铜及其重要化合物的主要性质及其应用。2.了解常见金属活动顺序。3.了解合金的概念及其重要应用。
铜及其重要化合物
1.铜的性质
(1)物理性质:铜是________色金属,具有良好的________性、________性和延展性。
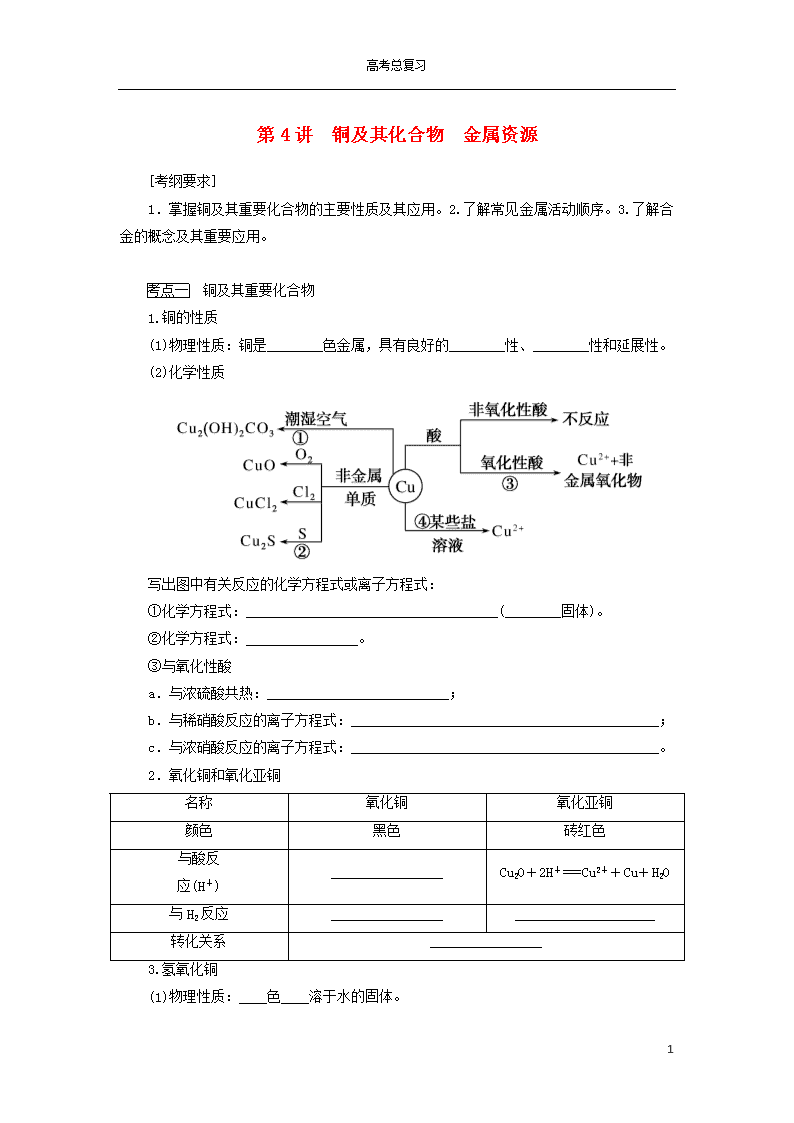
(2)化学性质
写出图中有关反应的化学方程式或离子方程式:
①化学方程式:____________________________________(________固体)。
②化学方程式:________________。
③与氧化性酸
a.与浓硫酸共热:__________________________;
b.与稀硝酸反应的离子方程式:____________________________________________;
c.与浓硝酸反应的离子方程式:____________________________________________。
2.氧化铜和氧化亚铜
名称
氧化铜
氧化亚铜
颜色
黑色
砖红色
与酸反
应(H+)
________________
Cu2O+2H+===Cu2++Cu+H2O
与H2反应
________________
____________________
转化关系
________________
3.氢氧化铜
(1)物理性质:____色____溶于水的固体。
21
高考总复习
(2)化学性质及应用
4.硫酸铜
CuSO4·5H2O为________晶体,俗称____________。无水CuSO4为________粉末,遇水变蓝色(生成CuSO4·5H2O),可作为水的检验依据。
[回扣判断](正确的打“√”,错误的打“×”)
(1)过量的铜与浓硝酸反应一定没有一氧化氮生成( )
(2)利用无水硫酸铜遇水变成蓝色这一性质,来检验水的存在( )
(3)将铁片置于CuSO4溶液中,铁片上有红色物质析出,说明铁比铜活泼( )
(4)铜在干燥的空气中性质稳定,但是在潮湿的环境中则易被锈蚀,生成铜绿( )
(5)铜与氯气、氧气、硫分别反应,得到的产物中铜的化合价均为+2价( )
(6)湿法炼铜和火法炼铜的反应中,铜元素都发生了还原反应( )
(7)CuO是黑色固体,与水反应可生成Cu(OH)2( )
(8)Cu2O遇硝酸会被氧化成Cu2+( )
(9)Cu2(OH)2CO3是铜锈的主要成分,在干燥的空气中不易生成( )
(10)无水硫酸铜生成CuSO4·5H2O属于物理变化( )
(11)铜绿在灼烧条件下会分解生成氢氧化铜和二氧化碳( )
[重点提醒]
1.铜及其化合物的颜色
物质
颜色
物质
颜色
Cu
紫红色
CuSO4
白色
CuO
黑色
CuSO4·5H2O
蓝色
Cu2O
砖红色
Cu2(OH)2CO3
绿色
Cu2S
黑色
Cu(OH)2
蓝色
2.无水CuSO4只能作为水的检验试剂,但不能作为水蒸气的吸收试剂而用于除杂。
对点速练
21
高考总复习
练点一 铜及其化合物的性质
1.某同学通过系列实验,探究Cu及其化合物的性质,下列操作正确且能达到目的的是( )
A.将铜粉和硫粉混合均匀加热以制取CuS
B.将Cu片放入过量浓硫酸中,一段时间后加水以观察CuSO4溶液的颜色
C.向CuSO4溶液中加入NaOH溶液,过滤洗涤并收集沉淀,加热以制取CuO
D.设计Cu—Al—浓硝酸原电池,以证明金属活动性:Cu
相关文档
- 人教版高中化学选修五 3_2醛(教案2)2021-07-085页
- 高中化学作业12酚含解析 人教版选2021-07-086页
- 【化学】湖北省鄂州市部分高中联考2021-07-0819页
- 2019-2020学年高中化学作业7化学键2021-07-085页
- 2019-2020学年高中化学课时作业182021-07-089页
- 2020版新教材高中化学第3章简单的2021-07-086页
- 2020高中化学第三章重要的有机化合2021-07-087页
- 高中化学解题方法大全2021-07-08130页
- 高中-化学:2离子反应及其发生的条件2021-07-0826页
- 2019-2020学年高中化学课时作业2有2021-07-089页