- 109.50 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
- 1 -
高一化学 1 月月考试题 09
时间:90 分钟;满分:100 分
可能用到的相对原子质量:H-1,O-16,Na-23,Ne-20,N-14,C-12,S-32,Cl-35.5
第Ⅰ卷(44 分)
一、单项选择题(本题共有 10 小题,每小题 2 分,共 20 分。每小题只有一个正确答案,请
将答案填入答题栏中。)
1、下列混合物可用溶解 过滤 蒸发操作分离的是
A、混有泥沙的食盐 B、混有水的酒精
C、白糖与食盐的混合物 D、铁粉和泥沙的混合物
2、想一想:Ba(OH)2(固体)、CuSO4(固体)、CH3COOH(液态)这些物质为什么归为一类,下
列哪些物质还可以和它们归为一类
A、75%的酒精溶液 B、硝酸钠 C、Fe(OH)3 胶体 D、豆浆
3、设 NA 表示阿伏加德罗常数的值,下列说法中正确的是
A、1 mol NH4
+ 所含质子数为 10NA B、10 克氖气所含原子数约为 NA
C、22.4 L SO2 所含的分子数为 NA
D、2.3 克金属钠变为钠离子时失去的电子数是 0.1NA
4、下列说法正确的是
A、在标准状况时,20mLNH3与60mLO2所含的分子个数之比为1:3
B、将 80gNaOH 溶于 1L 水中,所得溶液中 NaOH 的物质的量浓度为 2mol/L
C、18g 水在标准状况下的体积为 22.4L
D、相同质量的 CO 和 N2,其体积比为 1:1
5. 在盛放浓硫酸的试剂瓶的标签上应印有下列警示标记中的
6、下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是
A、浓硫酸质量变大 B、铝的表面生成致密的保护膜
C、澄清的石灰水变浑浊 D、氢氧化钠固体表面变潮
7、下列反应中,水作还原剂的是
A、CO2+H2O = H2CO3 B、Na2O + H2O = 2NaOH
C、2F2 + 2H2O = 4HF + O2 D、2Na + 2H2O = 2NaOH + H2↑
8、下列各组两种物质在溶液中反应,可用同一离子方程式表示的是
A、氢氧化铜和盐酸 氢氧化钡和盐酸 B、氯化钡和硫酸钾 氢氧化钡和硫酸
C、澄清石灰水和碳酸钠 氯化钙和碳酸钾 D、碳酸氢钠和硫酸 碳酸钠和盐酸
9、下列离子组能大量共存的是
A、K+ 、H+、SO4
2—、OH— B、Na+、Mg2+、OH—、NO3
—
C、Na+、H+、Cl—、CO3
2— D、Mg2+、Cu2+、Cl—、SO4
2—
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
- 2 -
10、等质量的①CH4、②H2、③HCl、④SO2,在标准状况下所占体积由大到小排列的顺序是
A、②>①>③>④ B、④>③>①>②
C、③>②>④>① D、①>④>②>③
二、不定项选择题(本题共有 6 小题,每小题 4 分,共 24 分。每小题有 1—2 个正确答案,
有 2 个答案的,全选且正确得 4 分,只选 1 个且正确得 2 分,多选、错选不得分。)
11、下列叙述正确的是
A、摩尔是国际上规定的七个基本物理量之一
B、一定温度、压强下,气体体积由其物质的量的多少决定
C、不同的气体,若体积不等,则它们所含的分子数一定不等
D、体积为22.4L的O2,其质量可能为32g
12、现仅有下列仪器:烧杯、铁架台(带铁圈)、三脚架、分液漏斗、石棉网、酒精灯、玻璃
棒、蒸发皿、温度计、牛角管和圆底烧瓶,从缺少仪器的角度分析,不能进行的实验项目有
A、过滤 B、蒸发 C、蒸馏 D、分液
13、下列离子方程式正确的有
A、硫酸镁溶液跟氢氧化钡溶液反应:SO4
2- + Ba2+ = BaSO4↓
B、稀硫酸滴在锌片上:Zn + 2H+ = Zn2+ + H2↑
C、NaHC03 溶液与稀 H2SO4 反应:CO3
2- + 2H+ = H2O + CO2↑
D、氢氧化铜与稀盐酸混合:OH- + H+ = H2O
14、氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶
瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
CNOAl 3232 COAlN 32
下列有关该反应的叙述正确的是
A、氮化铝中氮元素的化合价为-3
B、上述反应中每生成2molAlN,N2得到3mol电子
C、在氮化铝的合成反应中,N2是氧化剂,Al2O3是还原剂
D、该反应不属于四种基本反应类型中任一种
15、在 Na2SO4 和 Al2(SO4)3 的混合溶液中,测得 Al3+浓度为 0.1mol/L,SO4
2-浓度为 0.3mol/L,
则混合溶液中 Na+的浓度为
A、0.15mol/L B、0.45mol/L C、0.6mol/L D、0.3mol/L
16、将一定量的 MgCl2溶于 90g 水中,使每 10 个水分子中含有一个Cl-,则该MgCl2的物质的量是
A、0.05mol B、0.1mol C、0.25mol D、0.5mol
第Ⅱ卷(共 56 分)
三、填空题(方程式 3 分,其余每空 2 分,共 15 分。)
17、今有十种物质:①铝线 ②石墨 ③CO2 ④BaSO4 晶体 ⑤纯硫酸 ⑥金刚石
⑦石灰水 ⑧乙醇 ⑨熔化的 KNO3 ⑩液态 HCl(填序号)
其中,能导电的有 ,属于电解质的有 ,属于
非金属单质的有 。
18、在 3Cu+8HNO 3(稀)= 3Cu(NO3)2+4H2O+2NO↑中, 是还原剂,
是还原产物,若有 11.2L(标准状况)NO 气体生成,则电子转移的总数
是 。写出以上反应的离子方程式 。
四、推断题(方程式每个 3 分,其余每空 2 分,共 16 分)
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
- 3 -
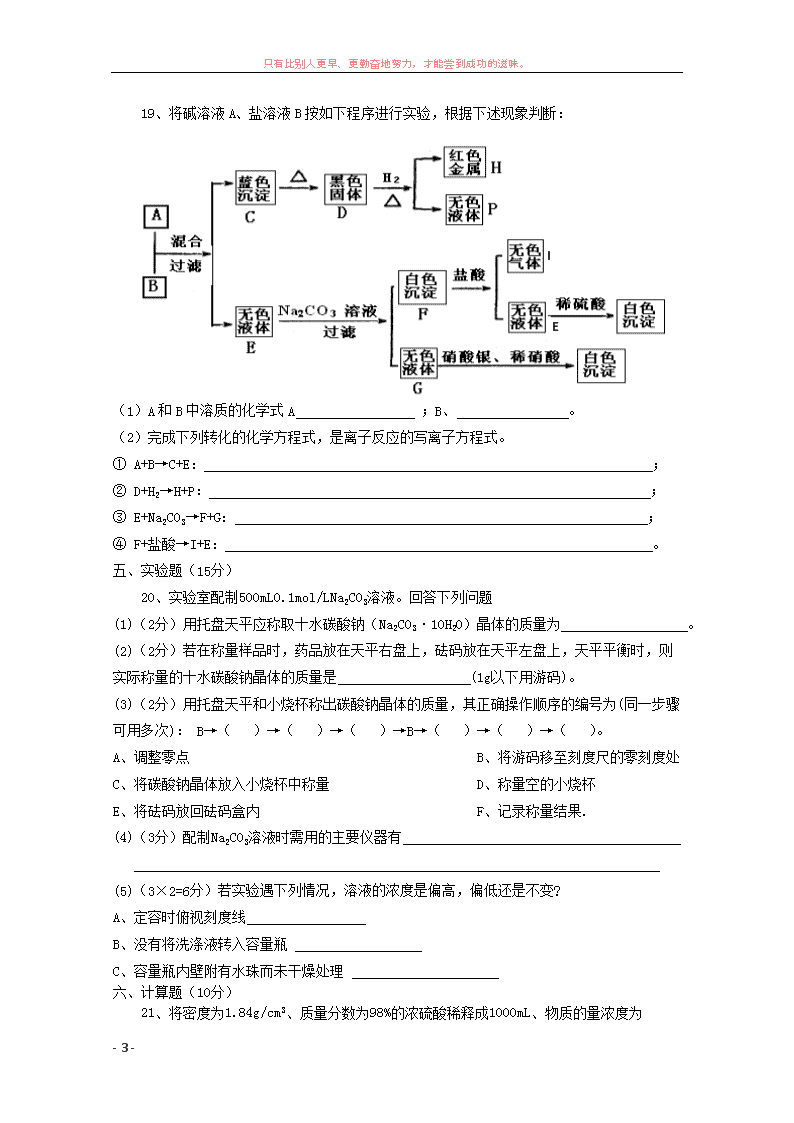
19、将碱溶液 A、盐溶液 B 按如下程序进行实验,根据下述现象判断:
(1)A 和 B 中溶质的化学式 A ;B、 。
(2)完成下列转化的化学方程式,是离子反应的写离子方程式。
① A+B→C+E: ;
② D+H2→H+P: ;
③ E+Na2CO3→F+G: ;
④ F+盐酸→I+E: 。
五、实验题(15分)
20、实验室配制500mL0.1mol/LNa2CO3溶液。回答下列问题
(1)(2分)用托盘天平应称取十水碳酸钠(Na2CO3·10H2O)晶体的质量为 。
(2)(2分)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,天平平衡时,则
实际称量的十水碳酸钠晶体的质量是 (1g以下用游码)。
(3)(2分)用托盘天平和小烧杯称出碳酸钠晶体的质量,其正确操作顺序的编号为(同一步骤
可用多次): B→( )→( )→( )→B→( )→( )→( )。
A、调整零点 B、将游码移至刻度尺的零刻度处
C、将碳酸钠晶体放入小烧杯中称量 D、称量空的小烧杯
E、将砝码放回砝码盒内 F、记录称量结果.
(4)(3分)配制Na2CO3溶液时需用的主要仪器有
(5)(3×2=6分)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?
A、定容时俯视刻度线
B、没有将洗涤液转入容量瓶
C、容量瓶内壁附有水珠而未干燥处理
六、计算题(10分)
21、将密度为1.84g/cm3、质量分数为98%的浓硫酸稀释成1000mL、物质的量浓度为2mol/L、
I
E
I
E
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
- 4 -
密度为1.10g/cm3的稀硫酸。求:(1)所需浓硫酸的体积;(2)所需水的体积。(水的密度
可视为1g/cm3)
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
- 5 -
参考答案
第Ⅰ卷(1-10 小题每小 2 分,11-16 小题每小题 4 分,共 44 分.)
题目 1 2 3 4 5 6 7 8 9 10
答案 A B D A A B C C D A
题目 11 12 13 14 15 16
答案 BD AC B AD D C
三、填空题(方程式 3 分,其余每空 2 分,共 15 分。)
四、推断题(方程式每个 3 分,其余每空 2 分,共 16 分)
19.(1)A、Ba(OH)2 B、CuCl2
(2)A+B→C+E:Cu2+ + 2OH- = Cu(OH)2↓
D+H2→H+P:H2 +CuO Cu + H2O
E+Na2CO3→F+G:Ba2+ + CO3
2- = BaCO3↓
F+盐酸→I+E:BaCO3 + 2H+ = Ba2+ + CO2↑+ H2O
五、实验题(15分)
六、计算题(10分)
21、(1)108.7mL ;(2)900mL。
相关文档
- 黑龙江省大庆市 2016-2017 学年高2021-07-0810页
- 高一化学必修一知识点总结特别精华2021-07-0845页
- 最新高一化学必修二全册知识点总结2021-07-0815页
- 2014《成才之路》高考化学一轮复习2021-07-0810页
- 河北省衡水中学 2016-2017 学年高2021-07-0817页
- 2016-2017 学年度下学期期中考试 2021-07-087页
- 高一化学必修一期中测试题2021-07-0810页
- 北京市第三十一中学2020-2021学年2021-07-0810页
- 人教版高一化学必修一知识点总结2021-07-0817页
- 高一化学必修1第一章-单元测试题及2021-07-083页