- 274.50 KB
- 2021-08-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
氯以及化合物的性质和应用
练习时间:40分钟,总分100分
一、 选择题:
1.一定条件下磷与干燥氯气反应,若0.25 g磷消耗掉314 mL氯气(标准状况),则产物中PCl3与PCl5的物质的量之比接近于 ( )
A.3∶1 B.5∶3 C.2∶3 D.1∶2
2.某同学在一张pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是 ( )
A.该实验说明Cl2分子具有漂白性
B.该实验说明H+的扩散速度比HClO分子快
C.将实验后的pH试纸在酒精灯上微热,试纸又恢复为原来的颜色
D.若用久置的氯水进行上述实验,现象完全相同
3.下列关于氯的说法正确的是 ( )。
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.Cl、Cl为不同的核素,有不同的化学性质
C.实验室制备Cl2,可用排饱和食盐水集气法收集
D.1.12 L Cl2含有1.7NA个质子(NA表示阿伏加德罗常数)
4.右图是模拟氯碱工业生产中检查氯气是否泄漏的装置,下列有关说法错误的是
A.烧瓶中立即出现白烟 B.烧瓶中立即出现红棕色
C.烧瓶中发生的反应表明常温下氨气有还原性
D.烧杯中的溶液是为了吸收有害气体
5.以下指定反应事实能用同一原理解释的是
A.Cl2与Fe、Cu反应均生成高价氯化物 B.NH4HCO3晶体、固体I2受热均能变成气体
C. SO2、Cl2均能使品红溶液褪色 D.ClO-与Fe2+、H+均不能大量共存
6.下列物质在空气中久置变质,在变质过程中,既有氧化还原反应发生,又有非氧化还原反
应发生的是
A.食盐 B.漂白粉 C.氯水 D.硫酸亚铁溶液
7.下列指定反应的离子方程式书写正确的是
A.氯气与水反应:Cl2+H2O=== 2H++Cl―+ClO―
B.氯气与氢氧化钠溶液反应:Cl2+2OH-=== Cl―+ClO―+H2O
C.浓盐酸与二氧化锰共热:MnO2+4HCl(浓) Mn2++2Cl―+Cl2↑+2H2O
D.漂白粉溶液通少量二氧化碳:Ca2++2ClO―+H2O+CO2=== CaCO3↓+2H++2ClO―
3
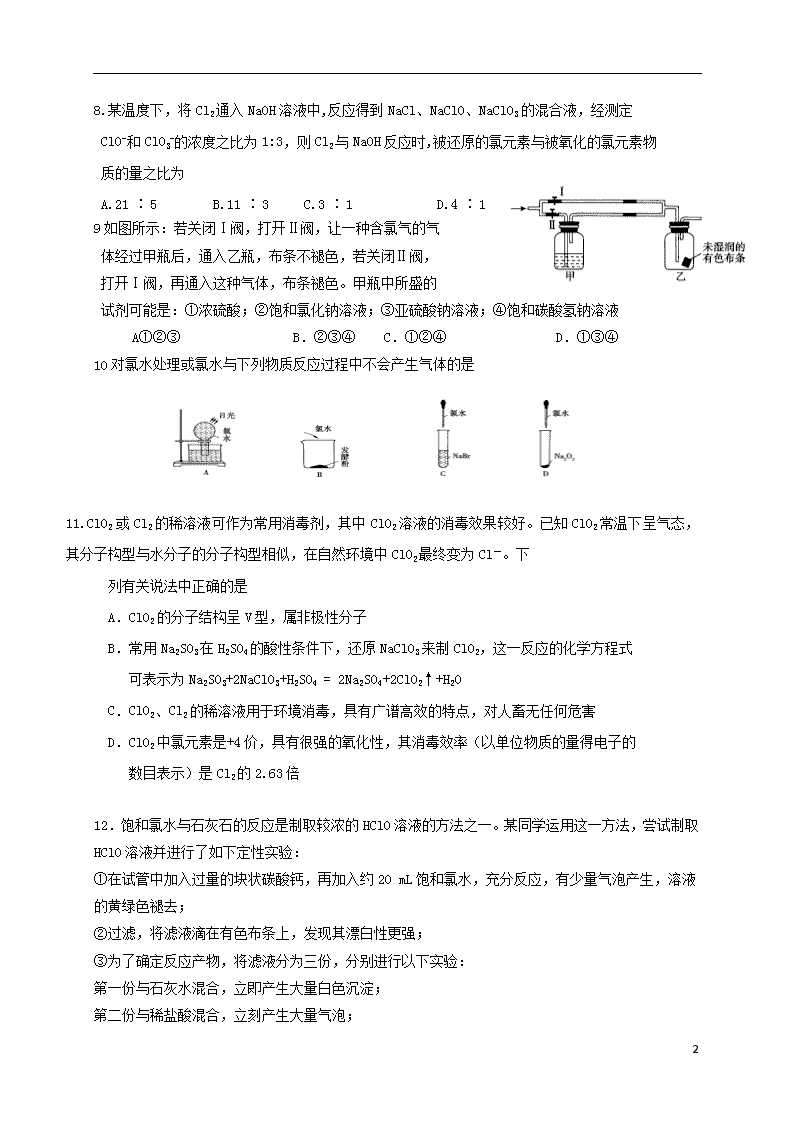
8.某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定
ClO-和ClO3-的浓度之比为1:3,则Cl2与NaOH反应时,被还原的氯元素与被氧化的氯元素物
质的量之比为
A.21 ∶5 B.11 ∶3 C.3 ∶1 D.4 ∶1
9如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含氯气的气
体经过甲瓶后,通入乙瓶,布条不褪色,若关闭Ⅱ阀,
打开Ⅰ阀,再通入这种气体,布条褪色。甲瓶中所盛的
试剂可能是:①浓硫酸;②饱和氯化钠溶液;③亚硫酸钠溶液;④饱和碳酸氢钠溶液
A①②③ B.②③④ C.①②④ D.①③④
10对氯水处理或氯水与下列物质反应过程中不会产生气体的是
11.ClO2或Cl2的稀溶液可作为常用消毒剂,其中ClO2溶液的消毒效果较好。已知ClO2常温下呈气态,其分子构型与水分子的分子构型相似,在自然环境中ClO2最终变为Cl-。下
列有关说法中正确的是
A.ClO2的分子结构呈V型,属非极性分子
B.常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式
可表示为Na2SO3+2NaClO3+H2SO4 = 2Na2SO4+2ClO2↑+H2O
C.ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害
D.ClO2中氯元素是+4价,具有很强的氧化性,其消毒效率(以单位物质的量得电子的
数目表示)是Cl2的2.63倍
12.饱和氯水与石灰石的反应是制取较浓的HClO溶液的方法之一。某同学运用这一方法,尝试制取HClO溶液并进行了如下定性实验:
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水,充分反应,有少量气泡产生,溶液的黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立刻产生大量气泡;
3
第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2气体。
(1)试解释可以在饱和氯水中加入石灰石制备HClO的原因:____________________________
____________________________________________________________________________________________________________________。
(2)写出步骤③中第一份及第二份滤液发生反应的离子方程式:
第一份________________________________________________________________________;
第二份________________________________________________________________________。
(3)试根据所学知识推测,在②的滤液中含有的溶质,除了溶解的极少量氯气外,还含有的其他溶质为__________________________________________(写化学式)。
13.为了探究新制饱和氯水的组成和性质而进行了科学实验:先观察了氯水的外观性质以后,
又用胶头滴管将该氯水逐滴滴入含有酚酞的NaOH溶液中,边滴边振荡,并连续观察现
象,发现溶液的红色逐渐褪去而得无色溶液。以下的一些问题需要请你来配合回答:
(1)请写出新制饱和氯水中含有氯元素物质的化学式:________________________。
(2)若不再进行更多的实验,请说明能快速判断氯水中含有Cl2的主要依据:
____________________________。
(3)根据预测,实验中溶液红色褪去的原因可能有两种,请用简要的文字说明之:
①_____________________________________________________________________。
②_____________________________________________________________________。
(4)他们又要通过实验进一步探究溶液红色褪去的原因究竟是上述中的①还是②。
[实验步骤]
①取试管内的无色溶液3 mL盛于另一支洁净的试管中;
②____________________________________________________________,振荡试管。
[实验现象及结论]
①若________,则证明溶液红色褪去的原因是①而不是②;
②若________,则证明溶液红色褪去的原因是②而不是①。
(5)为了从新制氯水中制得较高浓度的HClO,可向氯水中加入的试剂是________。
A.CaCO3 B.NaHSO3
C.H2SO4 D.Ca(OH)2
3
相关文档
- 高中化学必修1第3章 第1节 第2课时2021-08-066页
- 人教版高中化学必修1课件:4_4氨硝酸2021-08-0627页
- 高中化学 单元质量评估(一)新人教版2021-08-0610页
- 高中化学:人教版必修一 第三章《重2021-08-067页
- 2019高中化学 第二章 化学物质及其2021-08-065页
- 2019-2020学年高中化学课时作业212021-08-067页
- 2020年高中化学 专题过关检测(四)化2021-08-0614页
- 2019-2020版高中化学(人教版 选修3)2021-08-067页
- 高中化学必修1人教版课时练习及章2021-08-067页
- 人教版高中必修一化学课件:4_2富集2021-08-0634页