- 189.00 KB
- 2021-11-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
实验专题(四) 碱变质的探究
类型1 氢氧化钠变质的探究
1.(2018·滨州)小明完成中和反应实验几天后发现,忘记盖上盛放氢氧化钠溶液试剂瓶的瓶塞,请帮助小明完成如下实验方案来检验氢氧化钠溶液是否变质。
实验方案
实验步骤
实验现象
实验结论
方案一
取少量溶液于试管中,滴加几滴稀盐酸
没有气体产生
没有变质
方案二
取少量溶液于试管中,滴加几滴氯化钡溶液
__产生白色沉淀__
已经变质
(1)请写出方案二中发生反应的化学方程式__BaCl2+Na2CO3===BaCO3↓+2NaCl__。
(2)你认为方案一的实验设计是否正确?__不正确__(填“正确”或“不正确”),请说明理由__在氢氧化钠和碳酸钠的混合液中,滴入少量稀盐酸时,稀盐酸先与氢氧化钠反应__。
2.实验室有一瓶敞放着的氢氧化钠固体,同学们想探究这瓶固体的成分,请你一同参与探究并回答有关问题。
请你写出氢氧化钠在空气中变质的化学方程式:__2NaOH+CO2===Na2CO3+H2O__,可加入试剂__稀盐酸__,如有气泡产生则氢氧化钠变质。
【提出猜想】
猜想1:这瓶固体的成分是NaOH;
猜想2:这瓶固体的成分是__Na2CO3__;
猜想3:这瓶固体的成分是NaOH和Na2CO3的混合物。
【实验与结论】
(1)取少量样品于试管中,加入适量蒸馏水,振荡,样品全部溶于水,向其中加入无色酚酞溶液,溶液由无色变成红色。甲同学认为这瓶固体含有NaOH,猜想1正确。乙同学认为甲同学的结论不正确,其理由是__Na2CO3的水溶液也呈碱性__。
(2)向(1)溶液中加入过量的CaCl2溶液,生成白色沉淀,沉淀后静置,溶液由红色变成无色。同学们认为猜想__2__是正确的。
【问题讨论】
(3)丙同学认为实验时也可以先加入过量的CaCl2溶液,振荡、静置,然后在上层清液中加入无色酚酞溶液,你认为丙同学的说法__正确__(填“正确”或“不正确”),此时反应的化学方程式为__CaCl2+Na2CO3===CaCO3↓+2NaCl__;若猜想3正确,则现象为__有白色沉淀生成,上层清液变红__,其中无色酚酞溶液还可用一种盐溶液,如__CuCl2__(写化学式)来代替验证猜想。
(4)丁同学认为CaCl2溶液也可以改为Ca(OH)2溶液,你认为丁同学的说法__不正确__(填“正确”或“不正确”),理由是__会生成新的NaOH,无法检验原来样品中的NaOH__。
3.(2017·菏泽)实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过询问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组的同学进行了如下的探究活动:
【进行猜想】
猜想Ⅰ:原溶液的溶质是NaCl;
猜想Ⅱ:原溶液的溶质是NaOH;
猜想Ⅲ:原溶液的溶质是Na2CO3;
猜想Ⅳ:原溶液的溶质是NaHCO3。
3
【查阅资料】
常温下,有关物质的相关信息如下表:
物质
NaCl
NaOH
Na2CO3
NaHCO3
常温下的
溶解度/g
36
109
21.5
9.6
常温下稀
溶液的pH
7
13
11
9
从物质的相关信息可知,原溶液的溶质一定不是NaHCO3,因为__常温下,碳酸氢钠的溶解度是9.6__g,不可能制得溶质质量分数为10%的溶液__。
【进行实验】
(1)取少量样品,测得溶液的pH大于7,则原溶液的溶质肯定不是__氯化钠__。
(2)同学们另取样品又进行了如下实验,实验过程如下:
①生成白色沉淀A的化学方程式为__CaCl2+Na2CO3===CaCO3↓+2NaCl__。
②通过实验可以判断样品无色溶液中含有的溶质有__Na2CO3、NaOH__。
【获得结论】实验完成后,最终得到的结论:原瓶中的溶质是__NaOH__,且已变质。
类型2 氢氧化钙变质的探究
4.(2018·聊城)某化学学习小组的同学对一瓶敞口放置的氢氧化钙固体的化学成分产生了兴趣,他们根据自己所学知识进行如下探究:
【提出问题】该瓶药品的化学成分是什么?
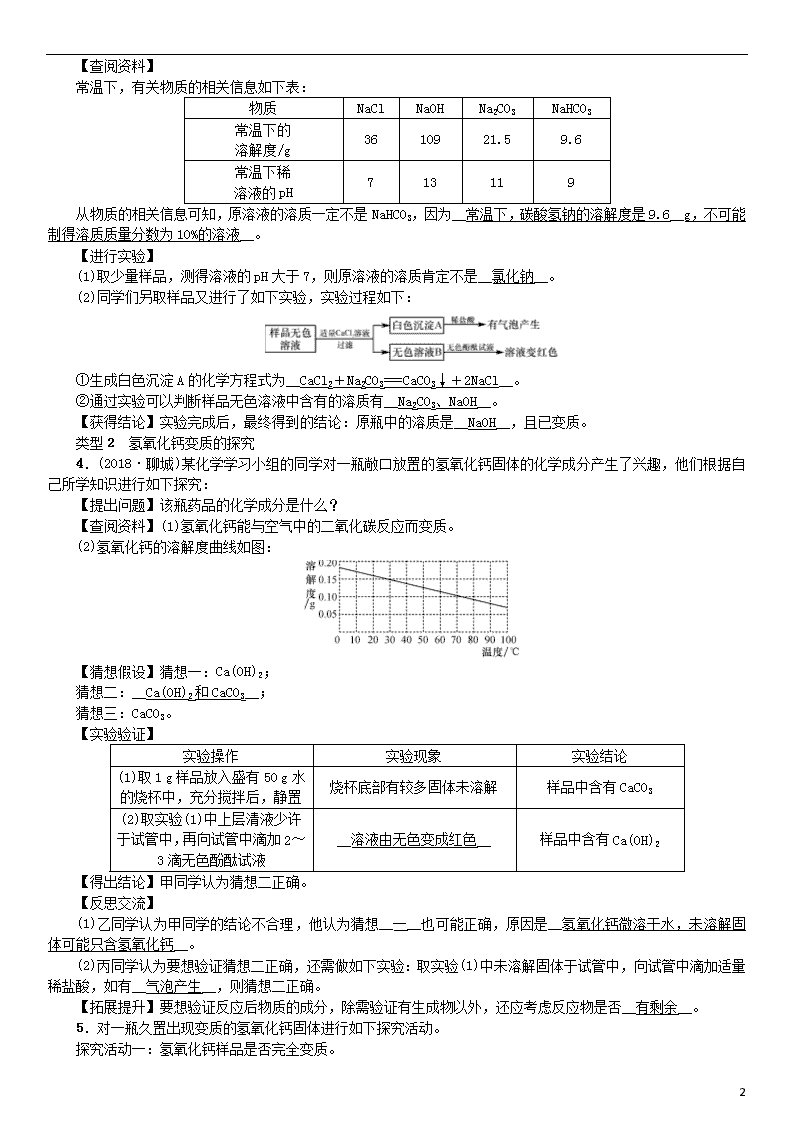
【查阅资料】(1)氢氧化钙能与空气中的二氧化碳反应而变质。
(2)氢氧化钙的溶解度曲线如图:
【猜想假设】猜想一:Ca(OH)2;
猜想二:__Ca(OH)2和CaCO3__;
猜想三:CaCO3。
【实验验证】
实验操作
实验现象
实验结论
(1)取1 g样品放入盛有50 g水的烧杯中,充分搅拌后,静置
烧杯底部有较多固体未溶解
样品中含有CaCO3
(2)取实验(1)中上层清液少许于试管中,再向试管中滴加2~3滴无色酚酞试液
__溶液由无色变成红色__
样品中含有Ca(OH)2
【得出结论】甲同学认为猜想二正确。
【反思交流】
(1)乙同学认为甲同学的结论不合理,他认为猜想__一__也可能正确,原因是__氢氧化钙微溶于水,未溶解固体可能只含氢氧化钙__。
(2)丙同学认为要想验证猜想二正确,还需做如下实验:取实验(1)中未溶解固体于试管中,向试管中滴加适量稀盐酸,如有__气泡产生__,则猜想二正确。
【拓展提升】要想验证反应后物质的成分,除需验证有生成物以外,还应考虑反应物是否__有剩余__。
5.对一瓶久置出现变质的氢氧化钙固体进行如下探究活动。
探究活动一:氢氧化钙样品是否完全变质。
3
(1)检验氢氧化钙样品是否完全变质,进行如下实验:
实验步骤
实验现象
实验结论
取氢氧化钙样品少量,研细后加适量蒸馏水充分混合后静置,__取上层清液于试管中,滴加1~2滴无色酚酞试液(或通入二氧化碳气体)__
__酚酞试液变红色(或溶液变浑浊)__
样品中还含有氢氧化钙
探究活动二:测定样品中含有的变质固体(以下用R表示)的质量分数
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数。实验装置(气密性良好)如图1所示。
(2)将稀盐酸滴入样品中,产生气体的化学方程式为__CaCO3+2HCl===CaCl2+H2O+CO2↑__,反应一段时间后,当观察到__无气泡产生__(填实验现象),才停止滴加稀盐酸。
(3)实验中量筒的作用是__根据进入量筒内水的体积,测量生成的二氧化碳体积__。
(4)实验结束后,量筒内进入水的体积如图2所示,其读数为__165__mL。
3
相关文档
- 初中语文PPT教学课件:16 中国人失掉2021-11-0625页
- 2019年初中语文知识点整理常见错别2021-11-062页
- 2020年邵阳市初中毕业学业考试数学2021-11-069页
- 人教版初中九年级化学上学期第六单2021-11-0611页
- 初中记叙文常见考题答题格式2021-11-064页
- 2020届初中物理章节复习 第11章 功2021-11-0613页
- 2019年初中语文基础知识点专题讲练2021-11-0620页
- 初中地理学业水平考试复习专项训练2021-11-0613页
- 初中历史中考《世界史》必考考点汇2021-11-016页
- 初中地理最新必考知识点汇总2021-11-0134页