- 249.00 KB
- 2021-11-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
十单元技能过关训练
可能用到相对原子质量 H:1 O:16 Na:23 Cl:35.5 Ca:40
一、选择题(每小题 1 分,共 10 分,每小题只有一个选项符合题意)
1.关于酸和碱的性质说法正确的是 ( )
A.用盐酸不能洗掉敞口盛放石灰水试剂瓶内壁的白色固体
B.用稀硫酸可洗掉试管里残存的红褐色氢氧化铁
C.酸具有一些相似的化学性质,原因是它们都能与金属反应有氢气产生
D.碱具有一些相似的化学性质,原因是它们都能与空气中的二氧化碳反应
2. 下列化学实验操作不正确的是 ( )
A.过滤时,用玻璃棒引流液体
B.溶解粗盐时,用温度计搅拌以加速溶解
C.称量少量氢氧化钠固体时,放在小烧杯中称量
D.稀释浓硫酸时,把浓硫酸沿烧杯内壁慢慢注入盛有水的烧杯中并不断搅拌
3.下列气体不能用固体的氢氧化钠干燥的是 ( )
A.一氧化碳 B.氢气 C.二氧化碳 D.氧气
4.下列物质敞口放置在空气中较长时间后,质量会增加且不发生化学变化的是 ( )
A.浓硫酸 B.浓盐酸 C.烧碱 D.熟石灰
5.下列实例不属于中和反应的是 ( )
A.土壤酸化后加入熟石灰改良
B.胃酸分泌过多的病人遵医嘱服用含有氢氧化铝的药物以中和过多胃酸
C.蚊虫叮咬人的皮肤分泌出蚁酸,如果涂含碱性物质的药水就可减轻痛痒
D.金属表面锈蚀后,可用稀盐酸进行清洗
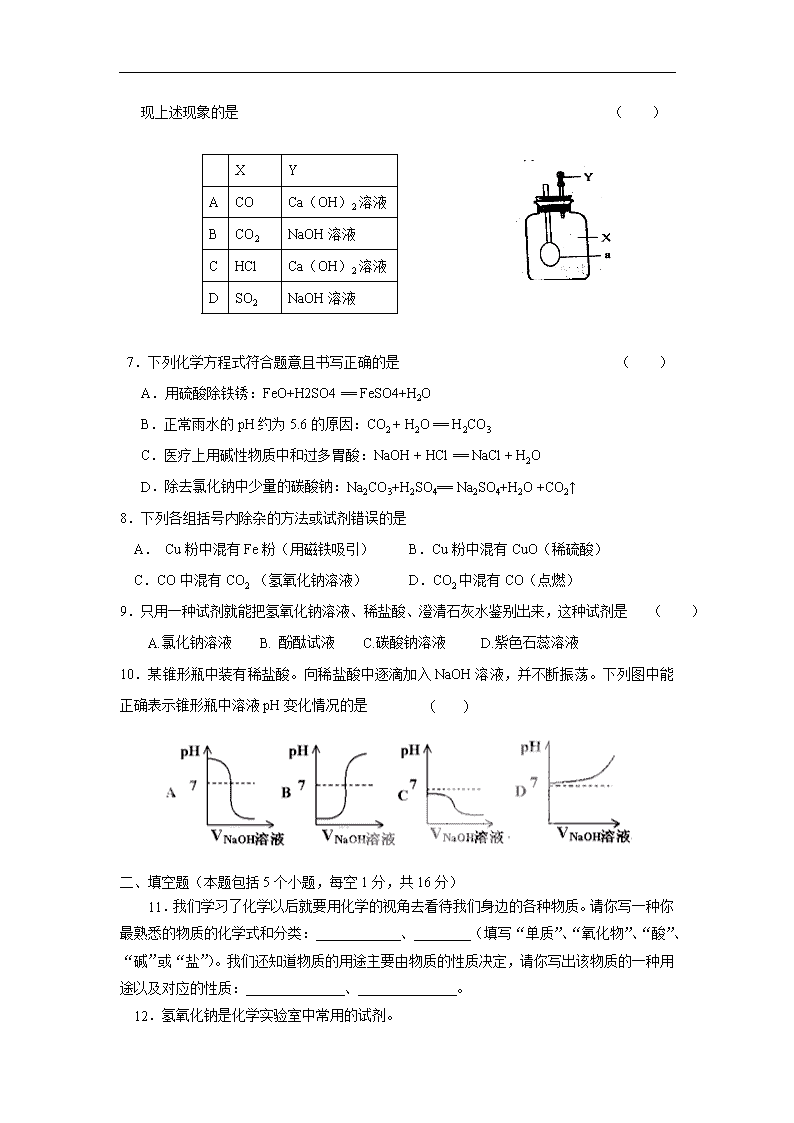
6.如图所示、广口瓶中盛有气体 X,胶头滴管中盛有液体 Y,若挤压胶头滴管使液体
滴入广口瓶中,振荡,一段时间后可见小气球 a 膨胀鼓起。下表中的各组物质不会出
现上述现象的是 ( )
7.下列化学方程式符合题意且书写正确的是 ( )
A.用硫酸除铁锈:FeO+H2SO4 == FeSO4+H2O
B.正常雨水的 pH 约为 5.6 的原因:CO2 + H2O == H2CO3
C.医疗上用碱性物质中和过多胃酸:NaOH + HCl == NaCl + H2O
D.除去氯化钠中少量的碳酸钠:Na2CO3+H2SO4== Na2SO4+H2O +CO2↑
8.下列各组括号内除杂的方法或试剂错误的是
A. Cu 粉中混有 Fe 粉(用磁铁吸引) B.Cu 粉中混有 CuO(稀硫酸)
C.CO 中混有 CO2 (氢氧化钠溶液) D.CO2 中混有 CO(点燃)
9.只用一种试剂就能把氢氧化钠溶液、稀盐酸、澄清石灰水鉴别出来,这种试剂是 ( )
A.氯化钠溶液 B. 酚酞试液 C.碳酸钠溶液 D.紫色石蕊溶液
10.某锥形瓶中装有稀盐酸。向稀盐酸中逐滴加入 NaOH 溶液,并不断振荡。下列图中能
正确表示锥形瓶中溶液 pH 变化情况的是 ( )
二、填空题(本题包括 5 个小题,每空 1 分,共 16 分)
11.我们学习了化学以后就要用化学的视角去看待我们身边的各种物质。请你写一种你
最熟悉的物质的化学式和分类: 、 (填写“单质”、“氧化物”、“酸”、
“碱”或“盐”)。我们还知道物质的用途主要由物质的性质决定,请你写出该物质的一种用
途以及对应的性质: 、 。
12.氢氧化钠是化学实验室中常用的试剂。
X Y
A CO Ca(OH)2 溶液
B CO2 NaOH 溶液
C HCl Ca(OH)2 溶液
D SO2 NaOH 溶液
(1)氢氧化钠固体曝露在空气中,容易吸收水分而使表面覆盖一层溶液(这一现象又叫
“潮解”);它还能 ,
这一变化的化学方程式可表示为: 。所以氢氧
化钠固体必须密封保存。
(2)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻
璃中的二氧化硅缓慢地发生反应,产物使瓶口与瓶塞粘合在一起,反应的化学方程式为:
SiO2 + 2NaOH == Na2SiO3 + X,试推断 X 的化学式为 。
13.用化学方程式说明问题:
(1)用盐酸除铁锈 ;
(2)烧水的铝壶中常结有一层水垢(水垢的主要成分是 CaCO3),用适量的稀盐酸可以将
它除去,反应的化学方程式是 ,若盐酸的用
量过多,会损坏铝壶,反应的化学方程式是 ;
(3)用氢氧化钠溶液来吸收有毒的二氧化硫气体 。
14.某校“酸雨”测量小组的同学,取刚降落的雨水的水样,用 pH 探头(测 pH 的仪器)
每隔五分钟测一次 pH,其数据见下表:
测定时间 3:10 3:15 3:20 3:25 3:30 3:35 3:40
pH 4.95 4.95 4.94 4.88 4.86 4.85 4.84
(1)根据所学知识,推测出“正常雨水”的 pH<7,引起这种 pH 的原因是
;
(2)根据以上数据,判断所降雨水是否为“酸雨”? 。
15.用熟石灰中和一定量的盐酸时,溶液的 pH 与加入的熟
石灰质量的关系如右图所示。熟石灰与盐酸反应的化学方程式
为 ;当加入熟石灰 mg 时,
溶液中的溶质为 。若改用 ng 氢氧化钠与相
同量盐酸反应,所得溶液的 pH 7(填“>"、“<"或“=”)o
三、简答题(本题包括 4 个小题,共 12 分)
16.(2 分)写出下列反应的化学方程式,并注明所属基本反应类型。
(1)镁条在二氧化碳中燃烧生成氧化镁和黑色炭粉末。
(2)用熟石灰中和硫酸厂污水中的硫酸。
17.(3 分) 某同学用如右图所示装置来测定空气中氧气的含量。
请回答下列问题:
(1)该实验中燃烧物为什么用红磷?
(2)实验完成后,若进入集气瓶中的水不足原空气体积的 1/5,
你认为导致这一结果的原因可能是什么?(写一条即可)
(1) 该同学考虑到燃烧后的产物五氧化二磷会污染空气,想把红磷改为木炭,他计划对
实验稍作改动,你认为他如何来对实验进行改动?
18.(3 分) (1) 西瓜适宜生长在 pH 为 6~7 的土壤中。设计实验检验某块土地是否适合种
植西瓜,请简述实验操作步骤。(2)若测得该块土地的 pH 为 5,为利于种植西瓜,应选用
哪种物质改良该块土地的土壤?
19.(4 分)某化学兴趣小组设计了下列三组实验装置,试图通过观察实验现象说明 CO2 与
NaOH 溶液可能发生了反应。
(1)请写出 CO2 与过量的 NaOH 发生反应的化学方程式。
(2)选择任意一组装置,简述预计出现的实验现象,解释产生该现象的原因。
四、综合应用题(共 12 分)
20.通过学习碱的性质,我校化学兴趣小组的同学对实验室的“氢氧化钙是否变质以及变质
的程度”展开了探究活动,请你一同参与:
(1)提出问题:氢氧化钙是否变质?
(2)猜想与假设:同学们经过讨论认为样品存在三种可能情况:没有变质;部分变质;完
全变质。
(3)实验探究:
实验步骤及操作 实验现象 实验结论
取样于试管中,加入足
量蒸馏水振荡,静置
1 取上层清液,滴入
无色酚酞试液
2 倒去上层清液,再向
试管中注入稀盐酸
若:①无色酚酞试液不变红
②有气泡产生
全部变质
若:①无色酚酞试液变红
②
若:①
②没有气泡产生
⑷小结与思考: 同学们根据上述实验方案进行实验,确定该样品已部分变质,请写出氢氧
化钙变质及实验中涉及的化学反应方程式:
、 。
(5)澄清的石灰水与稀盐酸反应没有明显外观现象。请你帮助他们找出实验方法,能通过
明显的外观现象,证明澄清的石灰水与稀盐酸反应,并且能控制它们在恰好完全反应时停止
实验。(已知氯化钙、硫酸钙、硝酸钙的水溶液呈中性)
(6)同学们为了测定氢氧化钙变质的程度,取已部分变质样品 20g 放入烧杯中,向其中
加入 100g 一定质量分数的稀盐酸,二者恰好完全反应。反应结束后,称量烧杯中剩余物质
的总质量为 117.8g(不包括烧杯的质量,且气体溶解忽略不计)。试计算氢氧化钙的纯度是
多少?
参考答案
一、选择题(共计 10 分)
题号 1 2 3 4 5 6 7 8 9 10
答案 B B C A D A B D C B
二、填空题(共计 16 分)
11.浓硫酸;酸;干燥剂;吸水性(其他合理答案均可)
12.(1)吸收二氧化碳(或与二氧化碳反应); 2NaOH+CO2==Na2CO3+H2O
(2)H2O
13.(1)Fe2O3 + 6HCl === 2FeCl3 + 3H2O
(2)CaCO3 + 2HCl ===CaCl2 + H2O + CO2↑; 2Al + 6HCl === 2AlCl3 + H2↑
(3)SO2 + 2NaOH === Na2SO3 + H2O
14.(1) 空气中的二氧化碳溶于雨水生成碳酸所致。 (2)是。
15.Ca(OH)2 + 2HCl ==== CaCl2 + 2H2O ;CaCl2 和 HCl ; <
三、简答题(共计 12 分)
四、综合应用题(共 12 分)
20.(3)实验探究:②有气泡产生;部分变质;①无色酚酞试液变红;没有变质;
相关文档
- 人教版化学九下第12单元测试卷2021-11-065页
- 部编版九年级历史(上册)第七单元测试2021-11-0612页
- 九年级语文上册第一单元测试题含答2021-11-066页
- 人教版九年级化学下册第八九单元测2021-11-0613页
- 部编版九年级历史(下册)第五单元测试2021-11-0611页
- 鲁教版九年级化学第八单元测试题含2021-11-066页
- 人教版九年级数学上册单元测试题2021-11-0652页
- 新人教版九年级物理上学期单元测试2021-11-0627页
- 人教版九年级化学(下册)第十一单元测2021-11-0610页
- 2019九年级历史上册 第六、七单元2021-11-065页