- 13.11 MB
- 2022-04-01 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第11课时溶液的酸碱性及中和反应第一篇 基础过关
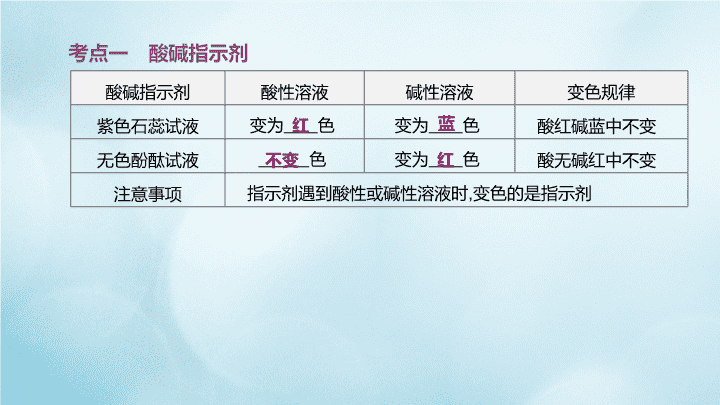
酸碱指示剂酸性溶液碱性溶液变色规律紫色石蕊试液变为色变为色酸红碱蓝中不变无色酚酞试液色变为色酸无碱红中不变注意事项指示剂遇到酸性或碱性溶液时,变色的是指示剂考点一 酸碱指示剂红蓝不变红
考点二pH1.pH与酸碱性的关系图11-1pH7:溶液呈酸性,pH越,酸性越强。pH7:溶液呈性。pH7:溶液呈碱性,pH越,碱性越强。<小=中>大
2.pH的测定在的玻璃片或白瓷板上放一片pH试纸,用蘸取待测溶液,滴到试纸上,立即将试纸显示的颜色与对照,读出对应的pH。洁净干燥洁净干燥的玻璃棒标准比色卡
[注意]①试纸不可直接伸入试剂中,以免污染试剂。②测定溶液的pH时,试纸不可事先用蒸馏水润湿,因为润湿试纸相当于稀释被检验的溶液,这样可能会导致测量结果不准确。若该溶液为酸性溶液,则所测pH偏大;若该溶液为碱性溶液,则所测pH偏小。③用pH试纸只能粗略地测定溶液的酸碱度,测得的pH是整数而不能是小数。
概念酸与碱作用生成和的反应与复分解反应的关系属于复分解反应现象现象常不明显,可通过指示反应情况应用改良土壤,如酸性土壤中加入来改良用于医药,如胃酸过多,可服用含氢氧化铝的药物;被蚊虫叮咬,因蚊虫能分泌出蚁酸,可涂稀氨水减轻痛痒处理工厂废水,如用熟石灰处理工厂含有硫酸的废水:(写化学方程式)考点三 酸碱中和反应盐水酸碱指示剂熟石灰Ca(OH)2+H2SO4CaSO4+2H2O
考点四 化学反应的类型图11-2
考向一 酸碱指示剂(6年2考)1.[2019·郴州]下列溶液能使紫色石蕊试液变成蓝色的是()A.澄清石灰水B.NaCl溶液C.稀硫酸D.KNO3溶液[答案]A[解析]澄清石灰水显碱性,能使紫色石蕊试液变成蓝色;氯化钠溶液、KNO3溶液显中性,不能使紫色石蕊试液变色;稀硫酸显酸性,能使紫色石蕊试液变红色。
2.[2018·凉山]阿依、阿卓、阿牛春游时,发现了一株被太阳晒成紫红色的蒲公英,他们将其带回家洗净、捣碎,用阿达喝的老白干浸泡,再用纱布过滤,取其汁液,将其分成两份。已知紫红色蒲公英汁与紫色石蕊性质相同,请您预测:向一份中滴入食醋,会显色,向另一份中滴加餐具洗洁精,会显色。[答案]红 蓝[解析]已知紫红色蒲公英汁与紫色石蕊性质相同,食醋显酸性,餐具洗洁精显碱性,所以向一份中滴入食醋,会显红色,向另一份中滴加餐具洗洁精,会显蓝色。
3.[2019·鄂尔多斯]从玫瑰花瓣中提取的花青素(紫色)可制成酸碱指示剂,滴入不同试剂中颜色变化如下表。结合表中信息回答:(1)NH4Cl溶液呈(填“酸性”“碱性”或“中性”),用作化肥长期施用的结果是。(2)向某无色溶液中滴入花青素,溶液变蓝色,则此溶液中一定不存在Na+、K+、中的(填离子符号)。(3)胃溃疡患者不用碳酸氢钠片治疗胃酸过多症的原因是(用化学方程式表示)。试剂NaCl溶液盐酸NaHCO3溶液NH4Cl溶液NaOH溶液颜色紫红蓝红蓝酸性使土壤酸化、板结(写出其中之一即可)NaHCO3+HClNaCl+H2O+CO2↑
考向二pH与酸碱性4.[2019·南京]一些食物的近似pH如下,其中显碱性的是()A.鸡蛋清7.6~8.0B.葡萄汁3.5~4.5C.番茄汁4.0~4.4D.苹果汁2.9~3.3[答案]A[解析]鸡蛋清的pH为7.6~8.0,大于7,显碱性;葡萄汁的pH为3.5~4.5,小于7,显酸性;番茄汁的pH为4.0~4.4,小于7,显酸性;苹果汁的pH为2.9~3.3,小于7,显酸性。
5.[2019·滨州]下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是()A.用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量B.先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量C.用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照D.用pH试纸测得该氢氧化钠溶液的pH=12.6
[答案]C[解析]测定未知溶液的pH时,正确的操作方法为用干燥洁净的玻璃棒蘸取少量待测液滴在干燥的pH试纸上,并与标准比色卡对比,确定pH。不能将pH试纸伸入待测液中,以免污染待测液;氢氧化钠溶液显碱性,用水湿润pH试纸,稀释了待测溶液,使测定结果偏小;标准比色卡上的数字只有整数,用pH试纸测得该氢氧化钠溶液的pH不能带小数。
6.[2019·天津]一些物质的近似pH如图11-3所示,下列有关说法正确的是()图11-3A.苹果汁的酸性比纯鲜牛奶的酸性弱B.肥皂水的碱性比炉具清洁剂的碱性强C.厕所清洁剂与炉具清洁剂能混用D.人被某些蚊虫叮咬后可涂抹肥皂水以减轻痛痒
[答案]D[解析]苹果汁的pH约为3,纯鲜牛奶的pH约为6~7,pH越小,酸性越强,所以苹果汁的酸性比纯鲜牛奶的酸性强;肥皂水的pH约为10,炉具清洁剂的pH约为12~13,pH越大,碱性越强,所以肥皂水的碱性比炉具清洁剂的碱性弱;厕所清洁剂呈酸性,炉具清洁剂呈碱性,二者能发生反应导致试剂失效,所以不能混合使用;某些蚊虫叮咬后会产生蚁酸,而肥皂水显碱性,能与蚁酸反应减轻疼痛,所以人被某些蚊虫叮咬后可涂抹肥皂水以减轻痛痒。
考向三 酸碱中和反应的探究7.某兴趣小组对中和反应进行如图11-4所示的实验探究。图11-4[探究活动一]借助无色酚酞试液,证明酸碱发生了反应。甲同学按图Ⅰ进行实验,证明了盐酸和NaOH溶液能发生化学反应,他依据的实验现象是,写出该反应的化学方程式:。
[答案][探究活动一]溶液由红色变为无色NaOH+HClNaCl+H2O[解析][探究活动一]无色酚酞试液在氢氧化钠溶液中显红色,滴加了稀盐酸后变成了无色,说明盐酸与氢氧化钠发生了反应,化学方程式为NaOH+HClNaCl+H2O。
7.某兴趣小组对中和反应进行如图11-4所示的实验探究。图11-4[探究活动二]检验反应生成的水,证明酸碱发生了反应。乙同学取硅胶(一种不与酸、碱反应的干燥剂,吸水后由蓝色变为红色)、无水醋酸(一种酸,常温下为液体)和固体氢氧化钠进行图Ⅱ所示的三个实验。(1)实验①和②可以作为参照,其目的是。
[答案][探究活动二](1)证明无水醋酸和氢氧化钠固体中不含水[解析][探究活动二](1)通过实验①②的现象,证明了无水醋酸和氢氧化钠不含水,不能使硅胶变色;由实验③硅胶变色,说明反应有水生成,证明酸、碱发生了反应。
7.某兴趣小组对中和反应进行如图11-4所示的实验探究。图11-4[探究活动二]检验反应生成的水,证明酸碱发生了反应。乙同学取硅胶(一种不与酸、碱反应的干燥剂,吸水后由蓝色变为红色)、无水醋酸(一种酸,常温下为液体)和固体氢氧化钠进行图Ⅱ所示的三个实验。(2)加入试剂后迅速塞紧橡皮塞的原因是。
[答案][探究活动二](2)防止空气中的水蒸气进入试管,干扰实验[解析][探究活动二](2)空气中含有水蒸气,也能使硅胶变色,迅速塞紧橡皮塞可防止空气中的水分进入试管,干扰实验。
7.某兴趣小组对中和反应进行如图11-4所示的实验探究。图11-4[探究活动二]检验反应生成的水,证明酸碱发生了反应。乙同学取硅胶(一种不与酸、碱反应的干燥剂,吸水后由蓝色变为红色)、无水醋酸(一种酸,常温下为液体)和固体氢氧化钠进行图Ⅱ所示的三个实验。(3)能证明酸和碱反应有水生成的现象是。
[答案][探究活动二](3)实验①②中硅胶不变色,③中硅胶由蓝色变为红色[解析][探究活动二](3)能证明酸和碱反应有水生成的现象是实验①②中硅胶不变色,③中硅胶由蓝色变为红色。
7.某兴趣小组对中和反应进行如图11-4所示的实验探究。图11-4[探究活动二]检验反应生成的水,证明酸碱发生了反应。乙同学取硅胶(一种不与酸、碱反应的干燥剂,吸水后由蓝色变为红色)、无水醋酸(一种酸,常温下为液体)和固体氢氧化钠进行图Ⅱ所示的三个实验。(4)实验③中反应的化学方程式为CH3COOH+NaOHCH3COONa+H2O,中和3g的无水醋酸(化学式为CH3COOH)需要g氢氧化钠固体。
[答案](4)2
考向四 化学反应的类型(6年2考)
[答案]D[解析]一氧化碳和氧气反应生成二氧化碳,属于“多变一”,是化合反应;碳酸分解生成水和二氧化碳,属于“一变多”,是分解反应;氢氧化钠和盐酸生成盐和水,是复分解反应;铝和盐酸反应生成氯化铝和氢气,是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应。
9.[2018·本溪]关于化学反应类型的说法正确的是()A.分解反应一定有单质生成B.化合反应一定是两种物质生成另一种物质C.置换反应一定有元素的化合价发生改变D.两种化合物生成另外两种化合物的反应一定是复分解反应
[答案]C[解析]分解反应不一定有单质生成,如碳酸分解生成水和二氧化碳;化合反应不一定是两种物质生成另一种物质,也可能是两种以上物质反应生成一种物质;置换反应是一种单质和一种化合物生成另一种单质和另一种化合物的反应,单质中元素的化合价为0,置换反应一定有元素的化合价发生改变;两种化合物生成另外两种化合物的反应不一定是复分解反应,如CO2+Ca(OH)2CaCO3↓+H2O。
10.[2019·宿迁]推理是学习化学时常用的思维方式。以下推理结果正确的是()A.用洗洁精洗油污是乳化作用,用汽油洗油污也是乳化作用B.NaOH溶液能使无色酚酞试液变红色,Cu(OH)2也能使无色酚酞试液变红色C.化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物D.复分解反应有沉淀、气体或水生成,有沉淀、气体或水生成的反应是复分解反应
[答案]C[解析]洗洁精除去油污是乳化作用,汽油能除去油污是因为汽油能溶解油污;碱的溶液能使无色酚酞试液变成红色,氢氧化钠能溶于水形成溶液,而Cu(OH)2难溶于水,不能使无色酚酞试液变红色;化合物是由不同种元素组成的纯净物,只含一种元素的物质可能是单质,也可能是混合物,但一定不是化合物;复分解反应发生的条件是有沉淀、气体或水生成,但有沉淀、气体或水生成的反应不一定是复分解反应。
11.[2016·宿迁]下列归纳和总结完全正确的一组是()A.化学反应基本类型①化合反应:4P+5O22P2O5②分解反应:H2CO3H2O+CO2↑③置换反应:3CO+Fe2O32Fe+3CO2B.化学反应中常见的“三”①煤、石油、天然气——三大化石燃料②塑料、合成纤维、合成橡胶——三大合成材料③分子、原子、离子——构成物质的三种粒子
(续表)C.对鉴别方法的认识①区分氮气和氧气——伸入带火星的木条②区分棉纤维和羊毛纤维——点燃后闻气味③区分硫酸铵和氯化铵——加熟石灰粉末研磨D.化学与生活①用甲醛水溶液浸泡水产品防腐②缺乏维生素C易患坏血病③自行车支架喷油漆防锈
[答案]B[解析]置换反应是一种单质与一种化合物反应生成另一种单质和另一种化合物的反应。A项的③中反应物为两种化合物,故不属于置换反应。硫酸铵和氯化铵加熟石灰粉末研磨都会生成有刺激性气味的气体,故用此法不能区分。甲醛属于有毒物质,不能用甲醛水溶液浸泡水产品。
12.[2019·宿迁]下列图像不能正确反映对应变化关系的是()A.①表示向pH=2的盐酸中不断加入NaOH溶液B.②表示一定量的Fe加到AgNO3溶液中C.③表示在20℃时,向一定量的水中不断加入KNO3晶体D.④表示等质量的Mg和Zn分别加足量盐酸图11-5
[答案]B[解析]①向一定量pH=2的盐酸中不断加入NaOH溶液,开始时溶液的pH小于7,恰好完全反应时pH等于7,氢氧化钠过量时溶液的pH大于7;②铁和硝酸银反应生成硝酸亚铁和银,反应过程中固体质量先增大,反应结束,质量不变;③刚开始时溶质质量分数为0,当不断加入硝酸钾晶体时,溶质的质量在不断增加,溶质的质量分数逐渐增大,当溶液饱和,硝酸钾不再溶解时,溶质的质量分数不再变化;等质量的稀盐酸分别与镁和锌完全反应,产生的氢气一样多,稀盐酸过量时,等质量的镁和锌与盐酸反应,产生氢气的质量镁比锌多。
13.[2017·宿迁]某兴趣小组在准备化学实验基本技能考试时,对以下问题进行了探究。Ⅰ.探究酸和碱能否发生反应方案1:甲同学向盛有少量NaOH溶液的试管中滴几滴无色酚酞试液,振荡,继续加入稀硫酸,观察到溶液由色变成无色。甲同学得出结论:酸和碱能发生反应。
方案2:乙同学取少量NaOH溶液,测得溶液pH为10,向该溶液中加入一定量稀硫酸后,测得溶液pH为9。乙同学发现溶液pH减小了,得出结论:酸和碱能发生反应。交流讨论:大家同意甲同学的结论,对乙同学的实验过程提出质疑,溶液pH减小的原因还可能是稀硫酸中的水稀释了NaOH溶液;大家认为,乙同学向NaOH溶液中加入稀硫酸后,测得溶液的pH必须(填“小于”或“小于或等于”)7才能证明酸和碱能发生反应。请写出稀硫酸和氢氧化钠溶液反应的化学方程式:。
[答案]Ⅰ.红 小于或等于2NaOH+H2SO42H2O+Na2SO4[解析]本题主要考查酸碱中和反应的实验探究方法。Ⅰ.方案1:NaOH溶液能使无色酚酞试液变红,加入稀硫酸,稀硫酸与氢氧化钠发生中和反应,酚酞在中性和酸性条件下呈无色,所以溶液会由红色变成无色。方案2:NaOH溶液的pH>7,稀硫酸的pH<7,所以NaOH溶液中加入稀硫酸后,二者反应,会使溶液的pH减小,如果溶液的pH小于或等于7就能证明酸和碱能发生反应。稀硫酸和氢氧化钠溶液反应生成硫酸钠和水,其化学方程式为2NaOH+H2SO42H2O+Na2SO4。
13.[2017·宿迁]某兴趣小组在准备化学实验基本技能考试时,对以下问题进行了探究。Ⅱ.探究酸和碱反应后溶液中溶质的成分丙同学对探究Ⅰ中甲同学实验后的无色溶液展开探究。[提出问题]试管中无色溶液的溶质除了酚酞还有什么?[提出猜想](1)Na2SO4;(2)Na2SO4和。
[答案]Ⅱ.[提出猜想]H2SO4(或硫酸)[解析]Ⅱ.[提出猜想]因为反应后溶液呈无色,所以反应后试管中的溶质中没有氢氧化钠;若二者恰好完全反应,溶质只有Na2SO4;如果H2SO4过量,则溶质为Na2SO4和H2SO4。
13.[2017·宿迁]某兴趣小组在准备化学实验基本技能考试时,对以下问题进行了探究。[设计实验]实验操作实验现象实验结论方案Ⅰ向试管中加入少量锌粒,然后加入甲同学实验后的无色溶液锌粒逐渐减少,有产生猜想(2)成立方案Ⅱ向试管中加入少量甲同学实验后的无色溶液,然后慢慢滴加NaOH溶液,并不断振荡试管开始无明显现象,过一会儿发现
[答案]Ⅱ.[设计实验]气泡溶液由无色变为红色[解析]Ⅱ.[设计实验]方案Ⅰ:如果猜想(2)成立,则锌粒与硫酸发生反应生成氢气,所以会看到锌粒逐渐减少,溶液中有气泡产生。方案Ⅱ:如果猜想(2)成立,则开始加入的NaOH溶液与溶液中的H2SO4反应,H2SO4被中和后再加入的NaOH溶液使无色酚酞变红。
13.[2017·宿迁]某兴趣小组在准备化学实验基本技能考试时,对以下问题进行了探究。[实验反思]为了验证猜想(2)成立,你认为还可以选择的药品是(填序号)。A.BaCl2溶液B.CuC.Fe2O3[答案]Ⅱ.[实验反思]C[解析]Ⅱ.[实验反思]为了验证猜想(2)成立,还可以选择只与稀硫酸反应产生明显现象的药品,BaCl2溶液能与H2SO4、Na2SO4反应生成硫酸钡沉淀;Cu不与H2SO4、Na2SO4反应,不能确定硫酸的存在;Fe2O3能和H2SO4反应生成硫酸铁,使溶液呈黄色,能确定硫酸是否存在。
相关文档
- 2019九年级化学全册 第二单元 常见2022-04-0111页
- 2020中考化学真题分类汇编 2考点132021-11-124页
- 2019年中考化学试题分类:考点13 溶2021-11-125页
- 九年级化学全册7-1溶液的酸碱性学2021-11-124页
- 溶液的酸碱性 教案2021-11-113页
- 江苏专版2020中考化学复习方案第一2021-11-115页
- 2019九年级化学全册 第二单元 常见2021-11-113页
- 2019年中考化学试题分类:考点13 溶2021-11-111页
- 2020中考化学真题分类汇编 2考点132021-11-111页
- 2019九年级化学全册 第二单元 常见2021-11-115页