- 215.00 KB
- 2021-11-11 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
单元复习(九) 溶液
01 知识框架
02 考情分析
近三年安徽中考主要以选择题的形式考查溶解度及溶解度曲线,且是每年的必考点,属于高频考点。考查的内容主要有:①溶解度大小的判断与比较;②溶解度随温度变化趋势的判断;③溶质质量分数的计算;④溶质质量分数大小的变化;⑤饱和溶液与不饱和溶液间的转化等。
03 单元精练
1.(2018·长沙)小军同学需要快速配制一杯可口的白糖溶液,下列措施不能达到目的的是(A)
A.用冰水溶解
B.用热水溶解
C.把白糖碾成粉末后再溶解
D.溶解时用筷子搅拌
2.向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是(D)
A.氢氧化钠
B.生石灰
C.浓硫酸
D.硝酸铵
4
3.(2017·长沙)下列说法错误的是(A)
A.饱和溶液一定是浓溶液
B.糖水、汽水都是溶液
C.洗洁精去油污是因为洗洁精具有乳化功能
D.溶液都是均一、稳定的混合物
4.(2017·潍坊改编)潍坊有丰富的海洋资源,氯化钠占整个海洋盐类的80%以上。下列有关氯化钠的说法正确的是(D)
A.室温下的氯化钠饱和溶液不能再溶解氯化钾
B.取出部分上层溶液,可将接近饱和的氯化钠溶液变为饱和
C.氯化钠是由氯化钠分子构成的
D.将100 g质量分数为20%的氯化钠溶液稀释为10%,所用的仪器有:烧杯、量筒、玻璃棒和胶头滴管
5.在“配制一定溶质质量分数的氯化钠溶液”实验中,下列操作正确的是(C)
A.甲图表示称取7.5 g氯化钠
B.乙图表示量取42.5 mL水
C.丙图表示溶解氯化钠
D.丁图表示向试剂瓶中转移溶液
6.现将40 ℃时的一杯硝酸钾溶液降温至20 ℃,结果有少量晶体析出,则下列说法不正确的是(A)
A.40 ℃时的溶液一定为饱和溶液
B.20 ℃时溶液中溶质的质量分数比40 ℃时的小
C.20 ℃时的溶液一定为饱和溶液
D.溶剂的质量没有改变
7.(2018·福建)某同学模拟闽籍化学家侯德榜的“侯氏制碱法”制纯碱,需用50.0 g水配制20 ℃的NaCl饱和溶液(20 ℃时NaCl的溶解度为36.0 g),应称取NaCl的质量为(A)
A.18.0 g B.16.0 g C.13.2 g D.11.5 g
8. (2017·安徽)地球深处的水处于超临界状态,称为超临界水,如图为某压强下CaCl2和NaCl在超临界水中的溶解度曲线,该压强下,下列说法正确的是(C)
A.在超临界水中,NaCl的溶解度大于CaCl2的溶解度
B.在超临界水中,两种物质的溶解度都随温度的升高而增大
C.450 ℃时,NaCl在超临界水中的溶解度为0.04 g
D.450 ℃时,可得到0.04%的CaCl2的超临界水溶液
9.(2017·宁波)下表是不同温度下KNO3的溶解度表。
温度(℃)
0
20
40
溶解度(g)
13.3
31.6
63.9
(1)称取30 g KNO3固体时,在加一定量的KNO3固体后,发现托盘天平指针偏右,接下来的操作是__继续加KNO3固体__,直到天平平衡。
(2)20 ℃时,将30 g KNO3固体加入到盛有100 g水的烧杯中,所得溶液是否饱和?__不饱和__。
(3)要使20 ℃的KNO3不饱和溶液变成饱和溶液,可采用__加入硝酸钾(或蒸发溶剂或降低温度)
4
__的方法。(写出一种即可)
10.(2017·南宁)水和溶液在生产、生活中有着重要的作用。
(1)生活中常用__煮沸__的方法降低水的硬度。
(2)下列物质在水中不能形成溶液的是__B__(填序号)。
A.白糖 B.汽油
C.食盐 D.高锰酸钾
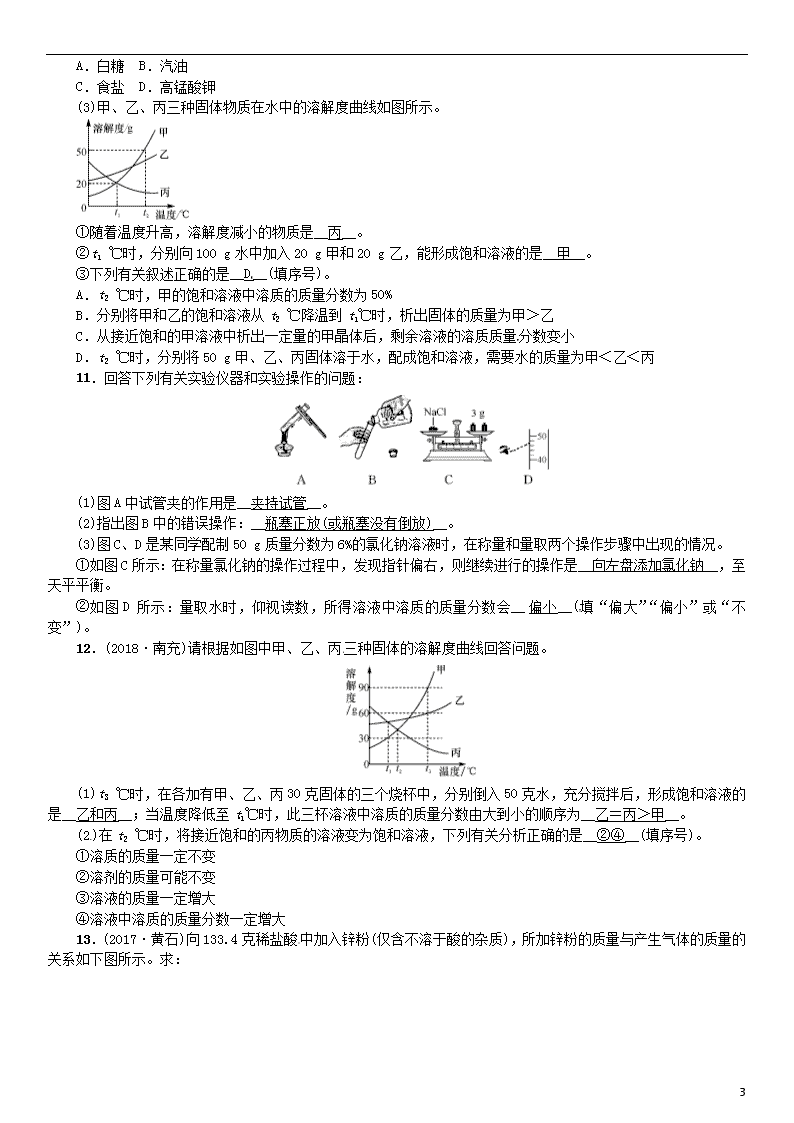
(3)甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。
①随着温度升高,溶解度减小的物质是__丙__。
②t1 ℃时,分别向100 g水中加入20 g甲和20 g乙,能形成饱和溶液的是__甲__。
③下列有关叙述正确的是__D__(填序号)。
A.t2 ℃时,甲的饱和溶液中溶质的质量分数为50%
B.分别将甲和乙的饱和溶液从t2 ℃降温到t1℃时,析出固体的质量为甲>乙
C.从接近饱和的甲溶液中析出一定量的甲晶体后,剩余溶液的溶质质量分数变小
D.t2 ℃时,分别将50 g甲、乙、丙固体溶于水,配成饱和溶液,需要水的质量为甲<乙<丙
11.回答下列有关实验仪器和实验操作的问题:
(1)图A中试管夹的作用是__夹持试管__。
(2)指出图B中的错误操作:__瓶塞正放(或瓶塞没有倒放)__。
(3)图C、D是某同学配制50 g质量分数为6%的氯化钠溶液时,在称量和量取两个操作步骤中出现的情况。
①如图C所示:在称量氯化钠的操作过程中,发现指针偏右,则继续进行的操作是__向左盘添加氯化钠__,至天平平衡。
②如图D所示:量取水时,仰视读数,所得溶液中溶质的质量分数会__偏小__(填“偏大”“偏小”或“不变”)。
12.(2018·南充)请根据如图中甲、乙、丙三种固体的溶解度曲线回答问题。
(1)t3 ℃时,在各加有甲、乙、丙30克固体的三个烧杯中,分别倒入50克水,充分搅拌后,形成饱和溶液的是__乙和丙__;当温度降低至t1℃时,此三杯溶液中溶质的质量分数由大到小的顺序为__乙=丙>甲__。
(2)在t2 ℃时,将接近饱和的丙物质的溶液变为饱和溶液,下列有关分析正确的是__②④__(填序号)。
①溶质的质量一定不变
②溶剂的质量可能不变
③溶液的质量一定增大
④溶液中溶质的质量分数一定增大
13.(2017·黄石)向133.4克稀盐酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如下图所示。求:
4
(1)此过程产生气体的最大质量是__0.4__g__;
(2)原稀盐酸中溶质的质量分数为多少?(请写出计算过程)
解:设原稀盐酸中溶质的质量分数为x。
Zn+2HCl===ZnCl2+H2↑
73 2
133.4 g×x 0.4 g
= x=10.9%
答:原稀盐酸中溶质的质量分数为10.9%。
4
相关文档
- 初中化学九年级上册第六单元碳和碳2021-11-1119页
- 初中数学中考复习课件章节考点专题2021-11-1119页
- 2018年河北省初中毕业生升学文化课2021-11-118页
- 人教版初中语文9年级上册:第6单元 2021-11-1110页
- 初中物理中考复习单元复习课件:第十2021-11-1122页
- 2020届初中生物中考一轮复习考点测2021-11-116页
- 初中语文PPT教学课件:10 孤独之旅(人2021-11-1134页
- 初中历史学业水平考试模拟卷(三)(及答2021-11-1122页
- 2020届初中物理章节复习 第16章 电2021-11-1133页
- 初中物理单元复习课件中考物理复习2021-11-1167页