- 322.50 KB
- 2021-11-12 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
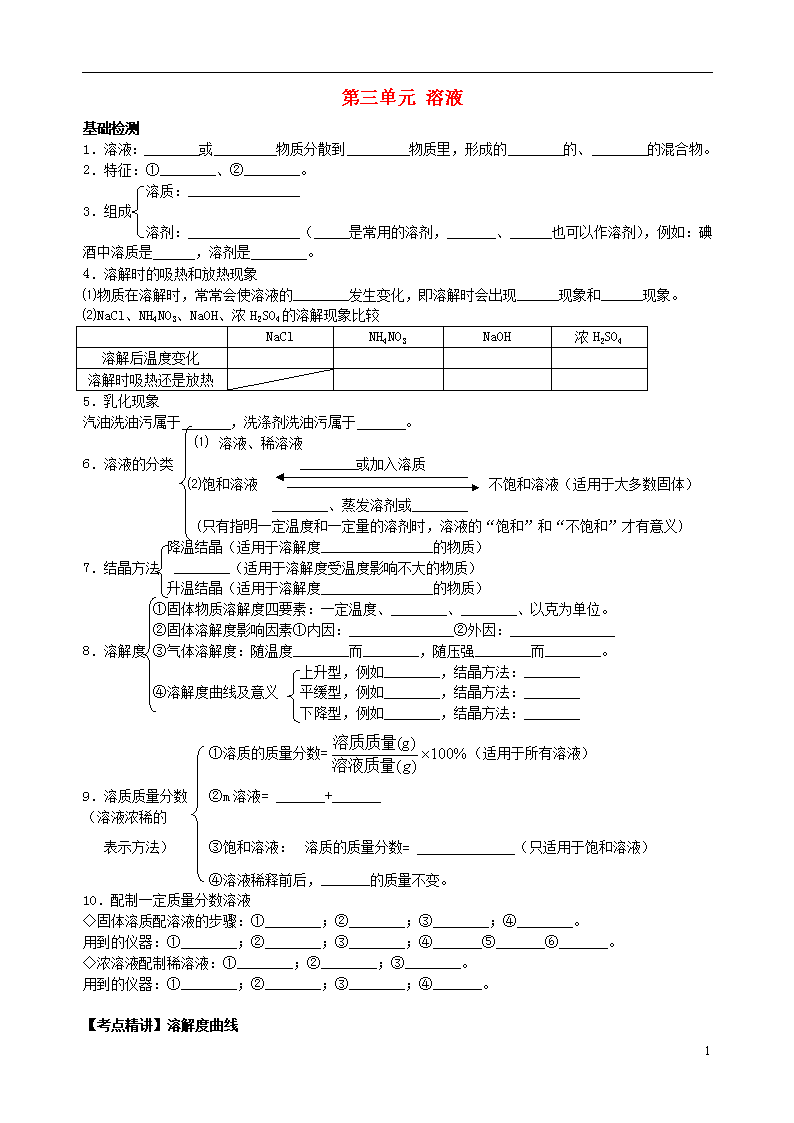
第三单元 溶液
基础检测
1.溶液:________或_________物质分散到_________物质里,形成的________的、________的混合物。
2.特征:①________、②________。
溶质:________________
3.组成
溶剂:________________(_____是常用的溶剂,_______、______也可以作溶剂),例如:碘酒中溶质是______,溶剂是________。
4.溶解时的吸热和放热现象
⑴物质在溶解时,常常会使溶液的________发生变化,即溶解时会出现______现象和______现象。
⑵NaCl、NH4NO3、NaOH、浓H2SO4的溶解现象比较
NaCl
NH4NO3
NaOH
浓H2SO4
溶解后温度变化
溶解时吸热还是放热
5.乳化现象
汽油洗油污属于 ,洗涤剂洗油污属于 。
⑴ 溶液、稀溶液
6.溶液的分类 ________或加入溶质
⑵饱和溶液 不饱和溶液(适用于大多数固体)
________、蒸发溶剂或________
(只有指明一定温度和一定量的溶剂时,溶液的“饱和”和“不饱和”才有意义)
降温结晶(适用于溶解度________________的物质)
7.结晶方法 ________(适用于溶解度受温度影响不大的物质)
升温结晶(适用于溶解度________________的物质)
①固体物质溶解度四要素:一定温度、________、________、以克为单位。
②固体溶解度影响因素①内因:_______________②外因:_______________
8.溶解度 ③气体溶解度:随温度________而________,随压强________而________。
上升型,例如________,结晶方法:________
④溶解度曲线及意义 平缓型,例如________,结晶方法:________
下降型,例如________,结晶方法:________
①溶质的质量分数=(适用于所有溶液)
9.溶质质量分数 ②m溶液= _______+_______
(溶液浓稀的
表示方法) ③饱和溶液:溶质的质量分数= ______________(只适用于饱和溶液)
④溶液稀释前后,_______的质量不变。
10.配制一定质量分数溶液
◇固体溶质配溶液的步骤:①________;②________;③________;④________。
用到的仪器:①________;②________;③________;④_______⑤_______⑥_______。
◇浓溶液配制稀溶液:①________;②________;③________。
用到的仪器:①________;②________;③________;④_______。
【考点精讲】溶解度曲线
4
I
Ⅱ
典型例题
⑴确定某物质在某一温度下的溶解度
如图Ⅱ,t3℃时,A的溶解度为_______g,将27gA溶于50g水中,则所得到的溶液为_______(填“饱和”或“不饱和”)。
⑵比较同一温度下,不同物质溶解度得大小。(如图Ⅱ)
在t1℃时,A的溶解度______(填“大于”“小于”或“等于”)。(比较两种物质的溶解度大小时,必须指明温度,否则没有意义。
⑶饱和溶液与不饱和溶液的转化。(如图Ⅰ)
①____________、____________、____________能使接近饱和的a(或b)溶液变为饱和溶液。
②____________、____________、____________能使接近饱和的c溶液变为饱和溶液。
⑷判断溶质质量分数。
图Ⅰ中:①a、b、c三种物质t1℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数的大小顺序:________________________。
②a、b、c三种物质t2℃时的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小顺序:________________________。
⑸根据几种物质的溶解度曲线的变化趋势,确定混合物的分离方法。如图Ⅰ中:
①如果a中混有少量的b,可采用_________法进行分离。
②如果b中混有少量的a,可采用_________法进行分离(留少量水,这时少量的a仍留在溶液中,趁热过滤可得到b).
⑹判断一定质量饱和溶液中所含溶质的质量。如图Ⅱ,t3℃时100gA的饱和溶液中所含溶质的质量为______g。
解题方法:利用饱和溶液的质量分数关系:
⑺根据溶解度曲线判断溶质的质量分数。如如图Ⅱ,t3℃时150g水中加入70gB物质,形成溶液的溶质质量分数为____________。
1.右图为甲、乙两种固体物质在水中的溶解度曲线,下列说法正确的是( )
A.降温或蒸发均可使乙物质从其饱和溶液中结晶出来
B.N点和M点表示的甲的溶液中溶质的质量分数相等
C.甲、乙饱和溶液从t1℃升温至.t2℃,其浓度均保持不变
D.t1℃时,甲、乙饱和溶液中溶质和溶液的质量比均为1︰3
中考真题演练
4
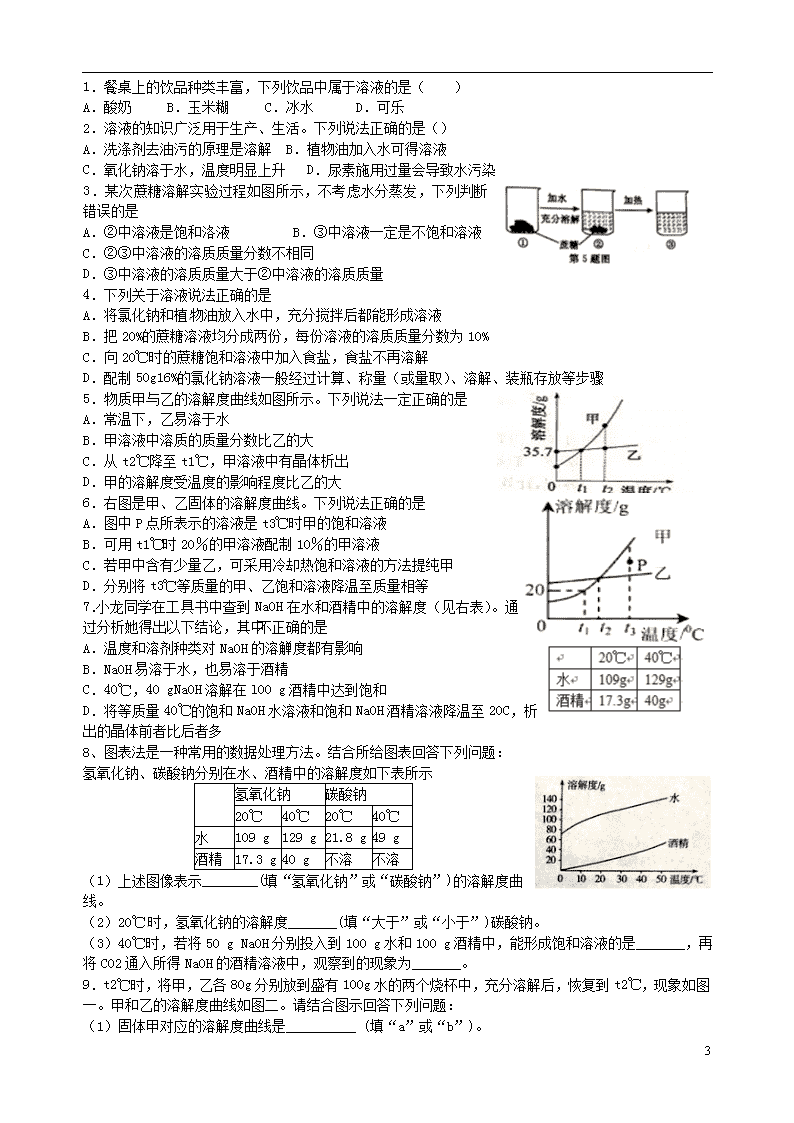
1.餐桌上的饮品种类丰富,下列饮品中属于溶液的是( )
A.酸奶 B.玉米糊 C.冰水 D.可乐
2.溶液的知识广泛用于生产、生活。下列说法正确的是()
A.洗涤剂去油污的原理是溶解 B.植物油加入水可得溶液
C.氧化钠溶于水,温度明显上升 D.尿素施用过量会导致水污染
3.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是
A.②中溶液是饱和洛液 B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
4.下列关于溶液说法正确的是
A.将氯化钠和植物油放入水中,充分搅拌后都能形成溶液
B.把20%的蔗糖溶液均分成两份,每份溶液的溶质质量分数为10%
C.向20℃时的蔗糖饱和溶液中加入食盐,食盐不再溶解
D.配制50g16%的氯化钠溶液一般经过计算、称量(或量取)、溶解、装瓶存放等步骤
5.物质甲与乙的溶解度曲线如图所示。下列说法一定正确的是
A.常温下,乙易溶于水
B.甲溶液中溶质的质量分数比乙的大
C.从t2℃降至t1℃,甲溶液中有晶体析出
D.甲的溶解度受温度的影响程度比乙的大
6.右图是甲、乙固体的溶解度曲线。下列说法正确的是
A.图中P点所表示的溶液是t3℃时甲的饱和溶液
B.可用t1℃时20%的甲溶液配制10%的甲溶液
C.若甲中含有少量乙,可采用冷却热饱和溶液的方法提纯甲
D.分别将t3℃等质量的甲、乙饱和溶液降温至质量相等
7.小龙同学在工具书中查到NaOH在水和酒精中的溶解度(见右表)。通过分析她得出以下结论,其中不正确的是
A.温度和溶剂种类对NaOH的溶觯度都有影响
B.NaOH易溶于水,也易溶于酒精
C.40℃,40 gNaOH溶解在l00 g酒精中达到饱和
D.将等质量40℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20C,析出的晶体前者比后者多
8、图表法是一种常用的数据处理方法。结合所给图表回答下列问题:
氢氧化钠、碳酸钠分别在水、酒精中的溶解度如下表所示
氢氧化钠
碳酸钠
20℃
40℃
20℃
40℃
水
109 g
129 g
21.8 g
49 g
酒精
17.3 g
40 g
不溶
不溶
(1)上述图像表示________(填“氢氧化钠”或“碳酸钠”)的溶解度曲线。
(2)20℃时,氢氧化钠的溶解度_______(填“大于”或“小于”)碳酸钠。
(3)40℃时,若将50 g NaOH分别投入到100 g水和100 g酒精中,能形成饱和溶液的是_______,再将CO2通入所得NaOH的酒精溶液中,观察到的现象为_______。
9.t2℃时,将甲,乙各80g分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答下列问题:
(1)固体甲对应的溶解度曲线是__________ (填“a”或“b”)。
4
(2)M点的含义______________。
(3)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出.你认为“全部溶解”的原因是________________。
(4)将t2℃等质量的甲、乙饱和溶液分别降温到们将t1℃时,所得溶液的有关说法正确的是___________(填字母)。
a.甲溶液仍为饱和溶液 b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙 d.两溶液溶质质量甲>乙
10.R是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示.某化学兴趣小组的同学进行了如图2所示实验。
(1)t1℃时,氯化铵的济解度为______g。
(2)①的溶液中溶质质量分数为____________。
(3)根据以上信息可推出R是________(写名称或化学式均可)。
(4)关于图2中烧杯内的物质,以下几种说法正确的有_________。
A.①、②、③中,只有③中上层清液是饱和溶液
B.若使③中的固体溶解,可采用加水或升温的方法
C.①和②的溶液中,溶质质量相等
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小。
11.某同学配制50g6%氯化钠溶液,整个操作过程如下图所示,回答下列问题:
(1)配制溶液的正确操作顺序为_______(填序号,下同),其中操作错误的是________。
(2)图② 中盛放氯化钠固体的仪器名称是 ______,需称取氯化钠 _______g。
(3)量水时选用的量筒的量程最合适的是______(填序号),读数时视线要与量筒内______保持水平。
A.10 ml B.25 ml C.50ml D.100ml
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是_______(填序号)。
A.氯化钠固体不纯 B.用生锈砝码称量
C.装瓶时有少量溶液洒出 D.溶解时烧杯内壁有水珠
4
相关文档
- 2020九年级化学下册溶液的形成2021-11-123页
- 溶液组成的表示2 教案2021-11-123页
- 2020年化学精品教学课件9单元 实验2021-11-1210页
- 2020-2021学年初中化学鲁教版(新)九2021-11-124页
- 人教版九年级化学下册第9单元课题32021-11-1223页
- 九年级化学下册第九单元溶液课题32021-11-125页
- 2020中考化学真题分类汇编 2考点132021-11-124页
- 中考年化学考点跟踪:第26讲 专题五2021-11-125页
- (第一辑)第9单元 溶液2021-11-1227页
- 徐州专版2020中考化学复习方案第62021-11-126页