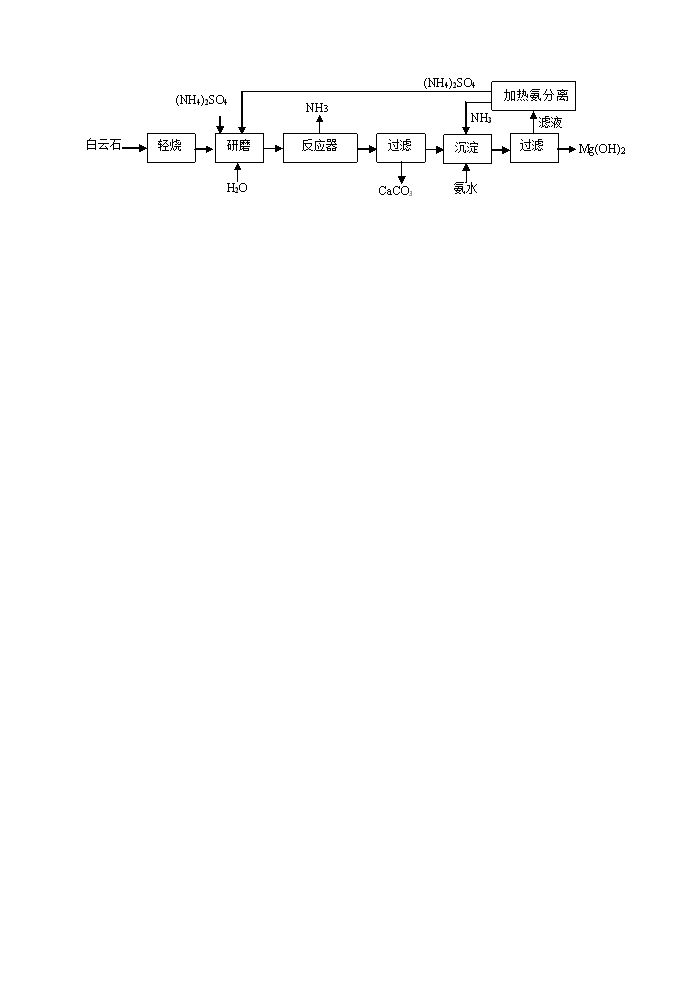- 194.00 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2018无锡市中考化学一模17题专项训练
17-1(6分)现代循环经济要求综合考虑环境污染和经济效益。高纯氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:提示:(NH4)2CO3溶液呈碱性,40 ℃以上时(NH4)2CO3分解
(1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器有玻璃棒、烧杯、 等。
(2)滤液Ⅰ中主要的溶质是 。
(3)加适量氨水的目的是 。
(4)根据题中信息,加入(NH4)2CO3后,该反应必须控制的条件是 。
(5)滤液Ⅱ中可回收的产品是 (写化学式)。
(6)写出在空气中煅烧FeCO3的化学反应方程式 。
17-2(6分)硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;铜离子完全沉淀
的pH是5左右,铁离子完全沉淀的pH是2左右。以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:
胆矾和石膏在不同温度下的溶解度(g/100g水)如表。
温度(℃)
20
40
60
80
100
石膏
0.32
0.26
0.15
0.11
0.07
胆矾
32
44.6
61.8
83.8
114[来源:学§科§网Z§X§X§K]
请回答下列问题:
(1)红褐色滤渣的主要成分是 ;
(2)铜和稀硝酸反应的化学方程式3Cu+8HNO3= +2NO↑+4H2O;
(3)石灰浆调pH大约要调节到___________
A. 2 B. 5 C. 7 D. 10
(4)操作I最后温度应该控制在 ℃左右;
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、 、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是 。
17-3(5分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。以孔雀石为原料可制备CuSO4 • 5H2O及纳米材料CaCO3,步骤如下:
请回答下列问题:
⑴写出Cu2(OH)2CO3与稀硫酸反应的化学方程式: 。
⑵操作Ⅱ的名称为 。
⑶由CuSO4溶液获得CuSO4•5H2O,需要经过蒸发浓缩、 、过滤、洗涤、
干燥等操作。在实验室进行“蒸发浓缩”时,除铁架台、蒸发皿、酒精灯外,还用到另 一玻璃仪器,该仪器是 。
⑷制备纳米材料CaCO3时,应向CaCl2溶液中先通入NH3,后通入CO2。请写出该反
应的化学方程式: 。
17-4(5 分)以白云石(主要成分为 MgCO3·CaCO3)为原料制备氢氧化镁的流程如下:
(NH4)2SO4
NH3
(NH4)2SO4
NH3
加热氨分离 滤液
白云石 轻烧 研磨 反应器 过滤
沉淀 过滤
Mg(OH)2
H2O
CaCO3 氨水
已知:MgCO3 MgO + CO2↑;CaCO3 CaO + CO2↑。
请回答下列问题:
(1)“研磨”的目的是 ,实验室“过滤”操作中玻璃棒的作用是 。
(2)根据流程,“轻烧”温度不应超过 ℃,“轻烧”后的固体主要成份是 。
(3)该流程中可循环使用的物质是 。
17-5(5分)(2017·南通改编)实验室以MnO2为原料制备少量高纯MnCO3的流程如下:
已知:①反应Ⅰ的化学方程式:MnO2+SO2=MnSO4
②MnCO3、Mn(OH)2均难溶于水,MnCO3在100℃时开始分解。
(1)流程中“操作”所需要的主要玻璃仪器有漏斗、玻璃棒和 。
(2)反应Ⅱ的化学方程式为 。
反应Ⅱ需控制溶液的酸碱度,若碱性过强,MnCO3粗产品中将混有 (填化学式)。
(3)检验MnCO3粗产品洗涤干净的方法是: 。
(4)为获得高纯MnCO3,需选择“低温”干燥的原因是 。
17-6.(5分)废旧碱性锌锰干电池内部的黑色物质A主要含有MnO2、NH4Cl、ZnCl2,还有少量的FeCl2和炭粉,用A制备高纯MnCO3的流程图如下。
(1) 第I步操作得滤渣的成分是 ;第Ⅱ步操作的目的是 。
(2) 步骤Ⅲ中制得MnSO4,反应的化学方程式为MnO2+H2O2+H2SO4= MnSO4+O2+2X;则X
的化学式为 。
(3) 已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,l00℃时开始分解;Mn(OH)2
开始沉淀时pH为7.7。
第V步系列操作可按以下步骤进行:
操作l:加入试剂 ,控制pH<7.7;
操作2:过滤,用少量水洗涤2-3次; 操作3:检测滤液;
操作4:用少量 洗涤2-3次; 操作5:低温烘干。