- 381.02 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2019化学中考模拟试题
可能用到的相对原子质量: H-1 O-16 Na-23 S-32 Cl-35.5 Fe-56 Cu-64 Ag-108
11. 日前,海安正在争创“全国文明城市”,下列做法与创建文明城市不相符的是 ( )
A.大量使用农药化肥,提高粮食产量 B.加强水体污染治理,保护水资源
C.加大空气质量检测,改善环境状况 D.分类回收生活垃圾,垃圾资源化
12. 下列对燃烧现象的描述中正确的是 ( )
A.镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色的氧化镁固体
B.硫在空气中燃烧,产生明亮的蓝紫色火焰,并生成无色有刺激性气味的气体
C.铁在氧气中燃烧,火星四射,生成黑色固体
D.红磷在空气中燃烧产生大量的白色烟雾
13. 下列涉及学科观点的有关说法正确的是 ( )
A.微粒观:和两个粒子最外层电子数相同,化学性质相似
B.转化观:二氧化碳和氧气在一定条件下能可以相互转化
C.能量观:硝酸铵固体溶于水放出热量,天然气燃烧吸收热量
D.结构观:金刚石和石墨物理性质存在较大差异是由于碳原子的结构不同
14. 下列实验操作正确的是
A B C D
15.下列排序正确的是 ( )
A.空气中物质含量: B.溶液pH:
C.金属活动性顺序: D.硫元素质量分数:
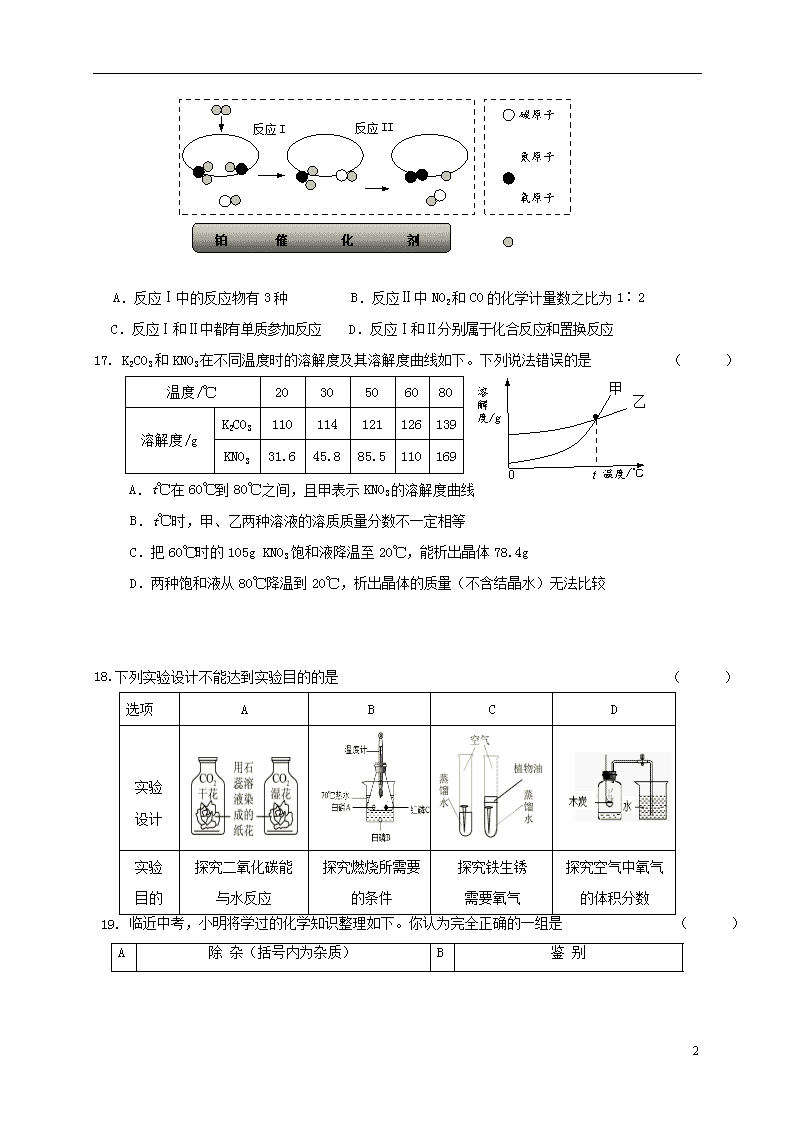
16. 汽车尾气净化装置中装有铂催化剂,尾气在催化剂表面反应的微观过程可用下图表示。下列有关说法正确的是 ( )
8
反应I
反应II
碳原子
氮原子
氧原子
铂 催 化 剂
A.反应Ⅰ中的反应物有3种 B.反应Ⅱ中NO2和CO的化学计量数之比为1∶2
C.反应Ⅰ和Ⅱ中都有单质参加反应 D.反应Ⅰ和Ⅱ分别属于化合反应和置换反应
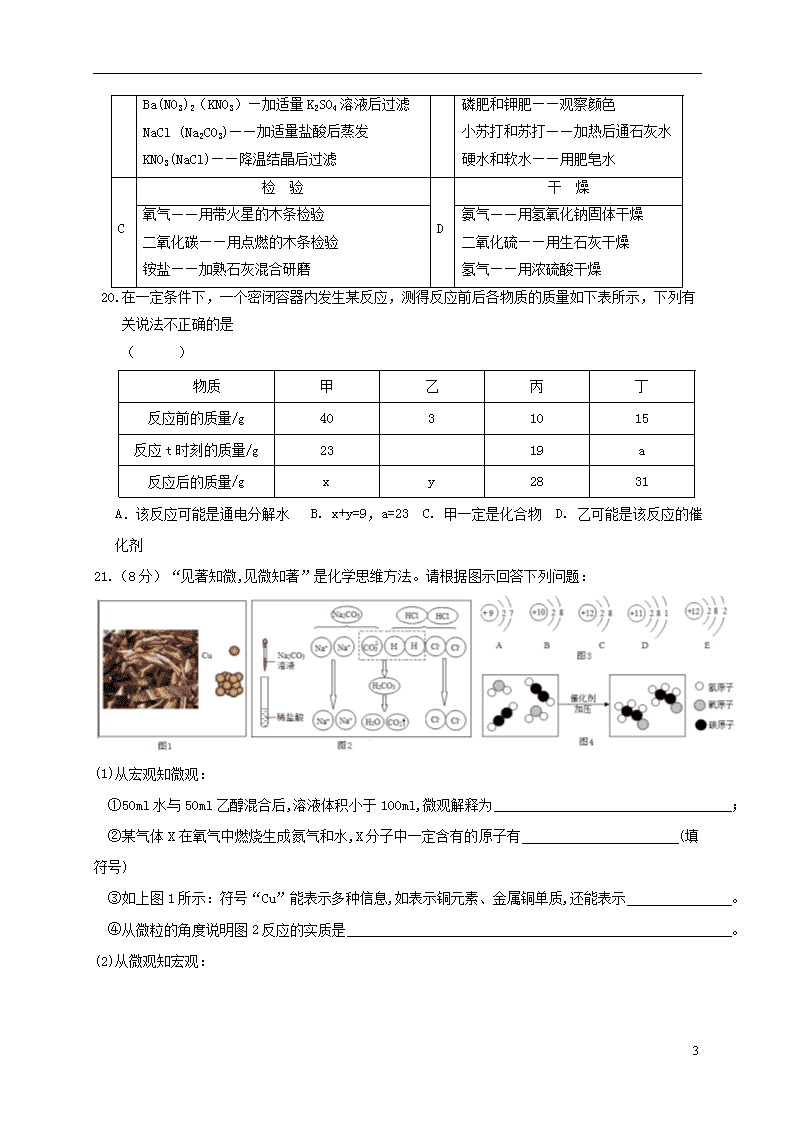
17. K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下。下列说法错误的是 ( )
温度/℃
20
30
50
60
甲
溶
解
度/g
0 t 温度/℃
•
乙
80
溶解度/g
K2CO3
110
114
121
126
139
KNO3
31.6
45.8
85.5
110
169
A.t℃在60℃到80℃之间,且甲表示KNO3的溶解度曲线
B.t℃时,甲、乙两种溶液的溶质质量分数不一定相等
C.把60℃时的105g KNO3饱和液降温至20℃,能析出晶体78.4g
D.两种饱和液从80℃降温到20℃,析出晶体的质量(不含结晶水)无法比较
18.下列实验设计不能达到实验目的的是 ( )
选项
A
B
C
D
实验
设计
实验
目的
探究二氧化碳能与水反应
探究燃烧所需要的条件
探究铁生锈
需要氧气
探究空气中氧气的体积分数
19. 临近中考,小明将学过的化学知识整理如下。你认为完全正确的一组是 ( )
A
除 杂(括号内为杂质)
B
鉴 别
8
Ba(NO3)2(KNO3)—加适量K2SO4溶液后过滤
NaCl (Na2CO3)——加适量盐酸后蒸发
KNO3(NaCl)——降温结晶后过滤
磷肥和钾肥——观察颜色
小苏打和苏打——加热后通石灰水
硬水和软水——用肥皂水
C
检 验
D
干 燥
氧气——用带火星的木条检验
二氧化碳——用点燃的木条检验
铵盐——加熟石灰混合研磨
氨气——用氢氧化钠固体干燥
二氧化硫——用生石灰干燥
氢气——用浓硫酸干燥
20.在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示,下列有关说法不正确的是 ( )
物质
甲
乙
丙
丁
反应前的质量/g
40
3
10
15
反应t时刻的质量/g
23
19
a
反应后的质量/g
x
y
28
31
A.该反应可能是通电分解水 B. x+y=9,a=23 C. 甲一定是化合物 D. 乙可能是该反应的催化剂
21.(8分)“见著知微,见微知著”是化学思维方法。请根据图示回答下列问题:
(1)从宏观知微观:
①50ml水与50ml乙醇混合后,溶液体积小于100ml,微观解释为 ;
②某气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子有 (填符号)
③如上图1所示:符号“Cu”能表示多种信息,如表示铜元素、金属铜单质,还能表示 。
④从微粒的角度说明图2反应的实质是 。
(2)从微观知宏观:
8
①如图2,微粒A、B、C、D、E中,对应单质化学性质最稳定的是 (填化学式),属于同种元素的是 (填编号),C在元素周期表位于第 周期。
②图4为某化学反应的微观示意图,则该反应的反应的化学方程式为 。
22.(7分)硬水受热后会产生水垢,水垢的主要成分是 CaCO3 和 Mg(OH)2。实验室由水垢制取纯净 CaCl2 固体的流程如下:(水垢中其它成分不参与反应),请按要求填空:
⑴ 试剂 A 的名称为 。
⑵ 试剂 B 的化学式是 ,若加入的试剂A、B都是过量的,则 加入试剂 B 发生的非中和反应的化学反应方程式是 。操作Ⅰ的名称是 ,该操作中除用到玻璃仪器外,还需要的实验用品有 。
⑶ 酸化过程加试剂 A 的作用 。
⑷“操作Ⅱ”包含的操作有:蒸发浓缩、 、过滤、洗涤、干燥等。
23.(9分)请用化学知识解释下列问题。
⑴电视中的化学:《奔跑吧,兄弟!》是一档热播的娱乐节目,其中蕴含着许多化学知识。
①节目中最刺激的游戏是“撕名牌”,“名牌”是贴在队员衣服后面,标有自己姓名的标牌,制作材料有棉布、涤纶等,鉴别棉布和涤纶的方法是___ __。
②其中一期节目,队员用水枪将酚酞溶液喷射到对方的“名牌”上,立即变红色,“名牌”可能预先用下列___ __溶液(填编号)浸泡过。
8
A.白酒 B.柠檬酸 C.食盐溶液 D.纯碱溶液
③另一期节目,蓝色的“污水”中注入“神秘水”后立即变得澄清透明,“污水”是单宁酸和硫酸亚铁溶液混合后发生一系列化学反应形成的,加入无色的“神秘水”草酸(H2C2O4)后,污水变澄清,其中一个反应为:2C76H49O46Fe+H2C2O4===2C76H50O46Fe+2X,则X的化学式为____ _,“Fe”是人体必需的一种 (填“微量”或“常量”)元素。
⑵生活中的化学:化学与生活息息相关,生活中也蕴含着许多化学知识。
①喝了冰冷的汽水后常常会打嗝,原因是 ;用洗涤剂除去油污的原理是洗涤剂能将油脂 。
②小明一家经常使用“共享汽车”出行。“共享汽车”中属于复合材料的是
(填材料名称);制造“共享汽车”往往需要较多的镁铝合金,该合金的优点是 (写1点即可);使用“共享汽车”出行的好处有 (填标号)
a.降低出行成本 b.减少汽车尾气排放 c.节约能源 d.缓解交通压力
24.(12分)Ⅰ.请结合下图回答问题。
(1)写出图中有标号仪器的名称: ① 。
(2)用高锰酸钾制取一瓶干燥的氧气,可选用装置组合为 (选填序号);实验室制取二氧化碳和氧气可选用发生装置C或B,C装置的优点是 ,用此装置制取O2的化学方程式是_ ;
(3)实验室常用甲酸(HCOOH)溶液滴加到浓硫酸中制CO气体,可选用的制取装置是 (选填序号)。该反应中浓硫酸既是催化剂又是脱水剂,试写出该反应的化学方程式_ 。
8
Ⅱ.某同学将氢氧化钠溶液滴入到一定量的稀氯化铜溶液中,出现蓝绿色不溶于水的固体。该同学对生成蓝绿色而不是蓝色固体的现象产生疑惑。
【查阅资料】
1.CuCl2溶液与NaOH溶液反应可生成蓝色固体【Cu(OH)2】,在氢氧化钠较少的情况下会生成蓝绿色碱式氯化铜【Cux(OH)yClz】,其不溶于水,能与酸反应。
2.Cu(OH) 2在60℃开始分解生成两种氧化物,100℃分解完全。碱式氯化铜在300℃开始分解生成氧化铜、水和氯化氢,在400℃分解完全。
【猜想】蓝绿色固体可能是:①Cu(OH)2;②Cux(OH)yClz晶体;③ 。
猜想①的理由是: (用化学方程式表示)。
【验证】该同学取31.25g蓝绿色固体,加热至100℃出现黑色固体。则猜想 不正确。继续加
甲 乙
浓硫酸
浓AgNO3溶液
气体
浓硫酸
浓AgNO3溶液
气体
热到400℃至质量不再改变,并使产生的气体全部缓缓通过如图 (选填“甲”或“乙”)装置(装置中药品足量)。
【实验数据】 ①最终得到剩余固体24.00g;
②与硝酸银溶液反应得到的沉淀经过滤、洗涤和低温烘干,得到固体14.35g;
加热前
100℃
400℃
250.00g
251.80g
253.60g
③浓硫酸装置中数据如右表。
【得出结论】猜想③成立,且碱式氯化铜中X∶Y:Z = 。
【拓展延伸】
为使实验中生成蓝色固体,少出现蓝绿色固体,应作 改进(选填序号)。
a.实验中将氯化铜溶液滴加到氢氧化钠溶液中
b.实验中应提供足量、较浓的氢氧化钠溶液
c.实验应该在80℃的水浴中进行
25.(5分)某化学兴趣小组的同学对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。他们称取了13.6g固体样品,用下图所示的装置继续实验,完全反应后,测定的有关数据如下表所示。
8
A中固体
的质量
澄清石灰水
的质量
反应前
13.6g
102.5g
反应后
11.2g
108.0g
请计算:
⑴实验中先通CO的目的是 。
⑵从上表中选择合适的数据,计算固体样品中氧化铁的质量是___ __克。
⑶在上述反应后的固体中加入100g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数。(请写出完整计算过程,结果精确到0.1%)
2019化学中考模拟试题参考答案
题号
11
12
13
14
15
16
17
18
19
20
答案
A
C
B
D
D
B
C
D
B
A
21.⑴①分子间有间隔 ②N、H ③一个铜原子 ④氢离子与碳酸根离子结合生成水和二氧化碳
⑵①Ne CE 三 ②C2H2+H2OC2H4O
22.⑴盐酸(或氯化氢溶液)
⑵Ca(OH)2 Ca(OH)2 + MgCl2 === Mg(OH)2↓+ CaCl2 过滤 铁架台(带铁圈)和滤纸
⑶除去过量的Ca(OH)2(或除去OH-)
⑷降温结晶
23.⑴①点燃后,闻气味(或观察灰烬或观察点燃时是否卷缩) ②D ③CO2 微量
⑵①气体的溶解度随温度的升高而减小 乳化
②玻璃钢 硬度大、抗腐蚀性强 abcd
24.Ⅰ.⑴分液漏斗
⑵AE 能控制反应的发生和停止(或随开随用,随关随停) 2H2O2====2H2O+O2↑
⑶BD HCOOH ====== H2O+CO↑
Ⅱ.【猜想】③Cux(OH)yClz与Cu(OH)2的混合物 CuCl2 +2NaOH=Cu(OH)2 ↓+2 NaCl
【验证】② 甲
8
【得出结论】X︰Y:Z= 2︰3:1
【拓展延伸】 a b(少写、多写、错写不给分)
25.⑴除去装置内的空气,防止加热时引起爆炸
⑵8 分析:因为少量澄清石灰水不能将生成的二氧化碳完全吸收,所以应该选择A中固体的质量变化进行计算,固体减少的质量为13.6g-11.2g=2.4g,即为氧化铁中氧元素的质量,
设氧化铁的质量为x,则
,解得x=8g
⑶设生成的FeCl2和H2质量分别为y、z,
Fe + 2HCl === FeCl2 + H2↑
56 127 2
11.2g y z
,解得y=25.4g ,z=0.4g
则反应后的溶液中溶质的质量分数为
(注:1.本卷除选择题每题2分和25题(3)为2分外,其余每空1分;2.合理答案均可酌情给分)
8