- 253.50 KB
- 2021-05-11 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第六~七单元测试卷
(测试时间:90分钟 满分:100分)
一、选择题(16×2分=32分)
1.(2016,连云港)今年4月22是第47个世界地球日,主题是“节约利用资源,倡导绿色简约生活”。下列做法不应该提倡的是(C)
A.少开私家车多步行
B.对废旧金属进行回收利用
C.经常使用一次性筷子、塑料袋等
D.开发太阳能、风能等,减少对化石能源的依赖
2.单层石墨称为石墨烯,这种“只有一个碳原子厚的碳薄片”被认为是目前世界上最薄、最坚硬、传导电子速度最快的新型材料,下列关于石墨烯的叙述中正确的是(B)
A.石墨烯属于化合物 B.石墨烯的化学式为C
C.石墨烯中碳元素化合价为+4 D.石墨烯的硬度小于金刚石
3.下列关于碳单质用途的叙述,错误的是(B)
A.用焦炭冶炼生铁 B.用碳粉和铅制成铅笔芯
C.用石墨做干电池的电极 D.用木炭粒做自制净水器的吸附剂
4.(2015,长沙)下列关于碳及其氧化物的说法中,正确的是(C)
A.金刚石、石墨都是碳的单质,其硬度都很大
B.CO2可用作燃料
C.CO有还原性,可用作冶炼金属
D.CO2通入紫色石蕊溶液,溶液变红,加热后溶液颜色不变
5.(2016,自贡)酒精灯的火焰太小时,将灯芯拨弄得松散些,可使火焰更旺。其原理主要是(B)
A.降低可燃物的着火点
B.增大可燃物与空气的接触面积
C.提高可燃物的着火点
D.增大空气中氧气的含量
6.有关二氧化碳的实验中,不能达到实验目的的是(C)
A.用向上排空气法收集一瓶CO2,观察CO2的颜色为无色
B.将CO2通入紫色石蕊试液中,证明CO2能与水反应,得到的溶液显酸性
C.将燃着的木条伸入集气瓶中,检验CO2是否收集满
D.将CO2通入澄清石灰水中,可看到白色沉淀产生
7.(2015,陕西)下列进行中的实验现象或实验原理正确的是(C)
8.(2016,青岛)采取正确的措施,能够避免火灾发生或减少灾害损失。下列灭火方法不恰当的是(D)
A.油锅起火——用锅盖盖灭
B.酒精灯着火——用湿抹布盖灭
C.森林起火——砍伐树木形成隔离带
D.汽车油箱着火——用水浇灭
9.(2016,重庆)目前,许多烧烤店都改用机制炭作燃料,引燃机制炭可以使用固体酒精,盖灭机制炭可以使用炭灰。下列有关说法错误的是(C)
A.酒精的燃烧是为了升高温度
B.炭灰可以隔绝空气而使机制炭熄灭
C.酒精的燃烧会升高机制炭的着火点
D.机制炭做成空心可以增大与空气的接触面积
10.(2016,十堰)关于燃料及其利用的相关知识叙述中错误的是(C)
A.可燃性气体点燃前一定要验纯
B.将煤粉制成蜂窝煤,能增大与空气的接触面积
C.堆放杂物的纸箱着火用水浇灭,降低了可燃物的着火点
D.食物的腐烂、动植物的呼吸都属于缓慢氧化
11.(2016,常德)下列关于自然界中碳循环和氧循环的说法中正确的是(D)
A.植物的光合作用使空气中的氧气含量逐年提升
B.动植物的呼吸作用使空气中的二氧化碳含量逐年增大
C.积极倡导“低碳”行动的目的是消除大气温室效应
D.大气中的氧气含量在各种因素作用下能保持相对稳定
12.下图为初中化学常见气体的发生与收集装置。有关这些装置的说法不正确的是(D)
A.装置Ⅰ可作为固体加热制取气体的发生装置
B.装置Ⅱ中长颈漏斗可以用分液漏斗、医用注射器代替
C.装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,且不与空气中各成分反应的气体
D.装置Ⅴ可以用于收集H2、O2,也可以用于实验室收集CO2
13.(2015,益阳)2015年5月25日,沅江市某纸厂芦苇仓库发生火灾,造成重大的经济损失。某同学给纸厂提供如下温馨提示,你认为错误的是(A)
A.芦苇着火时,只能用沙子灭火
B.芦苇仓库外要有明显的防火警示标志
C.芦苇仓库与周围建筑物之间要留有足够的防火距离
D.芦苇仓库要有良好的通风设备、齐备的消防器材
14.(2015,贵港)今年5月12日是我国第七个“防灾减灾日”。下列做法不合理的是(C)
A.扑灭森林火灾,可将大火蔓延路线前的一片树木砍掉,形成隔离带
B.室内电器着火,先切断电源,再用灭火器灭火
C.把燃气热水器安装在浴室内
D.油库、面粉加工厂、纺织厂等场所要严禁烟火
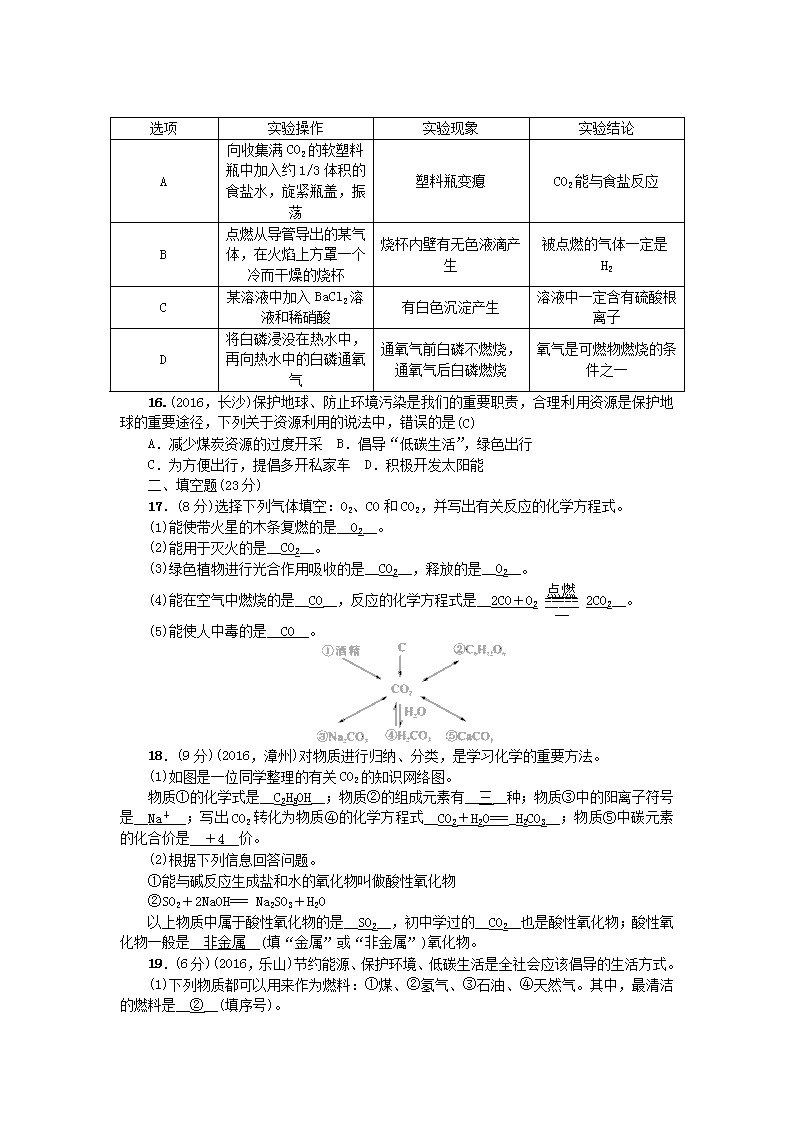
15.(2015,雅安)通过下列实验操作和现象能得出相应结论的是(D)
选项
实验操作
实验现象
实验结论
A
向收集满CO2的软塑料瓶中加入约1/3体积的食盐水,旋紧瓶盖,振荡
塑料瓶变瘪
CO2能与食盐反应
B
点燃从导管导出的某气体,在火焰上方罩一个冷而干燥的烧杯
烧杯内壁有无色液滴产生
被点燃的气体一定是H2
C
某溶液中加入BaCl2溶液和稀硝酸
有白色沉淀产生
溶液中一定含有硫酸根离子
D
将白磷浸没在热水中,再向热水中的白磷通氧气
通氧气前白磷不燃烧,通氧气后白磷燃烧
氧气是可燃物燃烧的条件之一
16.(2016,长沙)保护地球、防止环境污染是我们的重要职责,合理利用资源是保护地球的重要途径,下列关于资源利用的说法中,错误的是(C)
A.减少煤炭资源的过度开采 B.倡导“低碳生活”,绿色出行
C.为方便出行,提倡多开私家车 D.积极开发太阳能
二、填空题(23分)
17.(8分)选择下列气体填空:O2、CO和CO2,并写出有关反应的化学方程式。
(1)能使带火星的木条复燃的是__O2__。
(2)能用于灭火的是__CO2__。
(3)绿色植物进行光合作用吸收的是__CO2__,释放的是__O2__。
(4)能在空气中燃烧的是__CO__,反应的化学方程式是__2CO+O22CO2__。
(5)能使人中毒的是__CO__。
18.(9分)(2016,漳州)对物质进行归纳、分类,是学习化学的重要方法。
(1)如图是一位同学整理的有关CO2的知识网络图。
物质①的化学式是__C2H5OH__;物质②的组成元素有__三__种;物质③中的阳离子符号是__Na+__;写出CO2转化为物质④的化学方程式__CO2+H2O===_H2CO3__;物质⑤中碳元素的化合价是__+4__价。
(2)根据下列信息回答问题。
①能与碱反应生成盐和水的氧化物叫做酸性氧化物
②SO2+2NaOH=== Na2SO3+H2O
以上物质中属于酸性氧化物的是__SO2__,初中学过的__CO2__也是酸性氧化物;酸性氧化物一般是__非金属__(填“金属”或“非金属”)氧化物。
19.(6分)(2016,乐山)节约能源、保护环境、低碳生活是全社会应该倡导的生活方式。
(1)下列物质都可以用来作为燃料:①煤、②氢气、③石油、④天然气。其中,最清洁的燃料是__②__(填序号)。
(2)充分燃烧1 000 g天然气和煤所产生的CO2和SO2气体的质量如下图所示,根据图示分析,下列说法正确的是__AD__。
A.煤燃烧产生的气体更易导致酸雨
B.该天然气中不含硫元素
C.煤燃烧对环境影响较小
D.煤和天然气的燃烧都有温室气体产生
(3)硫酸型酸雨的形成主要经过以下两步: ①SO2在空气中被粉尘催化氧化得到SO3; ②SO3与水化合形成硫酸。其中反应②的化学方程式为__SO3+H2O===_H2SO4__。
(4)丙醇(化学式为C3H8O)是一种清洁燃料,它在一定量的氧气中燃烧的化学方程式可表示为C3H8O +4O2 4H2O+2CO2+X,生成物X的化学式为__CO__。要使6.0 g丙醇燃烧时不生成X,则消耗氧气的质量至少为__14.4__g。
三、实验探究题(36分)
20.(18分)(2016,邵阳)化学是一门以实验为基础的学科。结合提供的仪器,回答下列问题:
(1)写出仪器的名称:A__酒精灯__,E__长颈漏斗__。
(2)实验时,先要连接好仪器,把玻璃管插入带孔的橡胶塞时,先把玻璃管口__用水湿润__,然后对准橡胶塞上的孔稍微用力转动,将其插入。
(3)从提供的仪器中选择组装一套制取二氧化碳的装置,你选择的仪器是__CEFH__(填字母序号),组装仪器的两个原则是:①先左后右,②__先下后上__。组装好仪器,先检查__装置气密性__,然后加入药品,制取气体。
(4)实验室用澄清石灰水来检验二氧化碳气体,其反应的化学方程式是__Ca(OH)2+CO2===_CaCO3↓+H2O__。
(5)若用D装置来干燥二氧化碳气体,瓶内通常装入的试剂是__浓硫酸__。
(6)下列实验中哪一项能说明二氧化碳的物理性质__甲__(填序号)。
21.(18分)煤、石油和天然气等化石燃料是目前人类使用的最主要燃料,也是重要的化工原料。
(1)石油中主要含有__C、H__(填元素符号)两种元素;天然气的主要成分是__CH4__(填化学式)。
(2)化石燃料属于__不可再生__(填“可再生”或“不可再生”)能源,其燃烧排放的大量二氧化碳会引起全球气候变暖。一种新的处理方法是将二氧化碳气体通入含有长石(地壳中最常见的矿石,含量高达60%)成分的水溶液里,其中一种反应的化学方程式为:KAlSi3O8+CO2+2H2O===KHCO3+X↓+3SiO2↓,则X的化学式为__Al(OH)3__。
(3)工业上,煤炭燃烧前进行粉碎的目的是__增大煤与空气的接触面积__。煤隔绝空气加强热得到的焦炭,是冶铁的重要原料。为了测定某赤铁矿中氧化铁的质量分数,化学兴趣小组的同学设计了两种实验方案(假设该赤铁矿中的杂质既不溶于水,也不发生反应)。
方案Ⅰ 取8.00 g赤铁矿粉,加入足量稀硫酸,完全反应后过滤,得到1.60 g滤渣,则赤铁矿粉中氧化铁的质量分数为__80%__。
方案Ⅱ 如图所示,取8.00 g赤铁矿粉与过量的焦炭粉混合后加强热,充分反应。测得氢氧化钠溶液反应前后质量增加了1.32 g。如果产生的二氧化碳被氢氧化钠溶液完全吸收,根据所学反应3C+2Fe2O34Fe+3CO2↑计算,赤铁矿粉中氧化铁的质量分数为__40%__。
【实验反思】方案Ⅱ中硬质玻璃管内原有的空气对实验结果有影响,这会导致测出的氧化铁的质量分数__偏大__(填“偏大”“偏小”或“不变”)。
【实验分析】方案Ⅰ测出的氧化铁的质量分数明显大于方案Ⅱ测出的结果,可能的原因是__实验Ⅱ中生成的二氧化碳与过量的C反应生成一氧化碳不能被NaOH溶液吸收(或实验Ⅱ中生成的CO2不能全部被NaOH溶液吸收等合理即可)__(写出一种即可)。
四、计算题(9分)
22.(2016,贺州)重质碳酸钙粉体产业为我市一大支柱产业,产品远销全国各地。某化学兴趣小组对粉体中碳酸钙含量进行了探究,小组成员从一包粉体产品中取出样品5.10 g放入烧杯中,并逐滴加入相同浓度的稀盐酸(假设样品中的杂质不参与盐酸反应),实验测得烧杯中物质总质量与加入稀盐酸的总质量关系如表所示。
稀盐酸的总质量(g)
10.00
20.00
30.00
40.00
50.00
60.00
70.00
烧杯中物质总质量(g)
14.66
24.22
m
43.34
52.90
62.90
72.90
(1)碳酸钙的相对分子质量为__100__。
(2)表中m=__33.78__。
(3)求样品中碳酸钙的质量分数。(计算结果精确到0.01%)
解:(3)根据题意生成二氧化碳的质量为50.00 g+5.10 g-52.90 g=2.20 g
设5.10 g样品中碳酸钙的质量为x
CaCO3+2HCl=== CaCl2+H2O+CO2↑
100 44
x 2.20 g
= x=5.00 g
则碳酸钙的质量分数是×100%≈98.04%
答:样品中碳酸钙的质量分数为98.04%