- 118.50 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2019班 级 姓 名 考 场
…………………………………装………………………………………订………………………………线…………………………………………
学年度中考模拟测试化学试卷
(总分:40分 时间:50分钟)
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分40分。
可能用到的相对原子质量: H:1 C:12 O:16 Mg:24 Fe:56
第Ⅰ卷 (选择题 共15分)
一、选择题(1-5题每小题1分,6-10题每小题2分,共15分。每小题只有一个选项符合题意)
1.下列关于物质的性质或变化叙述正确的是
A.活性炭净水﹣化学性质
B.盐酸遇石蕊试液变红﹣物理性质
C.冰川融化﹣物理变化
D.工业上分离液态空气制取氧气、氮气﹣化学变化
2.下列关于水的说法不正确的是
A. 水是一种常见的溶剂
B.冰水混合物属于化合物
C.蒸馏水一定是软水
D.过滤能除去天然水中所有的杂质
3.地质考察人员发现一种带螺纹的矿石,研究时发现该矿石能在氧气中燃烧,主要反应是4X+11O2Fe2O3+8SO2。下列有关说法中不正确的是
A.X的化学式是FeS2
B.SO2中的硫、氧元素的个数比为1:2
C.反应前后氧元素的化合价发生改变
D.Fe2O3中铁元素的质量分数为70%
4.有句谚语“每天一个苹果,医生远离我”,苹果主要能为人体提供的营养素是
A.油脂 B.维生素 C.蛋白质 D.无机盐
5.下列说法正确的是
A.空气中氮气的体积分数为21%
B.生成盐和水的反应一定是中和反应
C.原子形成离子电子层数一定改变
D.玻璃钢属于金属材料
6.列关于物质的鉴别、除杂所选用的试剂或方法错误的是
选项
实验目的
试剂或方法
A
鉴别FeCl3、NaCl、NaOH、MgCl2四种溶液
不另加试剂
4
B
鉴别CaCO3、NaOH、NaCl、NH4NO3四种固体
水
C
除去MgCl2溶液中少量的CuCl2
加入过量铁粉、充分反应、过滤
D
除去N2中的少量O2
将气体缓缓通过灼热的铜网
7. 甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是
A.t2℃时将50g甲物质放入50g水中,充分搅拌后得
到100g甲溶液
B.t2℃时配制等质量的三种物质的饱和溶液,甲所需
要的水最少
C.分别将t2℃时三种物质的饱和溶液降温至t1℃,所
得溶液中溶质的质量分数的大小关系为乙>甲=丙
D.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲
溶液中析出的晶体最多,丙溶液中无晶体析出
8.室温时,随着向盛有稀硫酸的烧杯中逐滴加入Ba(OH)2溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化),下列分析正确的是
A.a点溶液中有两种溶质
B.b点溶液中滴加紫色石蕊溶液,溶液变蓝
C.c点烧杯内液体的pH=7
D.d点溶液中较多的Ba2+、OH﹣、SO42﹣、H+
9.下列各组离子在溶液中能大量共存的是
A.H+、SO42﹣、OH﹣ B.H+、Cl﹣、CO32﹣
C.Cu2+、Cl﹣、OH﹣ D.Na+、NO3﹣、SO42﹣
10.如图各组转化中,一定条件下均能一步实现的组合是
A.①② B.②③ C.①③ D.①②③
第Ⅱ卷 (非选择题 共25分)
二、填空及简答题(本题包括两小题,每空1分,共9分)
11.化学用语是学习化学的基本工具。请用化学符号或化学式填空:
⑴ 2个氢原子_________; ⑵地壳中含量最高的金属元素__________;
⑶天然气的主要成分_________;⑷ 硝酸铵的阴离子__________;
12.A~I为初中化学常见的物质,它们之间的转化关系如图1所示(只略去反应①的部分产物).其中B是紫红色金属,D、F为黑色固体,H是实验室中最常见的无色无味液体.
4
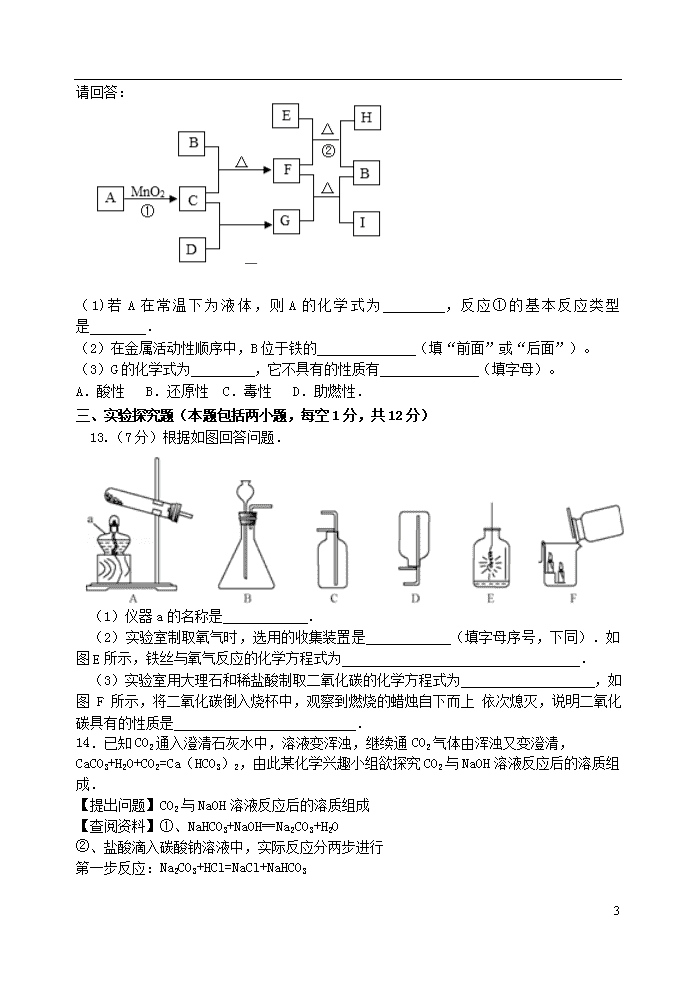
请回答:
(1)若A在常温下为液体,则A的化学式为 ,反应①的基本反应类型是 .
(2)在金属活动性顺序中,B位于铁的 (填“前面”或“后面”)。
(3)G的化学式为 ,它不具有的性质有 (填字母)。
A.酸性 B.还原性 C.毒性 D.助燃性.
三、实验探究题(本题包括两小题,每空1分,共12分)
13.(7分)根据如图回答问题.
(1)仪器a的名称是 .
(2)实验室制取氧气时,选用的收集装置是 (填字母序号,下同).如图E所示,铁丝与氧气反应的化学方程式为 .
(3)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为 ,如图 F 所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自下而上 依次熄灭,说明二氧化碳具有的性质是 .
14.已知CO2通入澄清石灰水中,溶液变浑浊,继续通CO2气体由浑浊又变澄清,CaCO3+H2O+CO2=Ca(HCO3)2,由此某化学兴趣小组欲探究CO2与NaOH溶液反应后的溶质组成.
【提出问题】CO2与NaOH溶液反应后的溶质组成
【查阅资料】①、NaHCO3+NaOH═Na2CO3+H2O
②、盐酸滴入碳酸钠溶液中,实际反应分两步进行
第一步反应:Na2CO3+HCl=NaCl+NaHCO3
4
第二步反应:NaHCO3+HCl=NaCl+H2O+CO2↑
【提出猜想】猜想1:溶质为Na2CO3。
猜想2:溶质为Na2CO3和NaOH。
猜想3:溶质为NaHCO3和Na2CO3。
猜想4:溶质为 。(填化学式,以下同)
【实验方案】Ⅰ甲组同学为确定CO2与NaOH溶液反应后所得溶液中溶质组成,设计如下实验方案.
(1)向所得溶液中加入足量的CaCl2溶液,若有白色沉淀生成,过滤后向溶液中加入足量的稀盐酸无气泡产生,则溶质为 。
(2)向所得溶液中加入足量的CaCl2溶液,若无白色沉淀生成,溶液中加入足量的稀盐酸有气泡产生,则溶质为 。
(3)(1)向所得溶液中加入足量的CaCl2溶液,若有白色沉淀生成,过滤后向溶液中加入足量的稀盐酸有气泡产生,则溶质为 。
Ⅱ乙组同学根据甲组同学的猜想,通过定量分析绘制出向所得溶液中逐滴加入稀盐酸的质量与生成二氧化碳的质量关系示意图,请根据图象确定溶质成分.
四、计算题(本题共4分)
15.将30g 碳酸钠溶液与48.2g氯化钡溶液混合,碳酸钠和氯化钡两种物质恰好完全反应。过滤,所得滤液质量为58.5g,试计算:
⑴反应后生成的沉淀质量为克.
⑵所得滤液中溶质的质量分数为多少?(用百分数表示,写出计算过程)
4
化 学 参考答案
一、选择题
题号
1
2
3
4
5
6
7
8
9
10
答案
C
D
B
B
A
C
B
C
D
C
二、填空题及简答题(每空1分,共9分)
11. 2H Al CH4 NO3-
12. (1)H2O2; 分解 (2)后面
(3)CO AD
三、实验探究题(共两小题,每空1分,共11分)
13.(1)酒精灯
(2)C,Fe+O2=Fe3O4
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑,密度比空气大,不可燃,不助燃
14. NaOH (1) Na2CO3或Na2CO3和NaOH (2)NaHCO3(3)NaHCO3和Na2CO3
B、NaHCO3;C、Na2CO3和NaOH;D、Na2CO3和NaHCO3;
四、计算题(本题共5分)
(1) 19.7 (2)20%
(2) 解:设溶液中溶质NaCl的质量为x
Na2CO3+BaCl2="2NaCl" + BaCO3↓
117 197
x 19.7g
x=11.7g
滤液中溶质的质量分数为×100%=20%
化学试卷 第 5 页 共 5 页