- 428.50 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
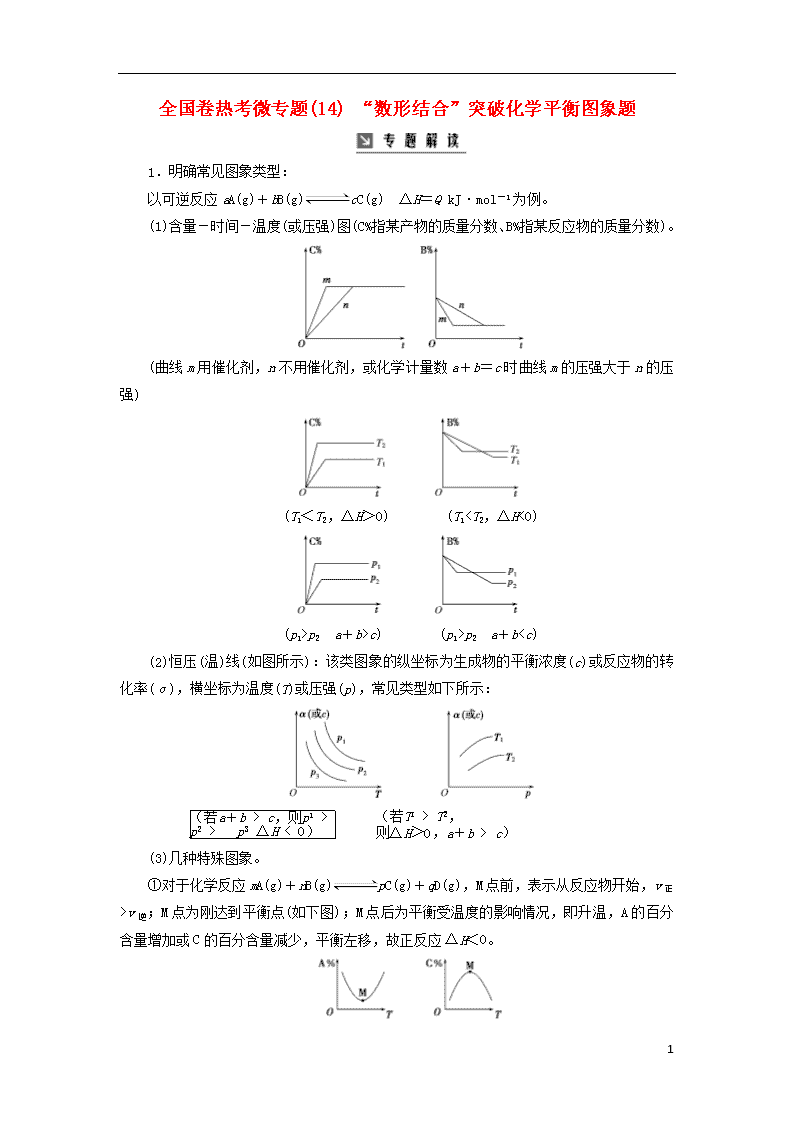
全国卷热考微专题(14) “数形结合”突破化学平衡图象题
1.明确常见图象类型:
以可逆反应aA(g)+bB(g)cC(g) ΔH=Q kJ·mol-1为例。
(1)含量-时间-温度(或压强)图(C%指某产物的质量分数、B%指某反应物的质量分数)。
(曲线m用催化剂,n不用催化剂,或化学计量数a+b=c时曲线m的压强大于n的压强)
(T1<T2,ΔH>0) (T1p2 a+b>c) (p1>p2 a+bv逆;M点为刚达到平衡点(如下图);M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,平衡左移,故正反应ΔH<0。
8
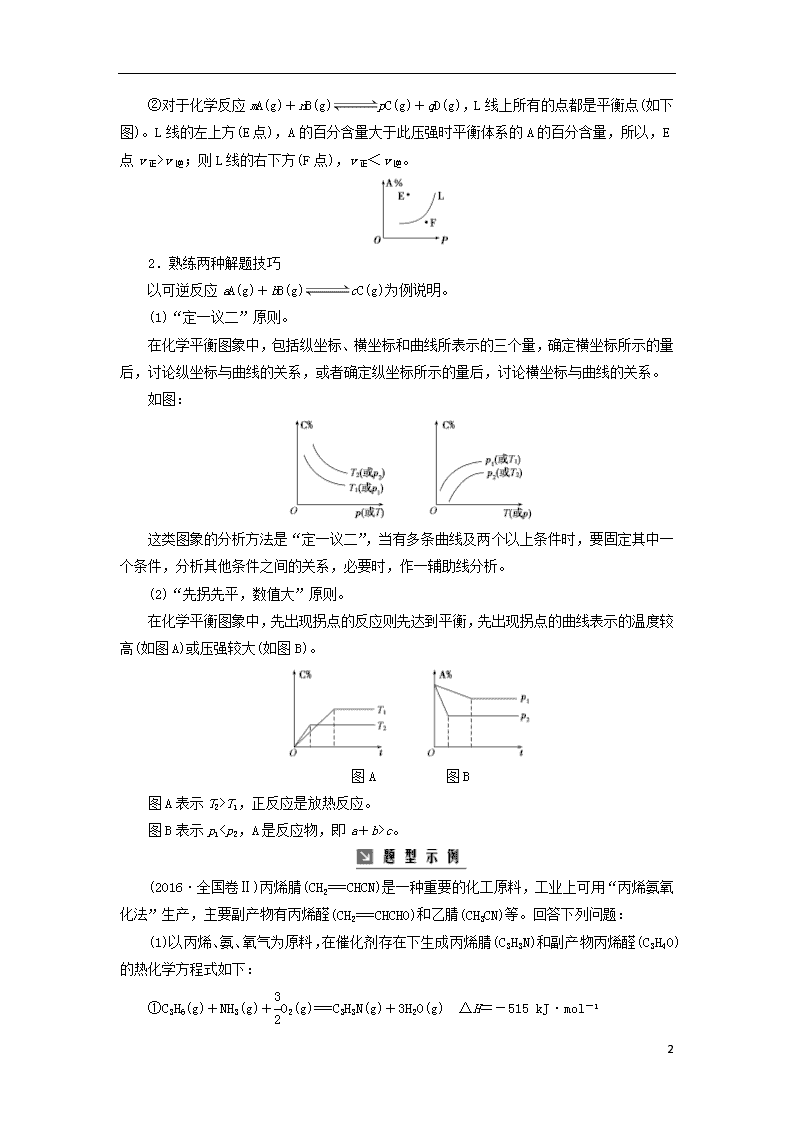
②对于化学反应mA(g)+nB(g)pC(g)+qD(g),L线上所有的点都是平衡点(如下图)。L线的左上方(E点),A的百分含量大于此压强时平衡体系的A的百分含量,所以,E点v正>v逆;则L线的右下方(F点),v正<v逆。
2.熟练两种解题技巧
以可逆反应aA(g)+bB(g)cC(g)为例说明。
(1)“定一议二”原则。
在化学平衡图象中,包括纵坐标、横坐标和曲线所表示的三个量,确定横坐标所示的量后,讨论纵坐标与曲线的关系,或者确定纵坐标所示的量后,讨论横坐标与曲线的关系。
如图:
这类图象的分析方法是“定一议二”,当有多条曲线及两个以上条件时,要固定其中一个条件,分析其他条件之间的关系,必要时,作一辅助线分析。
(2)“先拐先平,数值大”原则。
在化学平衡图象中,先出现拐点的反应则先达到平衡,先出现拐点的曲线表示的温度较高(如图A)或压强较大(如图B)。
图A 图B
图A表示T2>T1,正反应是放热反应。
图B表示p1c。
(2016·全国卷Ⅱ)丙烯腈(CH2===CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2===CHCHO)和乙腈(CH3CN)等。回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①C3H6(g)+NH3(g)+O2(g)===C3H3N(g)+3H2O(g) ΔH=-515 kJ·mol-1
8
②C3H6(g)+O2(g)===C3H4O(g)+H2O(g)
ΔH=-353 kJ·mol-1
两个反应在热力学上趋势均很大,其原因是_________________
_______________________________________________________
_____________________________________________________;
有利于提高丙烯腈平衡产率的反应条件是__________________
_______________________________________________________
_____________________________________________________;
提高丙烯腈反应选择性的关键因素是______________________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460 ℃,低于460 ℃时,丙烯腈的产率________(填“是”或“不是”)对应温度下的平衡产率,判断理由是__________________
_______________________________________________________
______________________________________________________;
高于460 ℃时,丙烯腈产率降低的可能原因是________(双选,填标号)。
A.催化剂活性降低 B.平衡常数变大
C.副反应增多 D.反应活化能增大
解析:(1)因为生成的产物丙烯腈和丙烯醛的两个反应均为放热量大的反应,所以它们均可自发进行且热力学趋势大;该反应为气体体积增大的放热反应,所以降低温度、降低压强有利于提高丙烯腈的平衡产率;由生成丙烯腈的反应条件可知,提高丙烯腈反应选择性的关键因素是催化剂。(2)因为该反应为放热反应,平衡产率应随温度升高而降低,反应刚开始进行,主要向正反应方向进行,尚未达到平衡状态,460 ℃以前是建立平衡的过程,故低于460 ℃时,丙烯腈的产率不是对应温度下的平衡产率;高于460 ℃时,丙烯腈产率降低,A项,催化剂在一定温度范围内活性较高,若温度过高,活性降低,正确;B项,平衡常数的大小不影响产率,错误;C项,根据题意,副产物有丙烯醛,副反应增多导致产率下降,正确;D项,反应活化能的大小不影响平衡,错误。
答案:(1)两个反应均为放热量大的反应 降低温度、降低压强 催化剂 (2)不是 该反应为放热反应,平衡产率应随温度升高而降低 AC
8
[方法指导] 掌握化学平衡图象题解答步骤
第一步:看特点。即分析可逆反应化学方程式,观察物质的状态、气态物质分子数的变化(正反应是气体分子数增大的反应,还是气体分子数减小的反应)、反应热(正反应是放热反应,还是吸热反应)等。
第二步:识图象。即识别图象类型,横坐标和纵坐标的含义、线和点(平台、折线、拐点等)的关系。利用规律“先拐先平,数值大”判断,即曲线先出现拐点,先达到平衡,其温度、压强越大。
第三步:想原理。联想化学反应速率、化学平衡移动原理,特别是影响因素及使用前提条件等。
第四步:巧整合。图表与原理整合。逐项分析图表,重点看图表是否符合可逆反应的特点、化学反应速率和化学平衡原理。
1.密闭容器中进行的可逆反应:aA(g)+bB(g)cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是( )
A.T1<T2,p1<p2,a+b>c,正反应为吸热反应
B.T1>T2,p1<p2,a+b<c,正反应为吸热反应
C.T1<T2,p1>p2,a+b<c,正反应为吸热反应
D.T1>T2,p1>p2,a+b>c,正反应为放热反应
解析:由(T1,p1)和(T1,p2)两条曲线可以看出:①温度相同(T1),但压强为p2时达到平衡所需的时间短,即反应速率大,所以p2>p1;②压强较大(即压强为p2)时对应的w(B)较大,说明增大压强平衡逆向移动,则a+b<c。由(T1,p2)和(T2、p2)两条曲线可以看出:①压强相同(p2),但温度为T1时达到平衡所需的时间短,即反应速率大,所以T1>T2;②温度较高(即温度为T1)时对应的w(B)较小,说明升高温度平衡正向移动,故正反应为吸热反应。
答案:B
2.有一化学平衡mA(g)+nB(g)pC(g)+qD(g),如图表示的是A的转化率与压强、温度的关系。下列叙述正确的是( )
8
A.正反应是放热反应;m+n>p+q
B.正反应是吸热反应;m+n<p+q
C.正反应是放热反应;m+n<p+q
D.正反应是吸热反应;m+n>p+q
解析:图象中有三个量,应定一个量来分别讨论另外两个量之间的关系。定压强,讨论T与A的转化率的关系:同一压强下,温度越高,A的转化率越高,说明正反应是吸热反应;定温度,讨论压强与A的转化率的关系:同一温度下,压强越大,A的转化率越高,说明正反应是气体体积缩小的反应,即m+n>p+q。
答案:D
3.在一恒容的密闭容器中充入0.1 mol·L-1 CO2、0.1 mol·L-1 CH4,在一定条件下发生反应:CH4(g)+CO2(g)2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )
A.上述反应的ΔH<0
B.压强:p4>p3>p2>p1
C.1 100 ℃时该反应的平衡常数为1.64
D.压强为p4时,在y点:v正>v逆
解析:p1、p2、p3、p4是四条等压线,由图象可知,压强一定时,温度越高,甲烷的平衡转化率越高,故正反应为吸热反应,ΔH>0,A项错误;该反应为气体分子数增加的反应,压强越高,甲烷的平衡转化率越小,故压强p4>p3>p2>p1,B项正确;压强为p4,温度为1 100 ℃时,甲烷的平衡转化率为80.00%,故平衡时各物质的浓度分别为c(CH4)=0.02 mol·L-1,c(CO2)=0.02 mol·L-1,c(CO)=0.16 mol·L-1,c(H2)=0.16 mol·L-1,即平衡常数K==1.64,C项正确;压强为p4时,y点未达到平衡,此时v正>v逆,D项正确。
答案:A
4.有一反应:2A+B2C,其中A、B、C均为气体,如图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c三点,则下列描述正确的是( )
8
A.该反应是放热反应
B.b点时混合气体的平均摩尔质量不再变化
C.T1温度下若由a点达到平衡,可以采取增大压强的方法
D.c点v正<v逆
解析:由于温度升高,B的转化率增大,说明平衡正向移动,推知该反应是吸热反应,A错误;在T1温度下,由a点达平衡时,B的转化率不断减小,若采取加压措施,结合化学方程式可知B的转化率会不断增大,C错误;在T2温度下,c点会达到平衡状态,此过程中B的转化率不断增大,说明该过程v正>v逆,D错误。
答案:B
5.(2016·海南卷)顺1,2二甲基环丙烷和反1,2二甲基环丙烷可发生如下转化:
该反应的速率方程可表示为v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。回答下列问题:
(1)已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K1=________;该反应的活化能Ea(正)小于Ea(逆),则ΔH________0(填“小于”“等于”或“大于”)。
(2)t2温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是________(填曲线编号),平衡常数值K2=______________;温度t2________t1(填“小于”“等于”或“大于”),判断理由是________
______________________________________________________。
解析:(1)根据v(正)=k(正)·c(顺)=0.006c(顺),v(逆)=k(逆)·c(反)=0.002c(反),化学平衡状态时正逆反应速率相等,则0.006c(顺)=0.002c(反),K1==0.006÷0.002=3;该反应的活化能Ea(正)小于Ea(逆),说明断键吸收的能量小于成键释放的能量,即该反应为放热反应,则ΔH小于零。
(2)反应开始时,c(顺)的浓度大,单位时间的浓度变化大,w(顺)的变化也大,
8
故B曲线符合题意,设顺式异构体的起始浓度为x,该可逆反应左右物质系数相等,均为1,则平衡时,顺式异构体为0.3x,反式异构体为0.7x,所以平衡常数值K2=0.7x÷0.3x=7/3,因为K1>K2,放热反应升高温度时平衡向逆反应方向移动,所以温度t2大于t1。
答案:(1)3 小于 (2)B 7/3 大于 放热反应升高温度时平衡向逆反应方向移动
6.甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇。发生的主要反应如下:
①CO(g)+2H2(g)CH3OH(g) ΔH1
②CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)CO(g)+H2O(g) ΔH3
回答下列问题:
(1)反应①的化学平衡常数K表达式为______________;图1中能正确反映平衡常数K随温度变化关系的曲线为________(填曲线标记字母),其判断理由是______________________________________
_____________________________________________________。
图1
(2)合成气组成n(H2)/n(CO+CO2)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而________(填“增大”或“减小”),其原因是__________________;
图2中的压强由大到小为________________,其判断理由是
_____________________________________________________。
图2
解析:(1)根据化学平衡常数的书写要求可知,反应①的化学平衡常数为K=c(CH3OH)/[c(CO)·c2(H2)]。反应①为放热反应,温度升高,平衡逆向移动,平衡常数K减小,故曲线a符合要求。
(2)由图2可知,压强一定时,CO的平衡转化率随温度的升高而减小,其原因是反应①为放热反应,温度升高,平衡逆向移动,反应③为吸热反应,温度升高,平衡正向移动,
8
又使产生CO的量增大,而总结果是随温度升高,CO的转化率减小。反应①的正反应为气体总分子数减小的反应,温度一定时,增大压强,平衡正向移动,CO的平衡转化率增大,而反应③为气体总分子数不变的反应,产生CO的量不受压强的影响,因此增大压强时,CO的转化率提高,故压强p1、p2、p3的关系为p1<p2<p3。
答案: (1)K=[或Kp=]
a 反应①为放热反应,平衡常数数值应随温度升高变小
(2)减小 升高温度时,反应①为放热反应,平衡向左移动,使得体系中CO的量增大;反应③为吸热反应,平衡向右移动,又使产生CO的量增大;总结果,随温度升高,使CO的转化率降低
p3>p2>p1 相同温度下,由于反应①为气体分子数减小的反应,加压有利于提升CO的转化率;而反应③为气体分子数不变的反应,产生CO的量不受压强影响。故增大压强时,有利于CO的转化率升高
8
相关文档
- 高中历史人民版选修三20世纪的战争2021-05-1322页
- 高中生物一轮复习蛋白质的相关高考2021-05-133页
- 2020版高中数学 第三章 概率 32021-05-134页
- 2018高考高中语文散文阅读技巧2021-05-139页
- 高考复习——高中历史知识点汇编更2021-05-13170页
- 2020版高中数学 第二章 算法初步 22021-05-133页
- 高中化学计算题总结高考真题2021-05-135页
- 高考备战冲刺指导高中数学必修15知2021-05-138页
- 2016江苏普通高中学业水平测试小高2021-05-1310页
- 河南普通高中新课程高考适应性考试2021-05-1315页