- 3.71 MB
- 2021-05-14 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
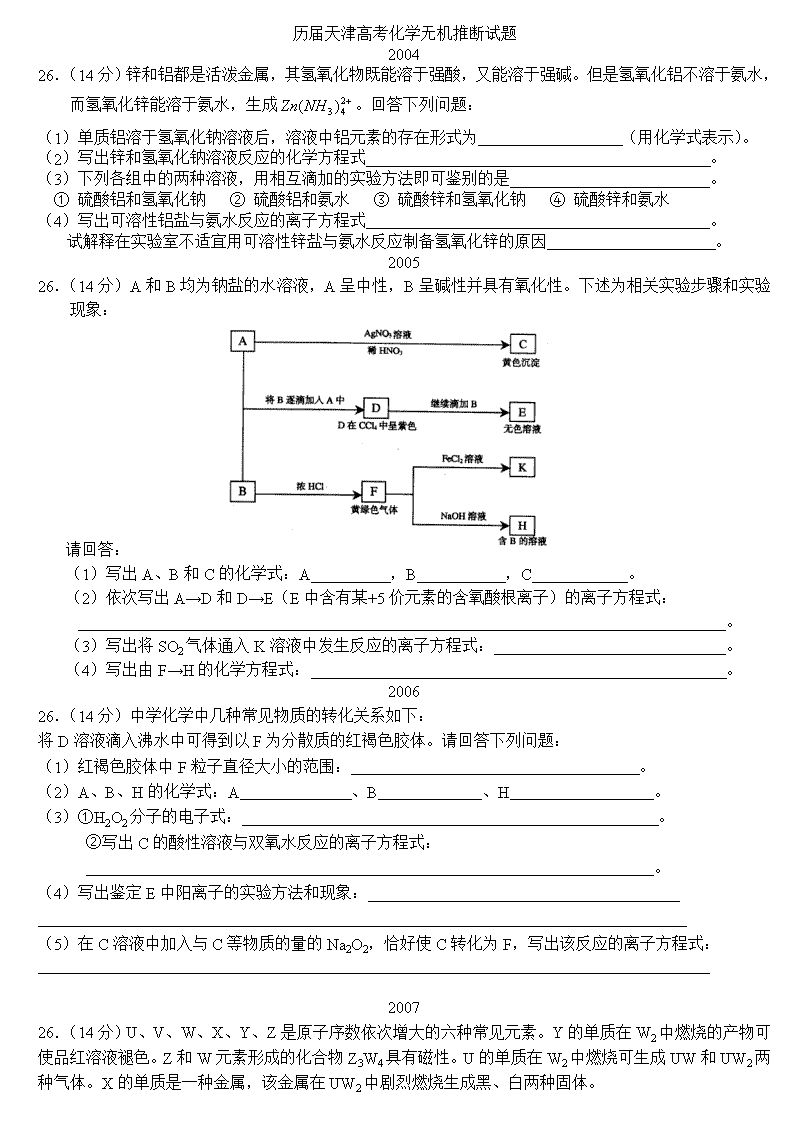
历届天津高考化学无机推断试题
2004
26.(14分)锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为 (用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式 。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是 。
① 硫酸铝和氢氧化钠 ② 硫酸铝和氨水 ③ 硫酸锌和氢氧化钠 ④ 硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式 。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因 。
2005
26.(14分)A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象:
请回答:
(1)写出A、B和C的化学式:A ,B ,C 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式: 。
(4)写出由F→H的化学方程式: 。
2006
26.(14分)中学化学中几种常见物质的转化关系如下:
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围: 。
(2)A、B、H的化学式:A 、B 、H 。
(3)①H2O2分子的电子式: 。
②写出C的酸性溶液与双氧水反应的离子方程式:
。
(4)写出鉴定E中阳离子的实验方法和现象:
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:
2007
26.(14分)U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
⑴.V的单质分子的结构式为_______________;XW的电子式为____________;
Z元素在周期表中的位置是_____________。
⑵.U元素形成的同素异形体的晶体类型可能是(填序号)__________。
① 原子晶体 ② 离子晶体 ③ 分子晶体 ④ 金属晶体
⑶.U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)____________;V、W的氢化物分子结合H+能力较强的是(写化学式)______________,用一个离子方程式加以证明____________________________________________________。
⑷.YW2气体通人BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为__________________________,由此可知VW和YW2还原性较强的是(写化学式)_________
2008
26.(14分)W、X、Z、Y是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为____________。
(2)W与Y可形成化合物W2Y,该化合物的电子式为___________________________。
(3)X的硝酸盐水溶液显_________性,用离子方程式解释原因:
__________________________________________________________________________。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
__________________________________________________________________________。
(5)比较Y、Z气态氢化物的稳定性:______________ >______________(用分子式表示)。(6)W、X、Y、Z因种元素简单离子的离子半径由大到小的顺序是
_____________ > ___________ > ___________ > ______________。
(7)Z的最高价氧化物为无色液体,0.25 mol 该物质与一定量水混合得到一种稀溶液,并
放出Q kJ 的热量。写出该反应的热化学方程式:
__________________________________________________________________________。
2009
7.(14分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族
周期
IA
0
1
①
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
②
③
④
3
⑤
⑥
⑦
⑧
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
X溶液与Y溶液反应的离子方程式为_____________________,
N→⑥的单质的化学方程式为________________。
常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至_________________。
2010
7.(14分)X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
⑴ L的元素符号为________ ;M在元素周期表中的位置为________________;五种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
⑵ Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___,B的结构式为____________。
⑶ 硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______,其最高价氧化物对应的水化物化学式为_______。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。[来源:学科网]
a.+99.7 mol·L-1 b.+29.7 mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
⑷ 用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式:______________;由R生成Q的化学方程式:_______________________________________________。
2011
7.(14分)图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。
回答下列问题:
⑴组成单质Y的元素在周期表中的位置是 ;M中存在的化学键类型为 ;R的化学式是 。
⑵一定条件下,Z与H2反应转化为ZH4。ZH4的电子式为 。
⑶已知A与1mol Al反应转化为X时(所有物质均为固体),放出akJ热量,写出该反应的热化学方程式: 。
⑷写出A和D的稀溶液反应生成G的离子方程式: 。
⑸向含4mol D的稀溶液中,逐渐加入X粉末至过量,假设生成的气体只有一种,请在坐标系中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值。
2012
7.(14分)X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
⑴ Y在元素周期表中的位置为________________。
⑵ 上述元素的最高价氧化物对应的水化物酸性最强的是_______(写化学式),非金属气态氢化物还原性最强的是_____(写化学式)。
⑶ Y、G的单质或两元素之间形成的化合物可作水消毒剂的有___________(写出其中两种物质的化学式)。
⑷ X2M的燃烧热ΔH = -a kJ·mol-1 ,写出X2M燃烧反应的热化学方程式:_____。
⑸ ZX的电子式为___________;ZX与水反应放出气体的化学方程式为__________。
⑹ 熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),反应原理为:
2Z + FeG2 Fe + 2ZG
放电时,电池的正极反应式为________:充电时,______________(写物质名称)电极接电源的负极;该电池的电解质为________。
2013
7、X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1) 五种元素原子半径由大到小的顺序是(写元素符号)
(2) X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)
(3) 由以上某些元素组成的化合物A、B、C、D有如下转化关系
其中C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式 ;D的电子式
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为
由A转化为B的离子方程式
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因 。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是 ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有 。
2014
7.(14分)元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
⑴ 按原子序数递增的顺序(稀有气体除外),以下说法正确的是__________。
a.原子半径和离子半径均减小 b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强 d.单质的熔点降低
⑵ 原子最外层电子数与次外层电子数相同的元素名称为_______,氧化性最弱的简单阳离子是_____________。
⑶ 已知:
化合物
MgO
Al2O3
MgCl2
AlCl3
类型
离子化合物
离子化合物
离子化合物
共价化合物
熔点/℃
2800
2050
714
191
工业制镁时,电解MgCl2而不电解MgO的原因是:____________________________。
制铝时,电解Al2O3而不电解AlCl3的原因是:________________________________。
⑷ 晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:
Si(粗) SiCl4 SiCl4(纯) Si(纯)
写出SiCl4的电子式:_____________________;在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:
__________________________________________________________。
⑸ P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是_____。
a.NH3 b.HI c.SO2 d.CO2
⑹ KClO3可用于实验室制O2 ,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程:___________________。
答案
04年
26.(14分) (1)[或]
(2)
[或]
(3)①③④ (4)
05年
26.(1)Nal NaClO Agl
(2)2I-+ClO-+H2O I2+Cl-+2OH-; I2+5ClO-+2OH- 2I3-+5Cl-+H2O
(3)2Fe3++SO2+2H2O 2Fe2++SO+4H+
(4)Cl2+2NaOH NaClO+NaCl+H2O
06年
26.(14分)
(1)1nm—100nm
··
··
··
··
··
··
H
··
O
O
H
(2)Fe FeS H2SO4(稀)
(3)①
②
(4)取少量E于试管中,用胶头滴管入NaOH溶液,加热试管,可观察到试管口处湿润的红色石蕊试纸变蓝。(或其他合理答案)
(5)4Fe2++4Na2O2+6H2O 4Fe↓+O2↑+8Na+
07年
26.(14分)
⑴.N≡N (1分)
⑵. (1分)
第4周期,第VIII族 (2分)
⑵.① ③ (2分)
⑶.CH4 NH3 (各1分,共2分)
NH3 + H3O+ ==== NH + H2O (2分)
⑷.3SO2 + 2NO + 3Ba2+ + 2H2O ==== 3BaSO4 ↓ + 2NO + 4H+ (2分)
SO2 (1分)
08年
26.(14分)
(1)Al(OH)3+OH-==Al+2H2O
(2)
(3)酸
Al3++3 H2O Al(OH)3+3H+
(4)SO2+Cl2+2H2O==H2SO4+2HCl
(5)HCl>H2S
(6)S>Cl>Na>Al
(7)Cl2O7(l)+H2O(l)==2HClO4(aq);ΔH=-4QkJ/mol
09年
7.(共14分)
10年
解析:(1)X、Y、Z、L是组成蛋白质的四种元素且原子序数依次增大,故分别为:H、C、N、O元素;M是地壳中含量最高的元素,为Al,其在周期表的位置为第3周第ⅢA族;再根据五种元素在周期表的位置,可知半径由大到小的顺序是:Al>C>N>O>H。
(2) N和H 1:3构成的分子为NH3,电子式为;2:4构成的分子为N2H4,其结构式为。
(3)Se比O多两个电子层,共4个电子层,1→4电子层上的电子数分别为:2、8 、18、6,故其原子序数为34;其最高价氧化物对应的水化物的化学式类似H2SO4,为H2SeO4。
非金属性越强,与氢气反应放出的热量越多,故2→5周期放出的热量依次是:d、c、b、a,则第四周期的Se对应的是b。
(4)Al作阳极失去电子生成Al3+,Al3++3HCO3-==Al(OH)3+3CO2,2Al(OH)3Al2O3+3H2O。
答案:
(1)O 第三周第ⅢA族 Al>C>N>O>H
(2)
(3) 34 H2SeO4 b
(4) Al-3e-Al3+ Al3++3HCO3-==Al(OH)3+3CO2 2Al(OH)3Al2O3+3H2O。
命题立意:本题以元素的推断为背景,综合考查了元素符号的书写、元素位置的判断和原子半径大小的比较;考查了电子式、结构式的书写,元素周期律,和电极反应式、化学方程式的书写,是典型的学科内综合试题。
2011年
7.⑴第二周期第VIA族 离子键、共价键 H2SiO3(或H4SiO4)
⑵
⑶8Al(s)+3Fe3O4(s)=9Fe(s)+4Al2O3(s) △H=-8a kJ/mol
⑷3Fe3O4+28H++NO3-9Fe3++NO↑+14H2O
⑸
2012
由已知条件首先推断X、Y、Z、M、G元素分别为H、O、Na、S、Cl
(1)Y第2周期VIA
(2)最高价氧化物对应水化物酸性最强的是HClO4,非金属性越弱,气态氢化物还原性越强,气态氢化物还原性最强的是H2S
(3)Y的单质O3、G的单质Cl2、二者形成的ClO2可作消毒剂
(4)据燃烧热的含义,写H2S燃烧的热化学方程式生成物应该生成SO2,
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-2aKJ·mol-1
(5),NaH+H2O=NaOH+H2
(6)2Na+FeCl2Fe+NaCl,放电时正极发生还原反应,应该是Fe2+得电子,电极反应式为Fe2++2e-= Fe。充电时原电池的负极材料Na接电源的负极。该电池的电解质为B-Al2O3
2013
(1)根据短周期元素、X、Y元素的X、Y两元素最高正价与最低负价之和均为0;推知X Y元素分别为H和C,Q与X同主族推知Q为Na元素,Z、R分别是地壳中含量最高的非金属元素和金属元素,推知Z为O元素,R为Al元素。
原子半径大小顺序为Na>Al>C>O>H
(2)C和H形成的物质是有机化合物,含极性键又含非极性键,分子质量最小的只能是
C2H2
(3)C溶于水显酸性的气体只能是CO2,D是淡黄色固体,只能是过氧化钠
,
①B为两性不溶物,A B均由三种元素组成,根据转化关系A为NaAlO2,
B为Al(OH)2由A转化为B的离子方程式AlO2-+2H2O+CO2=Al(OH)3+HCO3-或
2 AlO2-+3 H2O+CO2=2 Al(OH)3+CO32-
②A由三种元素组成,B由四种元素组成,A、B溶液均显碱性,A是Na2CO3,B是NaHCO3.A显碱性的原因是CO32-的水解。水解的离子方程式为CO32-+H2OHCO3-+OH-,二者等浓度的混合溶液中,离子浓度的大小顺序为c(Na+)> c(HCO3-) >c(CO32-)> c(OH-)> c(H+), 碳酸根的水解程度比碳酸氢根的水解程度大。在滴加盐酸至中性时,碳酸钠和盐酸反应生成NaHCO3,NaHCO3和盐酸反应生成NaCl、H2O、CO2、若果溶质全是NaCl,由于有CO2,溶液就显酸性,所以溶质是NaHCO3、NaCl、CO2。
2014
7.(14分)
⑴ b
⑵ 氩 Na+ (或钠离子)
⑶ MgO的熔点高,熔融时耗费更多能源,增加生产成本
AlCl3是共价化合物,熔融态难导电
⑷
SiCl4 (g) + 2H2 (g) Si (s) + 4HCl (g);△H = +0.025a kJ·mol-1
⑸ b
⑹ 4KClO3 KCl + 3KClO4
相关文档
- 2017高考语文试卷及解析2021-05-1410页
- 答案定语从句20122016高考真题2021-05-149页
- 冲刺高考完形填空30篇附答案解析2021-05-1428页
- 2019高考物理高频考点重点新题精选2021-05-1420页
- 2017上海高考数学试题完整Word版含2021-05-147页
- 2020届高考物理一轮复习 第7章 1 2021-05-143页
- 高考语文一轮复习对点训练 评价古2021-05-142页
- 高考历史时知识点专题练习322021-05-1414页
- 高考数学客观题训练6套选择填空题2021-05-148页
- 高考数学第一轮复习10三角恒等变换2021-05-1415页