- 139.50 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2019学年第一学期期中考试高(一)化学试题
(本试卷100分,共6页)
可能用到的相对原子质量:H-1, O-16, S-32,C-12,N-14,Cu-64 ,Na-23
一、选择题(每小题只有一个正确答案,每题2分,共60分)
1.下列实验操作正确的是( )
A.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部
B.用蒸发的方法使NaCl从溶液中析出时,将溶液蒸干才停止加热
C.利用碘在CCl4中溶解度比在水中大,可用CCl4从稀的碘水中萃取碘
D.过滤时,为加快过滤速率,可用玻璃棒快速搅拌漏斗中的悬浊液
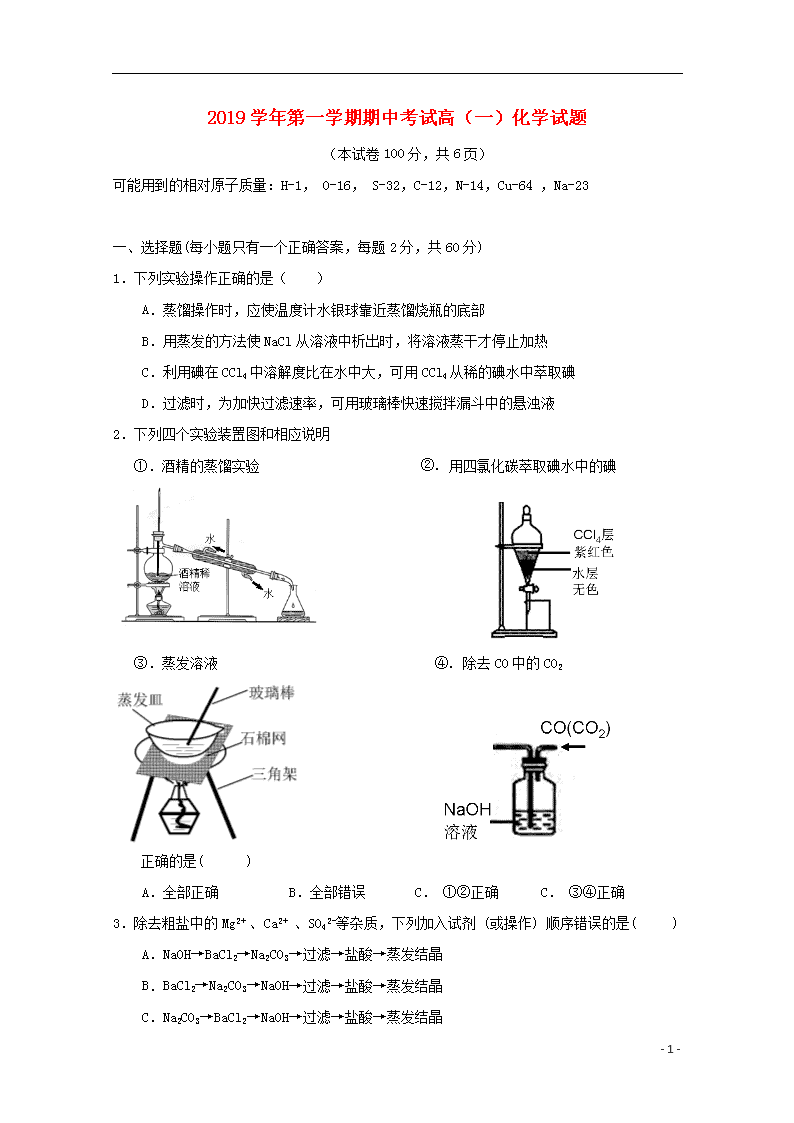
2.下列四个实验装置图和相应说明
①.酒精的蒸馏实验 ②. 用四氯化碳萃取碘水中的碘
③.蒸发溶液 ④. 除去CO中的CO2
正确的是( )
A.全部正确 B.全部错误 C. ①②正确 C. ③④正确
3.除去粗盐中的Mg2+ 、Ca2+ 、SO42-等杂质,下列加入试剂 (或操作) 顺序错误的是( )
A.NaOH→BaCl2→Na2CO3→过滤→盐酸→蒸发结晶
B.BaCl2→Na2CO3→NaOH→过滤→盐酸→蒸发结晶
C.Na2CO3→BaCl2→NaOH→过滤→盐酸→蒸发结晶
- 6 -
D.BaCl2→NaOH→Na2CO3→过滤→盐酸→蒸发结晶
4.下列实验能够说明溶液中存在SO42-的是( )
A.加入BaCl2溶液,产生白色沉淀
B.加入BaCl2溶液,产生白色沉淀,再加盐酸,沉淀不消失
C.加入足量稀盐酸,没有明显现象,再加入BaCl2溶液,产生白色沉淀
D.加入过量Ba(OH)2溶液,产生白色沉淀,再加入少量盐酸,沉淀不消失。
5.下列物质的分类正确的是( )
酸
碱
盐
氧化物
A
H2SO4
Na2CO3
CaCl2
H2O
B
硝酸
烧碱
小苏打NaHCO3
干冰
C
NaHSO4
铜绿Cu2(OH)2CO3
生石灰
熟石灰
D
CO2
氢氧化铜
氯化铵
生石灰
6.同类物质性质相似,SO2和CO2同属于酸性氧化物,性质类似。下列说法不正确的是( )
A.SO2与澄清石灰水反应生成白色沉淀CaSO3 B.SO2与BaO反应,生成BaSO3
C.SO2与水反应生成H2SO3 D.SO2和Na2O反应生成Na2SO4
7.溶液、胶体和浊液这三种分散系的根本区别是( )
A.是否有丁达尔现象 B.分散质粒子直径的大小
C.是否能透过滤纸 D.是否为均一、稳定、透明的外观
8.下列叙述正确的是( )
A.1 mol H2O 的质量是18 g/mol B.CH4 的摩尔质量是16 g
C.1mol/LMgCl2溶液中含有Cl﹣的数目为2NA D.3.01×1023个O2分子的质量是16 g
9.下列每组中的两种物质所含有原子总数目相等的是( )
A.3mol H2O2 2mol NH4Cl B. 18gH2O 18gCO2
C.1L CO2 1LCH4 D.2mol/L HCl 2mol/L HNO3
10.下列说法正确的是( )
A.1mol H2O分子中含有6.02×1023个微粒 B.44gCO2中含有1.204×1024个O原子
C.NH3的摩尔质量为17 D. 44.8L CH4含有2mol C原子
11.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
A. 9gH2O所含有的H原子数为2NA
- 6 -
B.0.2mol/L CaCl2溶液中所含有的Cl-数为0.4NA
C.22.4L H2SO4 的H原子数为2NA
D.标准状况下5.6L CH4气体中含有的H原子数为NA
12.下列溶液中,与100 mL 0.5 mol/LCaCl2溶液所含的Cl-的物质的量浓度相同的是( )
A.10 ml 0.5 mol/LMgCl2溶液 B.100 ml 0. 5 mol/L HCl溶液
C.500 ml 0.2 mol/L NaCl溶液 D.1000 ml0.05 mol/L BaCl2 溶液
13.下列类型的反应,一定发生电子转移的是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
14.下列变化中,加入氧化剂才可以实现的是( )
A. Cl2 → Cl- B.H+ → H2 C.Na2O → NaOH D.Cu → Cu2+
15. 实验室要配制1.0mol/L硫酸溶液500mL,需要用10mol/L的硫酸溶液的体积是( )
A.25mL B.12.5mL C.100mL D.50mL
16.下列粒子中,既有氧化性又有还原性的是( )
A.Na+ B.O2 C.Fe2+ D.Cl-
17.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO42ClO2↑+K2SO4+2CO2↑+2H2O,下列说法正确的( )
A.1 molKClO3参加反应有2mole- 转移 B.ClO2是氧化产物
C.H2C2O4在反应中被还原 D.KClO3在反应中得到电子,作还原剂
18.下列反应中,氯元素被氧化的是( )
A.2KClO32KCl+3O2↑ B.2P+5Cl22PCl5
C.MnO2+4HCl(浓)MnCl2+2H2O+Cl2↑ D.H2+Cl22HCl
19.下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是 ( )
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体
A.①和④ B.①和③ C.③和④ D.①和②
20.某实验需要用到80mL 0.1mol/L CuSO4溶液,下列说法正确的是( )
A.称取1.28gCuSO4粉末,溶解在80mL水中
B.称取2.0gCuSO4·5H2O晶体,溶解在80mL水中
C.称取2.0gCuSO4粉末,用容量瓶配制成100mL溶液
D.称取2.5gCuSO4·5H2O晶体,用容量瓶配制成100mL溶液
- 6 -
21.下列方法能够成功制备Fe(OH)3胶体的是( )
A、将1 mL饱和FeCl3溶液加入到20 mL NaOH溶液
B、将1 mL饱和FeCl3溶液逐滴加入到20 mL温水中,边加边振荡,并加热到沸腾
C、将1 mL饱和FeCl3溶液一次性加入到20 mL沸水中,并加以搅拌
D、将5-6滴饱和FeCl3溶液逐滴加入到20 mL沸水中,继续煮沸至呈红褐色
22.下列物质混合后,没有离子反应发生的是( )
A、Na2CO3溶液与稀盐酸 B、CuSO4溶液与BaCl2溶液
C、H2SO4溶液与NaCl溶液 D、稀HNO3与Ba(OH)2溶液
23.在无色透明的碱性溶液中,能够大量共存的离子组是 ( )
A.Cu2+、Na+、SO42-、Cl- B. NO3-、Cl-、Ba2+、Mg2+
C.Ba2+、Na+、Cl-、NO3- D. NH4+、Cl+、 H+、NO3-
24. 下列物质的水溶液可以导电,但是本身不是电解质的为( )
A.CO2 B.HCl C.蔗糖 D.BaCO3
25.下列反应的离子方程式正确的是( )
A.铁与盐酸:2Fe + 6H+ == 2Fe3+ + 3H2↑
B.CuO和硝酸:O2- + 2H+ == H2O
C.盐酸和NaHCO3: H+ + HCO3- == CO2 ↑+ H2O
D.Ba(OH)2和H2SO4 溶液:Ba2+ + OH- + H+ + SO42- == Ba SO4↓ + H2O
26.下列反应能用离子方程式 H++OH- = H2O 表示的是( )
A.Ba(OH)2和H2SO4 B.KOH和NaHSO4
C.Cu(OH)2和HNO3 D.KOH和醋酸
27.对于Fe+2HCl=FeCl2+ H2↑反应,下列说法不正确的是( )
A.Fe是还原剂,被氧化
B.HCl是氧化剂,发生了还原反应
C.此反应既是置换反应又是氧化还原反应
D.-1价氯在反应中价态未变,所以HCl既不是氧化剂,又不是还原剂
28.下列反应中是氧化还原反应且水是还原剂的是( )
A.SO3+H2O == H2SO4 B.2F2+2H2O == 4HF + O2
C.2H2 + O2 点燃 2H2O D.Cl2 + H2O == HCl + HClO
29.根据Cu2+ + Zn = Zn2+ +Cu ,2Ag + + Cu = 2Ag + Cu2+ 可知下列分析
- 6 -
①氧化性:Ag + > Cu2+ > Zn2+ ; ②氧化性:Ag + Cu > Ag ④还原性:Zn < Cu H>Cu,而氧化性:Mg2+I2>S,而还原性:Cl-
相关文档
- 人教版高中化学选修五 3_1醇 酚第42021-07-0233页
- 【化学】湖北省重点高中协作体20182021-07-0218页
- 2020版高中化学 第2章化学反应为人2021-07-025页
- 2019高中化学 第二章 化学物质及其2021-07-025页
- 高中化学第二章分子结构与性质第二2021-07-026页
- 2019-2020学年新教材高中化学课时2021-07-026页
- 初高中化学衔接7化合价:打开氧化还2021-07-028页
- 2020高中化学专题5生命活动的物质2021-07-028页
- 高中化学第一轮复习专题总结2021-07-0217页
- 2020_2021学年新教材高中化学微专2021-07-025页