- 157.50 KB
- 2021-07-05 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
选择题标准练(十一)
满分:42分
每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列诗句中,加点字(词)所指代物质的主要成分与其他三项不相同的是( A )
A.柳絮飞时花满城 B.朝如青丝暮成雪
C.狐裘不暖锦衾薄 D.春蚕到死丝方尽
解析:A项,柳絮飞时花满城,柳絮主要成分是纤维素,与其他三项不相同,正确;B项,朝如青丝暮成雪,青丝主要成分是蛋白质,错误;C项,狐裘不暖锦衾薄,狐裘主要成分是蛋白质,错误;D项,春蚕到死丝方尽,丝主要成分是蛋白质,错误。
2.莎普爱思的有效成分是由苄达酸与赖氨酸生成的有机盐,苄达酸结构如图所示。下列关于苄达酸的叙述正确的是( B )
A.分子式为C16H16N2O3
B.属于芳香族化合物,且有弱酸性
C.苯环上的一氯代物有5种
D.所有原子可能共平面
解析:A项,根据结构简式可知其分子式为C16H14N2O3,错误;B项,含有苯环属于芳香族化合物,含有羧基,具有弱酸性,正确;C项,分子中有两个苯环,苯环上的氢原子有七种,所以一氯代物有7种,错误;D项,根据甲烷为正四面体结构,分子中含有亚甲基,所有原子不可能共平面,错误。
3.a、b、c、d为原子序数依次增大的短周期不同主族元素,其中只有一种为金属元素,四种元素的单质在通常情况下只有一种不是气体,b与d的最外层电子数之和为a与c最外层电子数之和的四倍。下列叙述不正确的是( B )
A.原子半径:c>d>a
B.d的氧化物对应的水化物酸性均比b的强
C.a、b、d三种元素形成的化合物可能既含离子键又含共价键
D.单质的熔点:c>b>a
5
解析:b与d的最外层电子数之和为a与c最外层电子数之和的四倍,a、b、c、d为原子序数依次增大的短周期不同主族元素,a、b、c、d最外层电子数不同,a与c最外层电子数之和至少为3,b与d的最外层电子数之和至少为12;a、b、c、d中只有一种为金属元素,四种元素的单质在通常情况下只有一种不是气体,短周期主族元素的单质通常情况下呈气态的有H、N、O、F、Cl;代入分析,a为H元素,b为N元素,c为Mg元素,d为Cl元素。A项,根据“层多径大,序大径小”,原子半径:c>d>a,正确;B项,d的氧化物对应的水化物有HClO、HClO2、HClO3、HClO4,b的氧化物对应的水化物有HNO3、HNO2,d的氧化物对应水化物的酸性不一定比b的强,如酸性:HClOb>a,正确。
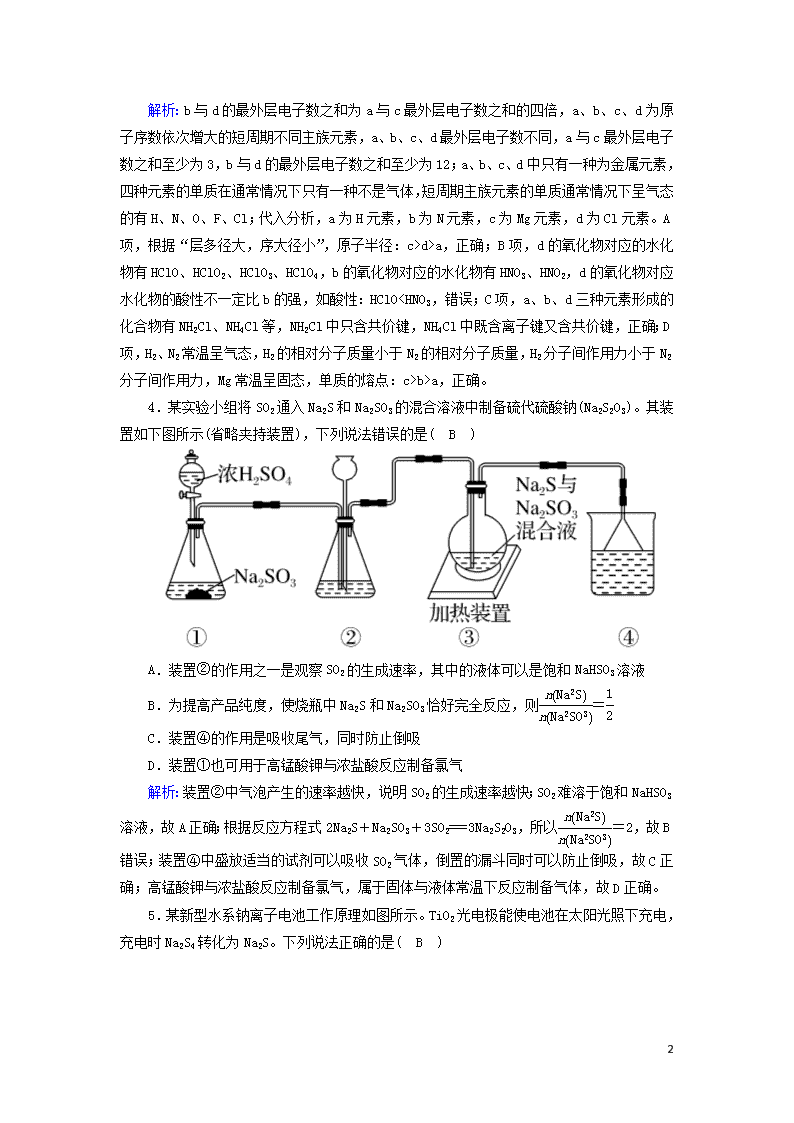
4.某实验小组将SO2通入Na2S和Na2SO3的混合溶液中制备硫代硫酸钠(Na2S2O3)。其装置如下图所示(省略夹持装置),下列说法错误的是( B )
A.装置②的作用之一是观察SO2的生成速率,其中的液体可以是饱和NaHSO3溶液
B.为提高产品纯度,使烧瓶中Na2S和Na2SO3恰好完全反应,则=
C.装置④的作用是吸收尾气,同时防止倒吸
D.装置①也可用于高锰酸钾与浓盐酸反应制备氯气
解析:装置②中气泡产生的速率越快,说明SO2的生成速率越快;SO2难溶于饱和NaHSO3溶液,故A正确;根据反应方程式2Na2S+Na2SO3+3SO2===3Na2S2O3,所以=2,故B错误;装置④中盛放适当的试剂可以吸收SO2气体,倒置的漏斗同时可以防止倒吸,故C正确;高锰酸钾与浓盐酸反应制备氯气,属于固体与液体常温下反应制备气体,故D正确。
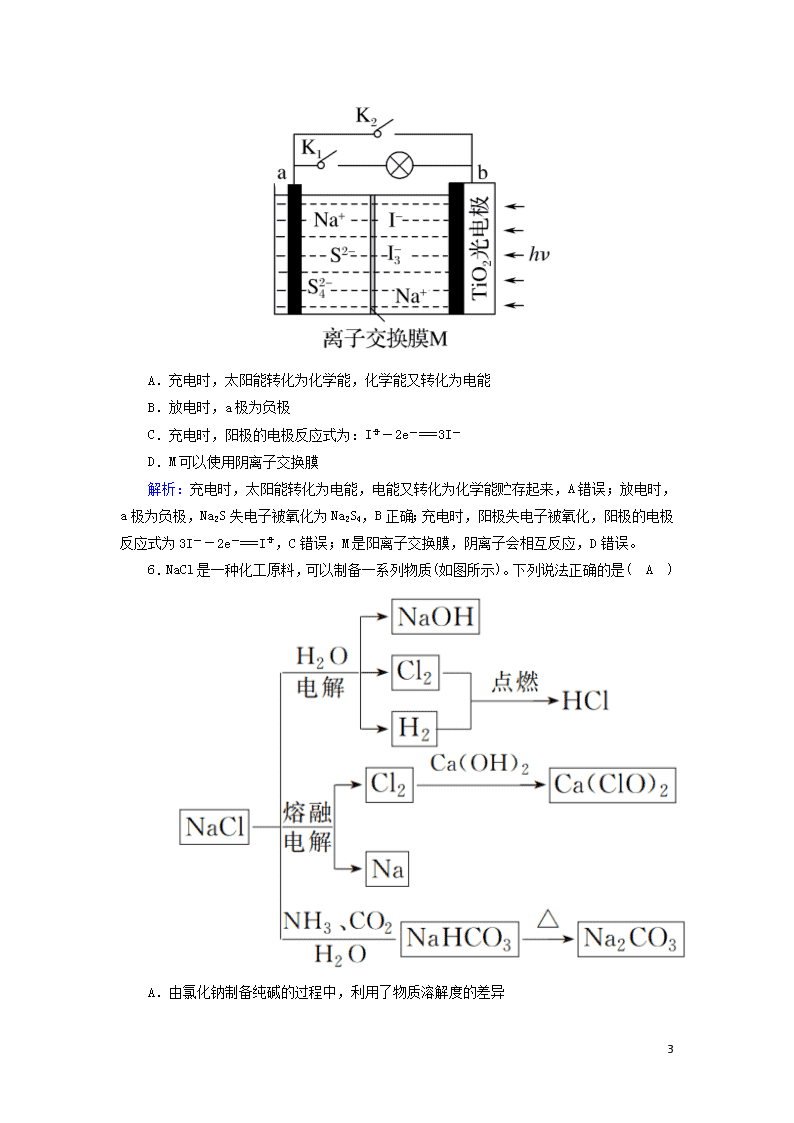
5.某新型水系钠离子电池工作原理如图所示。TiO2光电极能使电池在太阳光照下充电,充电时Na2S4转化为Na2S。下列说法正确的是( B )
5
A.充电时,太阳能转化为化学能,化学能又转化为电能
B.放电时,a极为负极
C.充电时,阳极的电极反应式为:I-2e-===3I-
D.M可以使用阴离子交换膜
解析:充电时,太阳能转化为电能,电能又转化为化学能贮存起来,A错误;放电时,a极为负极,Na2S失电子被氧化为Na2S4,B正确;充电时,阳极失电子被氧化,阳极的电极反应式为3I--2e-===I,C错误;M是阳离子交换膜,阴离子会相互反应,D错误。
6.NaCl是一种化工原料,可以制备一系列物质(如图所示)。下列说法正确的是( A )
A.由氯化钠制备纯碱的过程中,利用了物质溶解度的差异
5
B.用Cl2制备漂白粉时,是将Cl2通入澄清石灰水中
C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应
D.图示转化反应都是氧化还原反应
解析:A项,由氯化钠制备纯碱的过程中,发生的反应为NaCl+CO2+NH3+H2O===NaHCO3↓+NH4Cl,因NaHCO3溶解度最小,在饱和溶液中最先析出,所以利用了物质溶解度的差异,正确;B项,用Cl2制备漂白粉时,是将Cl2通入石灰乳中,澄清石灰水中Ca(OH)2的浓度太小,错误;C项,铁可以在氯气中燃烧,常温下干燥的氯气与铁不反应,错误;D项,图中所示反应有2个不是氧化还原反应:NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl、2NaHCO3Na2CO3+H2O+CO2↑,错误。
7.向10 mL 1 mol·L-1的HCOOH溶液中不断滴加1 mol·L-1的NaOH溶液,并一直保持常温,所加碱的体积与-lg c水(H+)的关系如图所示。c水(H+)为溶液中水电离的c(H+)。下列说法不正确的是( B )
A.常温下,Ka(HCOOH)的数量级为10-4
B.a、b两点pH均为7
C.从a点到b点,水的电离程度先增大后减小
D.混合溶液的导电性逐渐增强
5
解析:A项,甲酸溶液中水电离出的氢离子为10-12 mol·L-1,则溶液中氢离子浓度为0.01 mol·L-1,所以常温下,Ka(HCOOH)=≈10-4,因此数量级为10-4,正确;B项,a点甲酸过量,水电离出的氢离子为10-7 mol·L-1,溶液pH=7;b点氢氧化钠过量,pH>7,错误;C项,从a点到b点,溶液中的溶质由甲酸和甲酸钠变为甲酸钠,然后又变为甲酸钠和氢氧化钠,所以水的电离程度先增大后减小,正确;D项,溶液的导电能力强弱取决于溶液中离子浓度的大小和离子所带电荷的多少,离子浓度越大,离子所带的电荷越多,溶液的导电性越强。甲酸是弱酸,生成的甲酸钠以及氢氧化钠均是强电解质,所以混合溶液的导电性逐渐增强,正确。
5
相关文档
- 2020高考化学冲刺600分选择题标准2021-07-054页
- 2020高考化学冲刺600分选择题标准2021-07-034页
- 2020高考化学冲刺600分选择题标准2021-07-024页
- 2020高考化学二轮复习选择题标准练2021-07-025页
- 2020高考化学二轮复习选择题标准练2021-07-023页
- 2020高考化学冲刺600分选择题标准2021-07-024页
- 2020高考化学二轮复习选择题标准练2021-07-023页
- 浙江省2020高考物理二轮复习非选择2021-06-028页
- 浙江省2020高考物理二轮复习非选择2021-06-028页
- 浙江省2020高考物理二轮复习非选择2021-06-018页