- 143.50 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
1
广西全州县 2016 年春高一化学期中试题(无答案)
(考试时间: 90 分钟;满分: 100 分)
一、选择题(每小题只有一个正确答案,每小题 3 分,共 48 分。)
1.近年来,光化学烟雾污染问题已引起人们的注意,下列哪种气体是造成光化学烟雾的
最主要因素( )。
A.CO B.SO2 C.NO2 D.CH4
2.元素周期表中锶元素的数据见右图。下列说法正确的是( )
A.Sr 元素的质量数就是 87
B.Sr 元素的相对原子质量是 87.62
C.Sr 元素属于非金属元素
D.若 Sr 元素的一种核素核内有 50 个中子,则该核素的符号是 50 38Sr
3.下列化学用语正确的是( )
A.H2S 的电子式:H+[: S
··
··
:]2-H+ B.Ca2+的结构示意图:
C.Na2O 的电子式:Na+
2 [: O
··
··
:]2- D.N2 的电子式:
4.为了更简便地制取干燥的 NH3,下列方法中合适的是( )
A.NH4Cl 与浓 H2SO4 混合共热,生成的气体用碱石灰进行干燥
B.N2 + 3H2 2NH3 ,用烧碱进行干燥
C.加热浓氨水,气体用碱石灰干燥
D.加热 NH4HCO3,气体用 P2O5 干燥
5.在常温下,下列各组气体不能共存的是( )
A.SO2 与 O2 B.NO 与 O2 C.O2 与 N2 D.NO2 与 NO
6.下列物质中只含有共价键的是( )
A.NaCl、HCl、H2O、NaOH B.Cl2、Na2S、HCl、SO2
C.HBr、CO2、H2O、CS2 D.Na2O2、H2O2、H2O、O3
7.在 NO2 被水吸收的反应中,发生还原反应的物质和发生氧化反应的物质的质量比为( )
A.3 : 1 B.1 : 3 C.1 :2 D.2 : 1
8.下列叙述正确的是( )
A.35Cl 与 37Cl 核外电子排布方式不同
B.不同元素的原子构成的分子只含极性共价键
C.235U 和 238U 是中子数不同质子数相同的同种核素
N N
38 Sr
锶 5s2
87.62
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
2
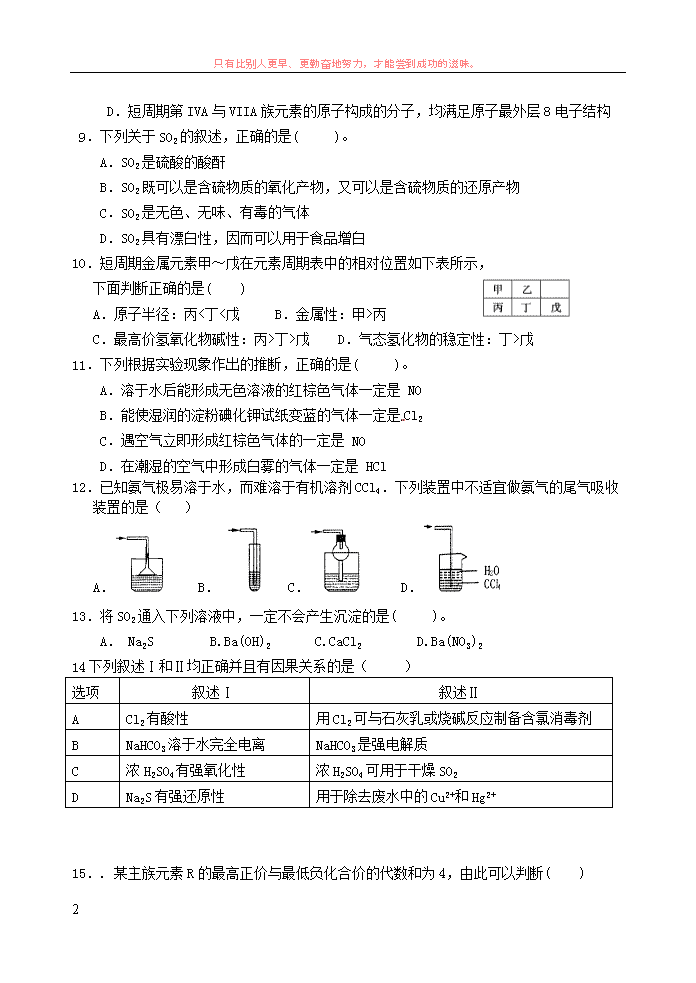
D.短周期第 IVA 与 VIIA 族元素的原子构成的分子,均满足原子最外层 8 电子结构
9.下列关于 SO2 的叙述,正确的是( )。
A.SO2 是硫酸的酸酐
B.SO2 既可以是含硫物质的氧化产物,又可以是含硫物质的还原产物
C.SO2 是无色、无味、有毒的气体
D.SO2 具有漂白性,因而可以用于食品增白
10.短周期金属元素甲~戊在元素周期表中的相对位置如下表所示,
下面判断正确的是( )
A.原子半径:丙<丁<戊 B.金属性:甲>丙
C.最高价氢氧化物碱性:丙>丁>戊 D.气态氢化物的稳定性:丁>戊
11.下列根据实验现象作出的推断,正确的是( )。
A.溶于水后能形成无色溶液的红棕色气体一定是 NO
B.能使湿润的淀粉碘化钾试纸变蓝的气体一定是 Cl2
C.遇空气立即形成红棕色气体的一定是 NO
D.在潮湿的空气中形成白雾的气体一定是 HClK]
12.已知氨气极易溶于水,而难溶于有机溶剂 CCl4.下列装置中不适宜做氨气的尾气吸收
装置的是( )
A. B. C. D.
13.将 SO2 通入下列溶液中,一定不会产生沉淀的是( )。
A. Na2S B.Ba(OH)2 C.CaCl2 D.Ba(NO3)2
14 下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A Cl2 有酸性 用 Cl2 可与石灰乳或烧碱反应制备含氯消毒剂
B NaHCO3 溶于水完全电离 NaHCO3 是强电解质
C 浓 H2SO4 有强氧化性 浓 H2SO4 可用于干燥 SO2
D Na2S 有强还原性 用于除去废水中的 Cu2+和 Hg2+
15.. 某主族元素 R 的最高正价与最低负化合价的代数和为 4,由此可以判断( )
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
3
A.R 一定是第四周期元素
B.R 一定是ⅣA 族元素
C.R 的气态氢化物比同周期其他元素气态氢化物稳定
D.R 气态氢化物化学式为 H2R
16 .6.4g 铜与过量的硝酸(8mol·L﹣1,60mL)充分反应后,硝酸的还原产物有 NO、NO2,
反应后溶液中所含 H+离子为 a mol.此时溶液中所含 NO3
﹣的物质的量为( )
A.(a+0.2)mol B.(a+0.4)mol
C.0.28mol D.0.3lmol
二.非选择题(17、18 小题每空 1 分,其余每空 2 分,共 52 分)
17.将下列性质的序号,填入题后面对应的括号中:
A.脱水性; B.强酸性; C 吸水性 D .强氧化性;
(1)将胆矾放入装有浓 H2SO4 的干燥器中,过一段时间胆矾变白色。_______
(2) 在稀 HNO3 中放入铝片产生 NO。_______
(3)在烧杯中放入蔗糖,滴入浓 H2SO4 变黑,并产生大量气体。_______
(4) 在冷浓 HNO3 中放入铝片没明显现象。_______
18.填写下列空白:
(1)、 碱性:NaOH_____Mg(OH)2 酸性:H2CO3_____ H2SiO4 半径:S2- ____K+
气态氢化物稳定性:HBr_____HCl (填“﹥”或“﹤”)
(2)、写出表示含 8 个质子、10 个中子的原子的化学符号:_______。
(3)、15 号元素位于元素周期表第_____周期_______族。
(4)、短周期元素中最活泼的金属元素是_______。
19.下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用元素符号或化学式等
化学用语回答下列问题:
(1) 元素①的名称是_______,常做半导体材料的是_______。
(2) 元素②、⑥、⑦的原子半径由大到小的顺序是_________________。
(3)写出元素③的最高价氧化物的水化物 (即最高价含氧酸)的化学式:________。
(4)用电子式表示出元素⑤与⑧形成化合
物的过程:_______________________。
(5)元素②的最高正价是_______,它与元
素④按照原子个数比为1:2形成的化合
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
4
物的电子式是______________,该化合物是_________(离子、共价)化合物。
(6)写出元素③的氢化物与元素⑧的氢化物反应的化学方程式:
______________________________________ 。
20. 某研究性学习小组利用固体 Na2SO3 与中等浓度的 H2SO4 反应,制备 SO2 气体并进行有关性
质探究实验。该反应的化学方程式为:Na2SO3(固)+H2SO4=Na2SO4 +H2O+ SO2↑。除固体
Na2SO3 和中等浓度的 H2SO4 外,可供选择的试剂还有:
①溴水 ②浓 H2SO4 ③品红试液 ④紫色石蕊试液 ⑤澄清石灰水 ⑥NaOH 溶液
回答下列问题:
(1)欲验证 SO2 的漂白作用,应将 SO2 气体通入___________中(填物质编号),观察到的
现象是______________________________________
(2)欲验证 SO2 的还原性,应将 SO2 气体通入_____________中(填物质编号),观察到的
现象是______________________________________ ;
(3)为防止多余的 SO2 气体污染环境,应将尾气通入_____________中(填物质编号),
反应离子方程式为______________________________________ 。
21. 非金属单质 A 经如下图所示的过程转化为含氧酸 D,已知 D 为强酸,请回答下列问题:
(1)若 A 在常温下为固体,B 是能使品红溶液褪色的有刺激性气味的无色气体。
① D 的化学式是______
②在工业生产中 B 气体的大量排放被雨水吸收后形成了______而污染环境
(2)若 A 在常温下为气体,C 是红棕色的气体。
①A、C 的化学式分别是:A ______ C ______
②D 的浓溶液在常温下可与铜反应并生成 C 气体,请写出该反应的化学方程式
______________________________________ .
2016 年上学期高一年级期中质量测试
化学科答题卡
只有比别人更早、更勤奋地努力,才能尝到成功的滋味。
5
一、选择题(每小题 3 分,共 48 分。)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
答案
二、非选择题(17、18 题每空 1 分,其余每空 2 分。)
17. (1) _______ (2) _______ (3) _______ (4) _______
18.
(1). _____ ,_____ , ____ , _____ (填“﹥”或“﹤”)
(2)、_______。(3)、第_____周期_______族。(4)、_______。
19
(1) _______, _______。(2) _________________。
(3) ________。(4) _______________________。
(5) _______, ______________, _________
(6)______________________________________ 。
20.
(1)__________, ______________________________________
(2)_____________, _____________________________________ ;
(3)_____________, ______________________________________ 。
21.
(1)① _____,_② ______
(2)① A ______ C ______
②______________________________________ .