- 366.00 KB
- 2021-07-09 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
课题二 乙醇和苯酚的性质
【学考报告】
知识条目
加试要求
①观察液态有机物颜色、状态、气味的方法
②用乙醇和浓硫酸制取乙烯的原理、方法和操作
③乙醇、苯酚分子中羟基的化学活性比较
④盐酸、碳酸、苯酚酸性的比较
⑤用铁离子检验酚类物质
a
b
b
b
a
一、乙醇的性质
1.物理性质
2.化学性质
分子发生反应的部位及反应类型如下:
条件
断键
位置
反应
类型
化学方程式
(以乙醇为例)
Na
①
置换
2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑
HBr,△
②
取代
CH3CH2OH+HBrCH3CH2Br+H2O
O2(Cu),△
①③
氧化
2CH3CH2OH+O22CH3CHO+2H2O
浓硫酸,
170 ℃
②④
消去
CH3CH2OHCH2===CH2↑+H2O
- 7 -
浓硫酸,
140 ℃
①或②
取代
2CH3CH2OHC2H5—O—C2H5+H2O
CH3COOH
(浓硫酸)
①
取代
(酯化)
CH3CH2OH+CH3COOHCH3COOC2H5+H2O
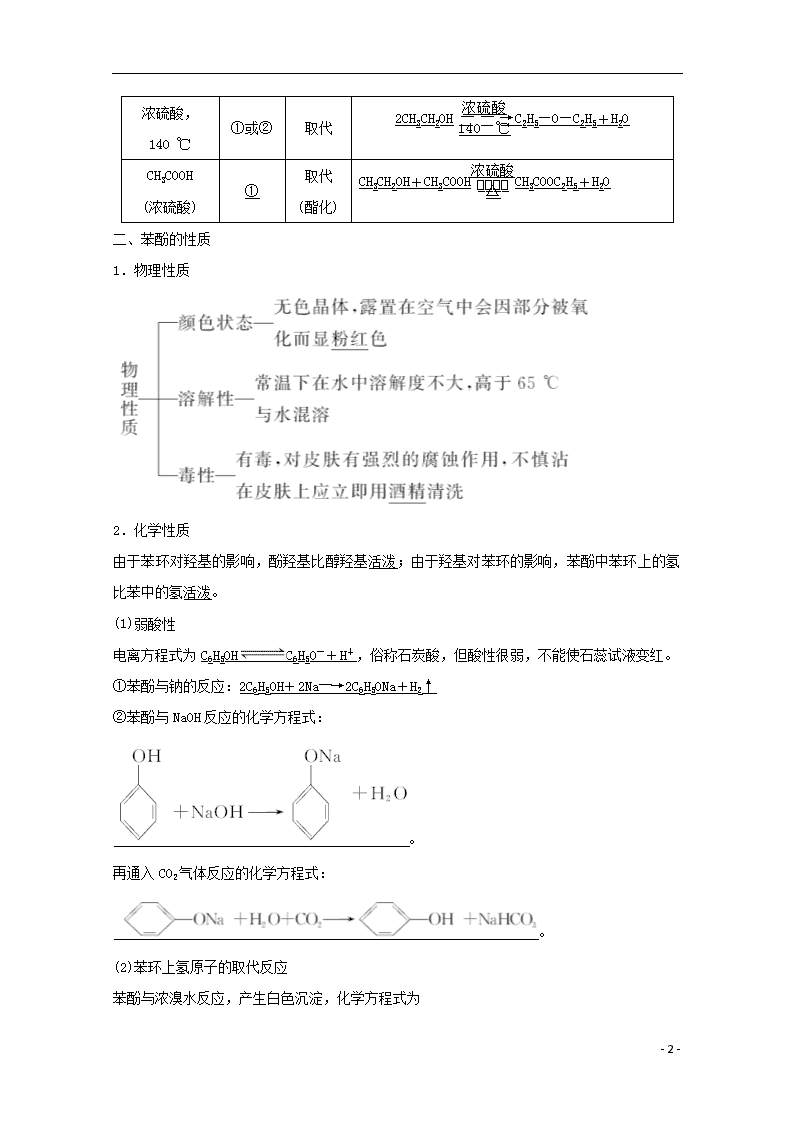
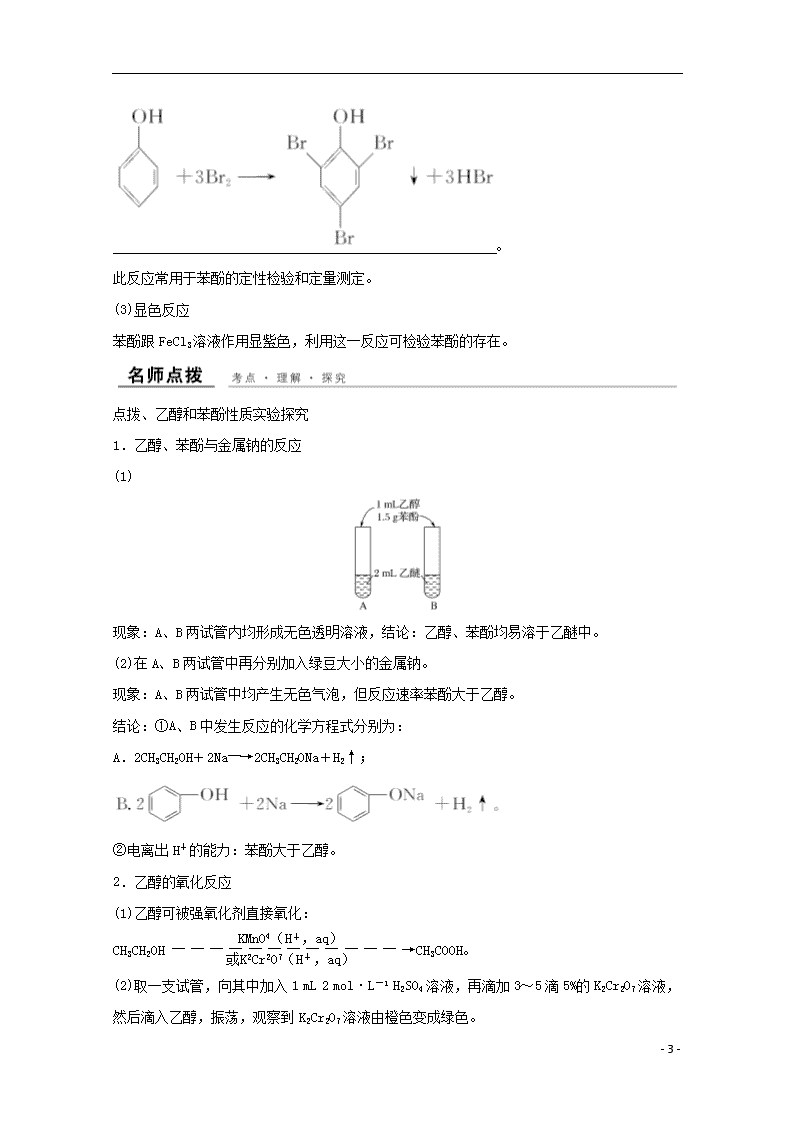
二、苯酚的性质
1.物理性质
2.化学性质
由于苯环对羟基的影响,酚羟基比醇羟基活泼;由于羟基对苯环的影响,苯酚中苯环上的氢比苯中的氢活泼。
(1)弱酸性
电离方程式为C6H5OHC6H5O-+H+,俗称石炭酸,但酸性很弱,不能使石蕊试液变红。
①苯酚与钠的反应:2C6H5OH+2Na―→2C6H5ONa+H2↑
②苯酚与NaOH反应的化学方程式:
。
再通入CO2气体反应的化学方程式:
。
(2)苯环上氢原子的取代反应
苯酚与浓溴水反应,产生白色沉淀,化学方程式为
- 7 -
。
此反应常用于苯酚的定性检验和定量测定。
(3)显色反应
苯酚跟FeCl3溶液作用显紫色,利用这一反应可检验苯酚的存在。
点拨、乙醇和苯酚性质实验探究
1.乙醇、苯酚与金属钠的反应
(1)
现象:A、B两试管内均形成无色透明溶液,结论:乙醇、苯酚均易溶于乙醚中。
(2)在A、B两试管中再分别加入绿豆大小的金属钠。
现象:A、B两试管中均产生无色气泡,但反应速率苯酚大于乙醇。
结论:①A、B中发生反应的化学方程式分别为:
A.2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑;
②电离出H+的能力:苯酚大于乙醇。
2.乙醇的氧化反应
(1)乙醇可被强氧化剂直接氧化:
CH3CH2OHCH3COOH。
(2)取一支试管,向其中加入1 mL 2 mol·L-1 H2SO4溶液,再滴加3~5滴5%的K2Cr2O7溶液,然后滴入乙醇,振荡,观察到K2Cr2O7溶液由橙色变成绿色。
- 7 -
3.乙醇的消去反应
(1)如图所示,在圆底烧瓶中加入4 mL乙醇,边振荡边慢慢加入12 mL浓硫酸,再加入少量沸石。给烧瓶配一个双孔橡胶塞,其中一孔插水银温度计,水银球插入乙醇和浓硫酸的混合液里;另一孔插导管,导管与洗气瓶连接,洗气瓶中盛有2 mol·L-1 NaOH溶液。加热烧瓶,使混合液温度迅速上升到170 ℃,观察到的现象是混合液逐渐变黑色,有气体生成。
(2)将产生的气体通入2 mL溴水中,观察到的现象是溴水褪色。
(3)将产生的气体通入2 mL 0.01 mol·L-1酸性KMnO4溶液中,观察到的现象是溶液紫色褪去。
4.苯酚的物理性质
(1)观察苯酚的颜色、状态,并闻气味,苯酚为无色晶体,有特殊气味。
(2)
5.苯酚的化学性质
(1)检验苯酚是否存在的两个反应分别是与浓溴水反应生成白色沉淀、遇FeCl3溶液显紫色的反应。
(2)苯酚与盐酸、碳酸的酸性强弱的比较:
装置:
现象:A中产生无色气泡,C中溶液变浑浊。
结论:A中反应为
- 7 -
Na2CO3+2HCl===2NaCl+CO2↑+H2O,
C中反应为
6.苯酚与甲醛的反应
(1)合成线型酚醛树脂:取一支试管,加入2.5 g苯酚,2.5 mL 40%甲醛溶液,再加入2 mL浓盐酸,振荡、混匀,塞上带玻璃导管的橡胶塞,置于沸水浴中加热5~8 min。将试管从水浴中取出,并把生成物倒入培养皿中,观察到生成物为白色固体,有的呈粉红色,原因是过量的苯酚被氧化所致。
(2)合成体型酚醛树脂:取一支试管,加入2.5 g苯酚、3.5 mL 40%甲醛溶液,再加入2 mL浓氨水,振荡、混匀,塞上带玻璃导管的橡胶塞,置于沸水浴中加热5~8 min。将试管从水浴中取出,并把生成物倒入培养皿中,观察到生成物为白色固体,有的呈棕黄色,原因是未反应的少量苯酚被氧化所致。
(3)加入酒精,浸泡几分钟,清洗试管。
[典例剖析]
经测定乙醇的分子式是C2H6O,由于有机化合物普遍存在同分异构现象,推测乙醇结构可能是下列两种之一:
为确定其结构,应利用物质的特殊性质进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,甲、乙、丙三名学生直接利用如图给定的装置进行实验确定乙醇的结构。
- 7 -
上图中量气装置是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~200 mL),供量气用;乙管可上下移动,以调节液面高低。
(1)学生甲得到一组实验数据。
乙醇物质的量
氢气的体积(标准状况)
0.010 mol
0.112 L
根据以上数据推断乙醇的结构应为________(用Ⅰ、Ⅱ表示),理由为__________________________________________________________________
______________________________________________________________。
(2)学生乙认为:为了较准确地测量氢气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数、求其差值的过程中,应注意____(填字母)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
(3)学生丙不想通过称取乙醇的质量来确定乙醇的量,那么他还需知道的数据是__________________________________________________________。
解析 (1)Ⅰ式中有一个H原子明显处于与其他H原子不同的位置上,Ⅱ式中则6个H原子处于完全相同的位置。与足量的钠反应,如果是Ⅰ式的话,可能性较大的有4种情况:①6个H原子全反应;②只有5个H原子反应;③只有1个H原子反应;④都不反应。如果是Ⅱ式的话,则只有两种可能:①6个H原子全反应;②都不反应。分析实验数据知,只有1个H原子被置换出来,显然乙醇的结构应为Ⅰ式。(2)在读数时,仰视和俯视都会对读数的准确性造成影响,因而一定要平视;另外,假设甲、乙两管液面不相平的话,就会造成仪器内部的压强与外部大气压不同,造成误差,因而读数时应上下移动乙管,使甲、乙两管液面相平。(3)如果不直接称取乙醇的质量.可以用量筒或其他仪器量出乙醇的体积,然后,用其体积乘以密度,可求算出其质量,进一步可确定其物质的量。
- 7 -
答案 (1)Ⅰ 乙醇和钠反应产生氢气,从量的关系看0.01 mol乙醇产生0.005 mol氢气,说明一个乙醇分子中有一个H原子与其他H原子不同,因此可确定乙醇的分子结构为Ⅰ (2)ac (3)乙醇的密度
[跟踪训练]
已知常温下苯酚微溶于水,溶解度为8.2 g,其饱和溶液的物质的量浓度约为0.8 mol/L。为了探究苯酚和乙醇分子中羟基上氢原子的活泼性,甲、乙两位同学分别设计了如下实验方案:
甲:向两支试管中,分别注入0.8 mol/L的乙醇和苯酚溶液3 mL,各放入一小块金属钠,观察反应产生H2的速率。
乙:在两支试管中,分别放入1 mL乙醇和1 g苯酚晶体,各注入3 mL蒸馏水,振荡,得到乙醇溶液和苯酚浊液,再向两试管中逐滴加入5 mol/L的NaOH溶液,观察其中的变化。
(1)苯酚溶液与钠反应的离子方程式为______________________________
______________________________________________________________。
(2)对于甲、乙两个实验方案,他们能否达到实验目的?理由各是什么?______________________________________________________________
______________________________________________________________。
(3)请你设计一个探究苯酚和乙醇分子中羟基上氢原子活泼性的实验方案。_______________________________________________________________
________________________________________________________________。
答案 (1)2C6H5OH+2Na―→2C6H5O-+2Na++H2↑
(2)甲:不能达到实验目的,因为水的存在使乙醇和苯酚与钠反应的速率难以比较;
乙:不能达到实验目的,因为乙醇溶液与NaOH溶液混合时溶液保持澄清,无法比较
(3)取适量的乙醇和苯酚,分别配制成同物质的量浓度的溶液,测定两溶液的pH,pH小的对应分子中羟基上的氢原子活泼
- 7 -
相关文档
- 高中化学选修5考点9 糖类2021-07-092页
- 高中化学58个精讲23氮和磷2021-07-098页
- 高中化学人教版选修二练习:2_3_1 石2021-07-094页
- 高中化学 2_2《影响化学反应速率的2021-07-0948页
- 2019高中化学 第一章 从实验学化学2021-07-095页
- 高中化学课件必修二《第二章 第二2021-07-0930页
- 高中化学第八章化学与可持续发展第2021-07-095页
- 2020版高中化学 第2章第1节与化学2021-07-0916页
- 2019-2020学年新教材高中化学课时2021-07-095页
- 高中化学必修2同步巩固练习解析:1-32021-07-097页