- 216.27 KB
- 2021-11-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
中考化学总复习
练习题十四
1.在密闭容器中加入甲、乙、丙、丁四种物质,使之充分反应,反应前后测得有关数据如表所示,下列说法中,不正确的是( )
物质
甲
乙
丙
丁
反应前质量/g
18
1
2
32
反应后质量/g
x
26
2
12
A.反应后物质甲的质量为13 g
B.乙是反应物
C.反应中乙、丁的质量比为5:4
D.物质丙可能是该反应的催化剂
2.镁在二氧化碳中燃烧的化学方程式为2Mg+CO22MgO+X,则X的化学式为( )
A.CO
B.C
C.Mg(OH)2
D.MgCO3
3.甲和乙在点燃条件下反应生成丙和丁。反应前后分子变化的微观示意图如下图所示,下列说法中,错误的是( )
A.一个甲分子含有4个原子
B.该反应的基本类型为置换反应
C.4种物质中,属于氧化物的只有甲和乙
D.该反应符合质量守恒定律
4.下列化学方程式书写错误的是( )
A.H2O2H2↑+O2↑
B.C+2CuO2Cu+CO2↑
C.CH4+2O2CO2+2H2O
D.FeCl3+3NaOHFe(OH)3↓+3NaCl
5.15 g不纯的碳酸钙样品与足量的稀盐酸反应,共得到6.95 g二氧化碳气体,则该碳酸钙样品中含有的杂质是下列物质中的( )
A.CaO
B.MgCO3
C.Na2CO3
D.K2CO3
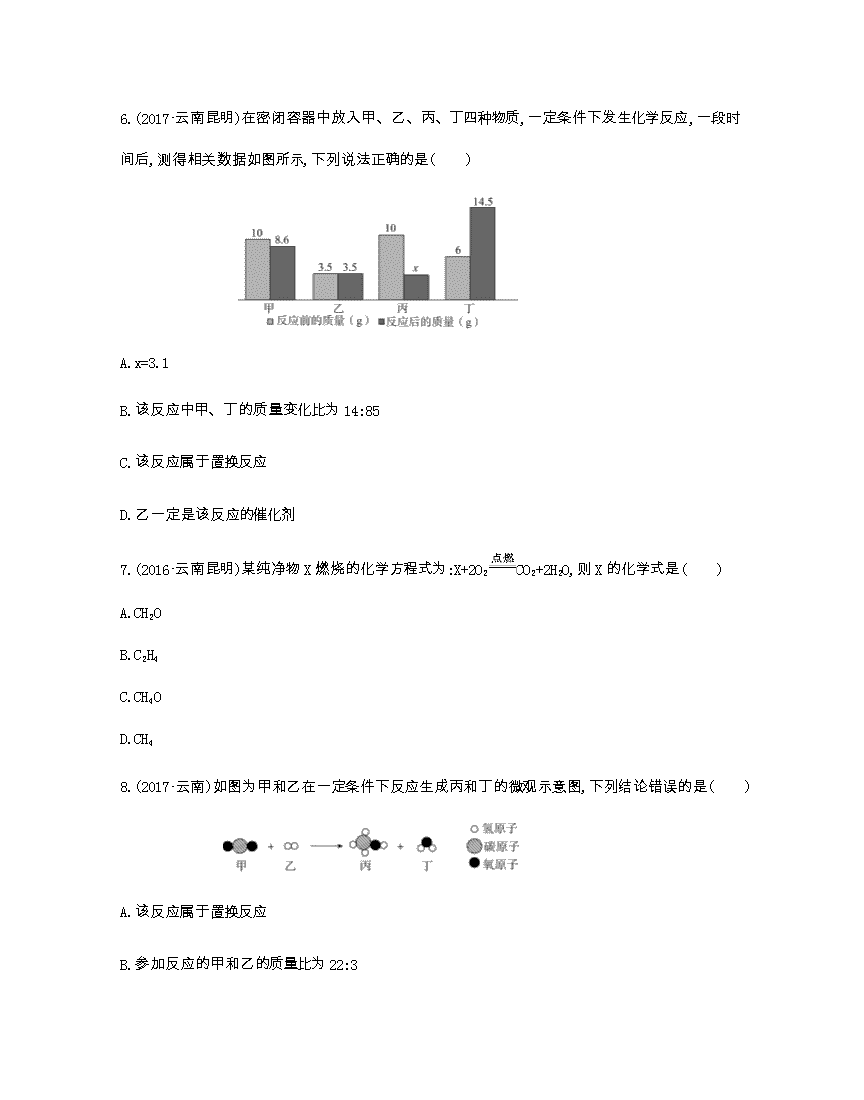
6.(2017·云南昆明)在密闭容器中放入甲、乙、丙、丁四种物质,一定条件下发生化学反应,一段时间后,测得相关数据如图所示,下列说法正确的是( )
A.x=3.1
B.该反应中甲、丁的质量变化比为14:85
C.该反应属于置换反应
D.乙一定是该反应的催化剂
7.(2016·云南昆明)某纯净物X燃烧的化学方程式为:X+2O2CO2+2H2O,则X的化学式是( )
A.CH2O
B.C2H4
C.CH4O
D.CH4
8.(2017·云南)如图为甲和乙在一定条件下反应生成丙和丁的微观示意图,下列结论错误的是( )
A.该反应属于置换反应
B.参加反应的甲和乙的质量比为22:3
C.图中的甲和丁属于氧化物
D.生成的丙和丁的分子个数比为1:1
9.(2017·云南昆明)某反应的微观示意图如图所示,其中“”和“”表示不同元素的原子。下列说法不正确的是( )
A.反应物有4种分子
B.反应前后原子个数不变
C.反应前后元素种类不变
D.化学变化中的最小粒子是原子
10.(2017·云南曲靖)如图所示是处理汽车尾气的某化学反应微观示意图,下列说法错误的是( )
A.该反应属于复分解反应
B.该反应中共涉及三种氧化物
C.反应前后原子的种类和数目都不变
D.该反应的化学方程式为2CO+2NO2CO2+N2
11.(2016·云南昆明)如图为某化学反应的微观示意图,其中相同的球代表同种原子。下列说法正确的是( )
A.反应前后原子种类改变
B.反应前后分子个数不变
C.反应前后元素种类不变
D.分子在化学变化中不可分
12.(2016·云南曲靖)如图所示是某反应前后的微观示意图,“○”和“”表示两种不同的原子,据图分析下列说法正确的是( )
A.该反应是分解反应
B.反应前后分子和原子的种类都发生改变
C.该反应可能为2H2+O2 2H2O
D.该反应的生成物为两种
13.(2016·云南曲靖)下列化学方程式书写正确的是( )
A.CO2+H2O+CaCl22HCl+CaCO3↓
B.2NaCl+MgSO4Na2SO4+MgCl2
C.2HgO2Hg+O2
D.2KOH+CO2K2CO3+H2O
14.(2016·云南昆明)(1)用化学用语填空。
①磷元素: ;
②5个锌原子: ;
③3个二氧化氮分子: ;
④钾离子: ;
⑤三氧化二铝: 。
(2)书写化学方程式:硫在氧气中燃烧: 。
15.(2017·云南)用47.8 g氢氧化钠溶液充分吸收二氧化碳气体,得到50.0 g碳酸钠溶液,请计算:
(1)参加反应的二氧化碳气体的质量是 g。
(2)反应后溶液中溶质的质量分数是多少?(计算结果精确到0.1%)
16.(2017·云南昆明)4 g氧化镁与100 g稀盐酸恰好完全反应。计算该稀盐酸中溶质的质量分数(结果精确到0.1%)。
17.化学反应前后一定不变的是( )
①原子数目
②分子数目
③元素种类
④物质种类
⑤原子种类
⑥反应前后的物质总质量
A.①④⑥
B.①③⑤⑥
C.①②⑥
D.②③⑤
18.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如下图所示,下列说法正确的是( )
A.丙可能是单质
B.在该反应中丁一定没有参加化学反应
C.该反应是置换反应
D.参加反应的甲和乙的质量之和一定等于生成丙的质量
19.化学反应中,反应前后一定发生变化的是( )
A.原子的种类
B.原子的数目
C.分子的种类
D.各物质的总质量
20.如图所示的反应中,甲、乙、丙三种分子的个数比为1:3:2,则从图示中获得的信息正确的是( )
A.生成物一定属于氧化物
B.原子种类在化学反应中发生了变化
C.该反应不可能是分解反应
D.乙分子中A与B的原子个数比为1:2
21.下列化学方程式书写正确的是( )
A.2H2O2H2+O2
B.2Fe+6HCl2FeCl3+3H2↑
C.4P+5O22P2O5
D.CO2+H2OHCO3
22.下列化学方程式符合题意且书写正确的是( )
A.正常雨水的pH约为5.6的原因:CO2+H2OH2CO3
B.医疗上用氢氧化镁中和过多胃酸:Mg(OH)2+HClMgCl2+H2O
C.工业上用高温煅烧石灰石的方法制生石灰:CaCO3CaO+H2O
D.证明铁是金属活动性顺序中氢之前的金属:2Fe+6HCl2FeCl3+3H2↑
23.煤气中加入有特殊臭味的乙硫醇可提示煤气是否泄漏。乙硫醇(C2H6S)燃烧时发生反应的化学方程式为2C2H6S+9O24CO2+2X+6H2O,则X是( )
A.S
B.SO2
C.SO3
D.CO
24.化学方程式S+O2 SO2能提供的信息是( )
A.硫加氧气等于二氧化硫
B.硫元素和氧元素反应生成二氧化硫
C.硫和氧气在点燃的条件下反应生成二氧化硫
D.每32份质量的硫与16份质量的氧气恰好完全反应生成48份质量的二氧化硫
25.将Cu、CuO、Cu(OH)2的混合物12 g加入到稀硫酸中,恰好完全反应后,过滤,得到含硫元素3.2%的溶液50 g和滤渣4 g,则原混合物中Cu元素的质量分数为( )
A.70%
B.60%
C.40%
D.33%
26.现在绿色保健食品风靡全球。山茶油就是其中一种,其主要成分是柠檬醛。现从山茶油中提取7.6 g柠檬醛,使其在氧气中充分燃烧,生成22 g CO2和7.2 g H2O,则柠檬醛中( )
A.只含碳、氢元素
B.一定含碳、氢、氧元素
C.一定含碳、氢元素,可能含氧元素
D.含有的元素无法判断
27.一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下。
物质
A
B
C
D
反应前质量/g
1.7
2.2
7.9
0.9
反应后质量/g
待测
6.6
0
2.7
(1)反应后A的质量为 g。
(2)该反应所属的基本反应类型是 。
28.天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是 ;用肥皂水检验某自来水是硬水还是软水时,发生的化学反应之一为2C17H35COONa+X(C17H35COO)2Ca↓+2NaCl,则X的化学式是 ;漂白粉的主要成分是Ca(ClO)2,是一种常见的泳池消毒剂,在Ca(ClO)2中氯元素的化合价为 价。
29.写出下列反应的化学方程式,并在括号内注明基本反应类型。
(1)铁丝在氧气中燃烧: ,( )反应。
(2)氢氧化钡溶液中加入稀盐酸: ,( )反应。
(3)氨气在氧气中燃烧生成氮气和水: ,( )反应。
30.化学与生产生活息息相关,请运用化学知识回答以下问题。
(1)为了使我们爱吃的酸菜长期保存,一般是将酸菜放在陶罐中,盖上盖后,再在盖的周围放适量的水,这样做的目的是 以防酸菜变质。
(2)工业上用盐酸去铁锈: (用化学方程式表示)。
(3)工业上用磁铁矿石炼铁: (用化学方程式表示)。
(4)用醋酸除水垢(主要成分为CaCO3): (用化学方程式表示)。
(5)硫酸铵不能与熟石灰混合施用,原因是 (用化学方程式表示)。
31.下图所示是初中化学中的一些重要实验。请回答:
(1)A中红磷必须足量的原因是 ;用如图A所示的实验测定空气中氧气的含量,下列对实验的认识中不正确的是 (填字母)。
A红磷燃烧产生大量白色烟雾
B该实验说明氧气难溶于水
C燃烧匙中的红磷可以换成细铁丝
D红磷燃烧结束后,要等装置冷却至室温才能打开弹簧夹
(2)B中玻璃棒的作用是 ;过滤后观察发现,滤液仍然浑浊,可能的原因
是 (答一条即可)。
(3)探究质量守恒定律时,某实验探究小组的同学按上图C所选用的药品和称量方法进行实验,反应停止后,可观察到天平不平衡,该反应 (填“符合”或“不符合”)质量守恒定律,天平不平衡的原因是 。
32.某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些石灰石矿石,准确称取样品10 g放于烧杯中(杂质既不溶于水,也不与稀盐酸反应,也不分解),向其中加入足量的稀盐酸,根据实验测得的数据绘制的图如下。
(1)10 g样品可以产生二氧化碳 g。
(2)该样品中碳酸钙的质量分数是多少?
33.把氯酸钾和二氧化锰的混合物共7 g放在试管中加热,完全反应后,冷却。称得剩余固体5.08 g。求:
(1)根据质量守恒定律计算可制得氧气多少克?
(2)剩余固体中含有什么物质?各多少克?
参考答案
1.B
2.B
3.C
4.A
5.B
6.B
7.D
8.A
9.A
10.A
11.C
12.C
13.D
14.(1)P 5Zn 3NO2 K+ Al2O3
(2)S+O2SO2
15.(1)2.2
(2)解:设反应后溶液中溶质的质量分数为x。
CO2+2NaOHNa2CO3+H2O
44 1062.2 g 50x g
=,解得x=10.6%
答:反应后溶液中溶质的质量分数为10.6%。
16.解:设该稀盐酸中溶质的质量分数为x。
MgO+2HClMgCl2+H2O
40 73
4 g 100x g
=,解得x=7.3%
答:该稀盐酸中溶质的质量分数为7.3%。
17.B
18.D
19.C
20.C
21.C
22.A
23.B
24.C
25.B
26.B
27.(1)3.4
(2)分解反应
28.蒸馏 CaCl2 +1
29.(1)3Fe+2O2Fe3O4 化合
(2)Ba(OH)2+2HClBaCl2+2H2O 复分解
(3)4NH3+3O22N2+6H2O 置换
30.(1)隔绝空气(或氧气)
(2)Fe2O3+6HCl2FeCl3+3H2O
(3)4CO+Fe3O43Fe+4CO2
(4)CaCO3+2CH3COOH(CH3COO)2Ca+CO2↑+H2O
(5)(NH4)2SO4+Ca(OH)2CaSO4+2NH3↑+2H2O
31.(1)消耗完集气瓶中的氧气 AC
(2)引流 滤纸破损(合理即可)
(3)符合 有二氧化碳气体逸散到空气中
32.(1)3.3
(2)解:设该样品中碳酸钙的质量为x。
CaCO3+2HClCaCl2+H2O+CO2↑
100 44
x 3.3 g
=
x=7.5 g
该样品中碳酸钙的质量分数为:×100%=75%
答:样品中碳酸钙的质量分数为75%。
33.解:(1)制得氧气的质量为:7 g-5.08 g=1.92 g
(2)剩余固体中含有氯化钾和二氧化锰两种物质。
设反应后剩余固体中氯化钾的质量为x。
2KClO32KCl+3O2↑
149 96
x 1.92 g
=
解得:x=2.98 g
则二氧化锰的质量为:5.08 g-2.98 g=2.1 g
答:(1)根据质量守恒定律计算可制得氧气1.92 g;
(2)剩余固体中含有氯化钾和二氧化锰两种物质,质量分别为2.98 g和2.1 g。
相关文档
- 2020中考化学复习方案第一篇基础过2021-11-0613页
- 中考数学专题复习练习:旋转2021-11-067页
- 2019九年级化学上册 5化学反应中的2021-11-062页
- 2019年湖南省岳阳市中考化学试卷2021-11-0627页
- 2016届江西省丰城中学九年级上学期2021-11-0611页
- 2018年浙江省衢州市中考数学试卷(2021-11-0616页
- 2019年黑龙江省齐齐哈尔市中考物理2021-11-0627页
- 2019年山东省济南市槐荫区中考历史2021-11-0632页
- 2020年化学精品教学课件十单元复习2021-11-0628页
- 人教版九年级下册数学单元测试题(第2021-11-0616页