- 110.00 KB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
1
第九单元 溶液
课题 2 溶解度(第一课时)
教学目标
通过实验探究,建立饱和溶液与不饱和溶液的概念,了解饱和溶液与不饱和溶液的相互转化的方法,
了解结晶现象。
初步培养活动与探究的一般程序:提出问题→建立假设→设计方案(画出实验简图)→动手实验→
观察记录→分析现象→得出结论。
通过实验条件的改变,让学生感受饱和溶液与不饱和溶液的存在和转化是有条件的,逐步建立用辩
证的、发展的思想观点来看待事物的变化,和逐步培养由具体到一般认识事物过程的能力,并培养学生互
相协作、友好相处的健康心态。
重点和难点
饱和溶液的涵义及“活动与探究”。
实验准备
将全班学生分成若干小组,每小组不超过 5 人。
每组准备器材:烧杯 2 个(各装 20 mL 水)、玻璃棒 1 根、5 g NaCl(预先称好)、5 g KNO3 4 包
(预先称好)、酒精灯、铁架台(带铁圈)、石棉网、火柴、量筒、胶头滴管。
CAI 课件、实物投影仪。
教学设计
教学过程 点评
激趣设境,问题导入
师生互动:俗话说:“饭前喝汤,苗条漂亮;饭后喝汤,肥胖晃晃。”妈妈在家为小槐同学
准备了一碗汤,小槐一尝淡了,要妈妈加 (盐);小槐一尝还说淡了,又要妈妈
加 (盐);小槐一尝还是说淡了,再要妈妈加 (盐)……食盐是我们
熟悉的物质,它是否无限制地溶解在一定量的水中呢?
以俗语作导语,由生
活经验作铺垫,学生
感到自然亲切,着力
创设快乐课堂。
问题探究,得出结论
小组讨论,提出假设。
NaCl 能(不能)无限制溶解在一定量的水中。
阅读 P33,确定方案(画出实验简图)。
投影方案,交流共享。
动手实验,观察记录。
上台展示,投影结论。
①5 g NaCl 能溶解在 20 mL 水中;②10 g NaCl 不能溶解在 20 mL 水中,杯底有少许固体
NaCl。
即 NaCl 不能无限制溶解在一定量水中。
误导结论,延伸探究。
“NaCl 不能无限制溶解在水中”这句话是否正确?教师有意漏读“一定量”三个字,引起
学生质疑猜想。
方案源于教材,形式
却别于教材,更显直
观、生动。
注重交流合作,掌握
直观区分“溶”与
“ 不 溶 ” 的 依 据
──杯底是否有未
溶固体溶质。
通过追究教师“疏
忽”增补方案,动手
实验,使学生关注、
重视“一定量”这
2
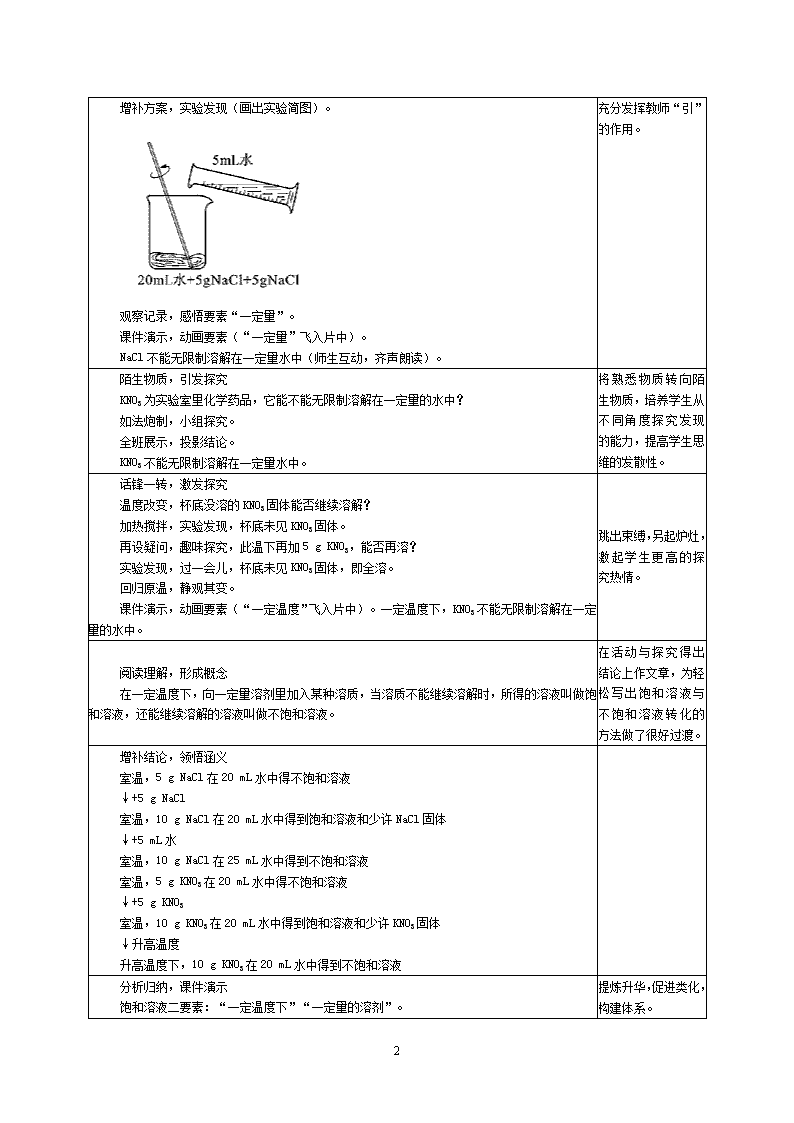
增补方案,实验发现(画出实验简图)。
观察记录,感悟要素“一定量”。
课件演示,动画要素(“一定量”飞入片中)。
NaCl 不能无限制溶解在一定量水中(师生互动,齐声朗读)。
个要素。充分发挥教
师“引”的作用。
陌生物质,引发探究
KNO3 为实验室里化学药品,它能不能无限制溶解在一定量的水中?
如法炮制,小组探究。
全班展示,投影结论。
KNO3 不能无限制溶解在一定量水中。
将熟悉物质转向陌
生物质,培养学生从
不同角度探究发现
的能力,提高学生思
维的发散性。
话锋一转,激发探究
温度改变,杯底没溶的 KNO3 固体能否继续溶解?
加热搅拌,实验发现,杯底未见 KNO3 固体。
再设疑问,趣味探究,此温下再加 5 g KNO3,能否再溶?
实验发现,过一会儿,杯底未见 KNO3 固体,即全溶。
回归原温,静观其变。
课件演示,动画要素(“一定温度”飞入片中)。一定温度下,KNO3 不能无限制溶解在一定
量的水中。
跳出束缚,另起炉
灶,激起学生更高的
探究热情。
阅读理解,形成概念
在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得的溶液叫做饱
和溶液,还能继续溶解的溶液叫做不饱和溶液。
在活动与探究得出
结论上作文章,为轻
松写出饱和溶液与
不饱和溶液转化的
方法做了很好过渡。
增补结论,领悟涵义
室温,5 g NaCl 在 20 mL 水中得不饱和溶液
↓+5 g NaCl
室温,10 g NaCl 在 20 mL 水中得到饱和溶液和少许 NaCl 固体
↓+5 mL 水
室温,10 g NaCl 在 25 mL 水中得到不饱和溶液
室温,5 g KNO3 在 20 mL 水中得不饱和溶液
↓+5 g KNO3
室温,10 g KNO3 在 20 mL 水中得到饱和溶液和少许 KNO3 固体
↓升高温度
升高温度下,10 g KNO3 在 20 mL 水中得到不饱和溶液
分析归纳,课件演示
饱和溶液二要素:“一定温度下”“一定量的溶剂”。
提炼升华,促进类
化,构建体系。
3
深化探究,激活思维
室温下,10 g KNO3 在 20 mL 水中溶液达到饱和,升高温度,杯底 KNO3 固体继续溶解,且又
溶解了 5 g KNO3;冷却到室温,20 mL 水溶解 KNO3 的质量不超过 10 g,此时多余的 KNO3 会怎样?
(观察杯中 KNO3 晶体和课本上图 9-11,阅读感悟,请生上台投影 KNO3 晶体)
探究发现,联想顿悟
观察玻璃片上的白色斑迹。
观察教材上从海水中提取食盐过程图。
联想:炒菜时,菜汤在锅里蒸发,锅底上有白色斑迹;运动出汗衣服上会出现白色斑迹……
学以致用,趣味延伸
练习:教材 P40,习题 1、5、6。
家庭小实验:制取白糖晶体(P39)。
创设新的问题情境,
培养学生求异思维,
提升学生质疑能力。
4
第九单元 溶液
课题 2 溶解度(第二课时)
教学目标
了解固体物质溶解度的涵义。
会利用溶解性表或溶解度曲线,查阅相关物质的溶解性或溶解度,能依据给定的数据绘制溶解度曲
线。
知道影响气体溶解度的一些因素。会利用有关气体溶解度的知识解释身边的一些现象。重点和难点
重点:利用溶解度曲线获得相关信息。
难点:固体物质溶解度的涵义;利用溶解度曲线获得相关信息。
实验准备
投影仪、坐标纸、汽水两瓶、火柴、带导管的橡皮塞、试管、澄清的石灰水。
教学设计
教学过程 点评
教师:我国有许多盐碱湖,湖水中溶有大量的氯化钠和纯碱,那里的农民冬天捞
碱,夏天晒盐,你知道为什么吗?
学生:(议论纷纷)
教师:你可能暂时还不知道为什么。
学习了今天的知识后,你就会从中找到答案。
在前面的活动与探究中,所用的水均为 20 mL,其中溶解 NaCl 与 KNO3 的质量是否
相同?
学生甲:不相同。
乙:不加热时,二者相近。
丙:加热后,等量水中溶解的 KNO3 要多。
教师:大家回答得都很好。我们如何来定量地描述 KNO3 与 NaCl 在水中的溶解性
强弱呢?
学生:溶解度。
教师:这位同学回答得不错。什么叫溶解度呢?请同学们阅读教材。找出溶解度
的概念。
学生:(大声朗读)(教师板书)
溶解度:在一定温度下,某固态物质在 100 g 溶剂(通常溶剂为水)里达到饱和
状态时所溶解的质量。
教师:在教材 P36,表 9-1,给出了几种物质在不同温度时的溶解度,请大家查
一查 20 ℃时 NaCl 的溶解度。
学生甲:(很快找出答案)36.0。
乙:不对,应该是 36.0 g,溶解度有单位,单位是 g。
设置悬念,激发学
生的求知欲。
教师:(表扬乙,肯定甲)乙同学回答得很准确,溶解度有单位。“在 20 ℃时,
NaCl 的溶解度为 36.0 g。”这句话所表达的含义是什么呢?
学生:(踊跃发言)
甲:在 20 ℃时,36.0 gNaCl 在 100 g 水中溶解达到饱和状态。
乙:在 20 ℃时,100 g 水中最多能溶解 36.0 g NaCl。
让学生 体验成功
后的喜悦。
教师:同学们回答得都不错,溶解度的概念包括四个要素:
①指明一定温度;②溶剂为 100 g;③必须达到饱和状态;④单位为 g。
及时小结,纠正偏
差。
学习了溶解度的概念,下面我们一起来做一个练习,相信你会做!
鼓励学 生大胆尝
试。
5
巩固练习(投影)。
查表 9-1,完成下列练习。
1 20 ℃时,KNO3 的溶解度为 ,60 ℃时 KNO3 饱和溶液中,溶质与溶剂
的质量比为 。
2 下列有关 NaCl 的溶解度,说法正确的是( )
A 20 ℃时,18.0 g NaCl 溶解在 50 g 水中达到饱和状态,20 ℃时,NaCl 的溶
解度为 18.0 g。
B 36.0 g NaCl 溶解在 100 g 水中达到饱和状态,NaCl 的溶解度为 36.0 g
C 20 ℃时,36.0 g NaCl 溶解在 100 g 水中,20 ℃时,NaCl 的溶解度为 36.0 g
D 20 ℃时,100 g 水中最多能溶解 36.0 g NaCl,20 ℃时,NaCl 的溶解度为 36.0
g。
(教师巡回指导后,请学生代表说出答案,简单点评)
通过习题,及时巩
固新知。
教师:我们在学习过程中,往往会遇到“易溶”“微溶”“难溶”等一些概念,
它表示什么意思呢?学生通过阅读 P36“资料”寻找答案。
我们知道,影响固体物质溶解度大小的因素主要是温度,同一物质在水中的溶解
度随温度的变化而变化,这种变化关系可以用物质的溶解度曲线来表示。
鼓励学 生自主学
习。
活动与探究:学习绘制物质溶解度曲线的方法。
教师简单介绍方法,学生结合表 9-1 分组绘制 NaCl、KCl、KNO3 的溶解度曲线,
教师巡回指导,然后展示交流,分享快乐,结合学生绘制的溶解度曲线及教材中图 9-12,
分组讨论、交流。
(投影)
①你所绘制的溶解度曲线有何特点,为什么?
②从你绘制的溶解度曲线图上能否找出上述几种物质在 25 ℃、85 ℃时的溶解
度?如果能,请找出,你是怎样查找的?
③从图中,你能比较出 45 ℃时 KCl、KNO3 的溶解度大小吗?
④从溶解度曲线中,你能获得哪些信息?
(学生汇报展示,教师小结归纳)
教师:通过溶解度曲线,可以判断固体物质的溶解度受温度影响的变化情况,可
以比较不同物质在同一温度时溶解度的大小,也可以查出同一种物质在不同温度时的溶
解度。
巩固练习(投影)
亲自动手,自主参
与,乐于探究。
教师:除了固体物质能溶解在水中外,生活中气体溶解在水中的现象也很多,你
能举出一些实例吗?
学生甲:鱼儿能在水中生存,说明水中有 O2。
乙:烧开水时,水未沸腾时也冒气泡。
丙:把汽水瓶打开,有大量气泡产生。
教师:同学们都很善于思考,以上现象均说明了气体能溶解在水中的事实。(展
示两瓶汽水,取其中一瓶不打开,摇晃,然后打开,学生观察现象)
教师:你能观察到什么现象?
学生:不打开时,无明显现象,打开后有大量气泡产生。
教师:为什么打开后产生气泡,而不打开时没有。
学生:打开后,压强减小,CO2 在水中的溶解度减小。
教师:这说明气体的溶解度受压强的影响。压强增大,气体溶解度增大;压强减
小,溶解度减小。
联系生活实际,引
出新知 ,气氛活
跃。
6
刚才一位同学说汽水中冒出的气体为 CO2,你能用实验方法将其检验出来吗?
学生:(上台演示)
教师:(加以肯定,给予激励性评价)烧开水时,水未开时就看到水中冒气泡,
这些气泡是什么?(贴近生活)
学生:水中溶解的空气。
教师:这说明气体的溶解度受温度的影响,温度升高,气体的溶解度变小。
教师小结:气体的溶解度受温度与压强的影响。
教师:我们学习化学知识的目的就是为了利用,解决我们所遇到的一些实际问题。
现在问题来了!
鼓励学 生动手实
践。
巩固练习:(投影)夏天,阵雨来临之前,鱼塘里的鱼常会出现“浮头”现象,
你知道为什么吗?假如你承包了这个鱼塘,你将采取哪些措施?
教师:(肯定学生的种种措施)
整理与归纳:(师生共同进行)
怎样表示固体物质溶解性的大小?如何表示溶解度与温度的关系?通过溶解度
曲线我们可获得哪些信息?影响气体的溶解度的因素有哪些?
课后练习
利用所学,解决问
题,关注生活。
相关文档
- 甘肃省镇原县屯字中学2012-2013学2021-11-108页
- 【沪教版】九年级化学:3-2《组成物2021-11-108页
- 九年级化学(上册)第二单元 我们周2021-11-108页
- 人教版九年级化学下册第9单元实验2021-11-1024页
- 2020学年度初中人教版九年级化学第2021-11-1011页
- 九年级化学下册 课题2 化学元素与2021-11-1021页
- 九年级化学下册第十一单元盐化肥课2021-11-104页
- 【沪教版】九年级化学:7-3《几种重2021-11-104页
- 人教版九年级化学上册第五单元知识2021-11-1017页
- 人教版九年级化学复习课件第11单元2021-11-10118页