- 133.81 KB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第7单元 常见的酸和碱单元测试卷
一.选择题(共20题)
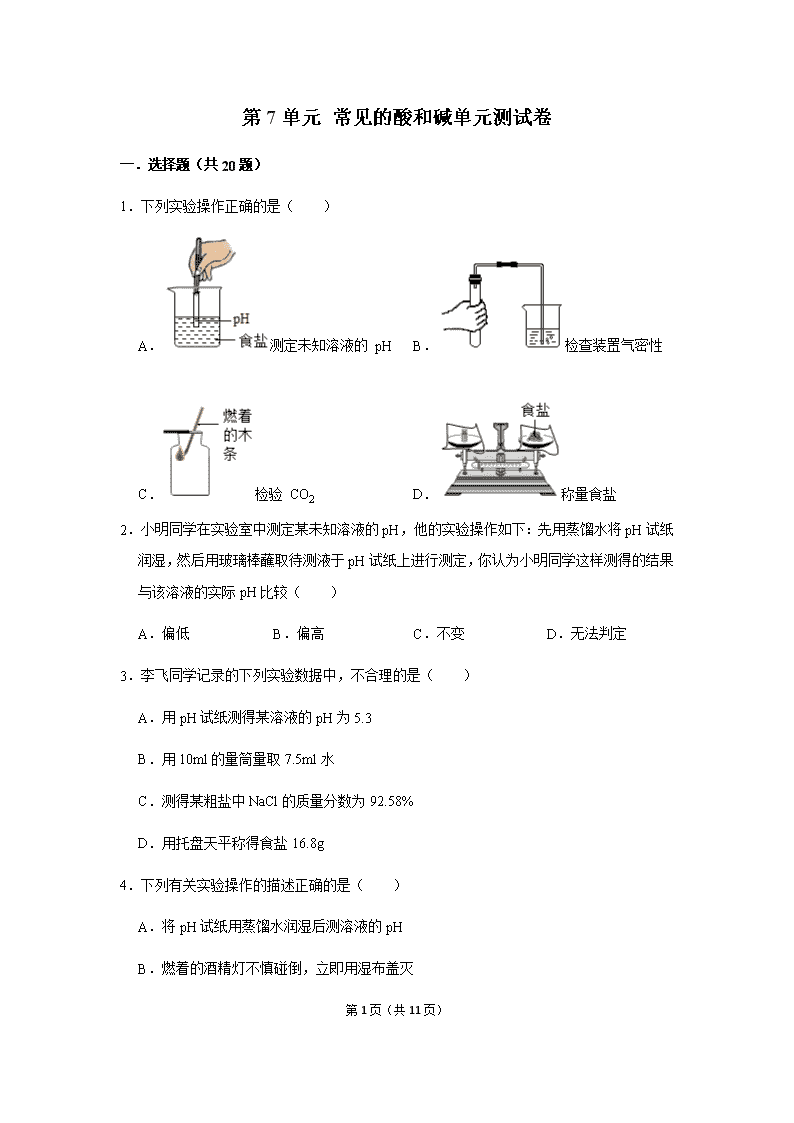
1.下列实验操作正确的是( )
A.测定未知溶液的 pH B.检查装置气密性
C.检验 CO2 D.称量食盐
2.小明同学在实验室中测定某未知溶液的pH,他的实验操作如下:先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取待测液于pH试纸上进行测定,你认为小明同学这样测得的结果与该溶液的实际pH比较( )
A.偏低 B.偏高 C.不变 D.无法判定
3.李飞同学记录的下列实验数据中,不合理的是( )
A.用pH试纸测得某溶液的pH为5.3
B.用10ml的量筒量取7.5ml水
C.测得某粗盐中NaCl的质量分数为92.58%
D.用托盘天平称得食盐16.8g
4.下列有关实验操作的描述正确的是( )
A.将pH试纸用蒸馏水润湿后测溶液的pH
B.燃着的酒精灯不慎碰倒,立即用湿布盖灭
第11页(共11页)
C.实验室中用双氧水制备氧气和用氯酸钾制备氧气,可用同一种装置
D.将氢氧化钠固体直接放在托盘天平的右托盘上称量
5.某化学兴趣小组以“太湖水污染情况调查”为课题进行研究性学习,为了较准地测定湖水样品的酸碱度,可以使用( )
A.紫色石蕊试液 B.无色酚酞试液
C.pH试纸 D.蓝色石蕊试液
6.紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素,花青素遇酸性溶液变红色,遇碱性溶液变蓝色,在凉拌紫甘蓝丝时,观察到菜丝变成红色,可能是加入了下列哪种调味品( )
A.食盐 B.味精 C.食醋 D.香油
7.向某无色溶液中滴入无色酚酞试液后不变色,向该溶液中滴入紫色石蕊试液则( )
A.一定显红色
B.可能仍为紫色,也可能显红色
C.一定显无色
D.可能显蓝色
8.将浓硫酸和浓盐酸分别暴露在空气中,变化的结果是( )
A.溶液的质量都增大
B.溶液的质量都减小
C.溶液中溶质的质量分数都增大
D.溶液中溶质的质量分数都减小
9.下列实验现象描述错误的是( )
A.打开盛有浓盐酸的试剂瓶的瓶盖,瓶口出现白烟
B.将二氧化碳通入紫色石蕊溶液中,溶液变红色
第11页(共11页)
C.硫在氧气中燃烧发出蓝紫色火焰
D.氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀
10.在A+B→盐+水的反应中,A和B不可能是( )
A.HCl和NaOH B.CO2 和NaOH
C.H2SO4和Fe2O3 D.H2SO4 和BaCl2
11.推理是化学学习中常用的思维方法,下推理中正确的是( )
A.酸中都含有氢元素,所以含有氢元素的化合物一定是酸
B.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
C.酸与碱反应有盐和水生成,因此有盐和水生成的反应一定是酸与碱反应
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
12.盐酸能使紫色石蕊试液变红色,这是因为盐酸中含有大量的( )
A.氢原子 B.氢分子 C.氢离子 D.氯离子
13.向盛有一定质量稀硫酸的烧杯中加入过量的锌粉,下列4个图象中,能正确反映对应变化关系的是( )
A. B.
第11页(共11页)
C. D.
14.在农业上常用来改良酸性土壤的物质是( )
A.烧碱 B.石灰石 C.消石灰 D.稀盐酸
15.对于氢氧化钠和氢氧化钙性质叙述错误的是( )
①都是白色固体;
②都易溶于水放出大量的热;
③溶液都能使酚酞试液变红;
④都能与酸发生中和反应;
⑤溶液通入二氧化碳都变浑浊;
⑥与Na2CO3反应都变浑浊.
A.② B.⑤⑥ C.①② D.②⑤⑥
16.向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法不正确的是( )
A.a点溶液中滴入紫色石蕊试液变红
第11页(共11页)
B.bc段(不含b点)反应的化学方程式为MgCl2+2NaOH═Mg(OH)2↓+2NaCl
C.整个变化过程中氯离子数目没有改变
D.d点溶液中含有两种溶质
17.下列图象能正确反映其对应关系的是( )
A.电解水
B.常温下向H2SO4、MgSO4混合溶液中滴加NaOH溶液
C.两份完全相同的双氧水在有无MnO2的情况下产生O2
D.在一定温度下向接近饱和的KNO3溶液中加入KNO3固体
18.实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )
第11页(共11页)
A.该实验是将氢氧化钠滴入盐酸溶液中
B.A点时的溶液能使石蕊试液变红
C.B点表示盐酸和氢氧化钠恰好完全反应
D.C点时,溶液中的溶质只有氯化钠
19.根据下表判断,肉类变质过程中酸碱性的变化趋势是( )
名称
新鲜肉
次鲜肉
变质肉
pH
5.8~6.2
6.3~6.6
>6.7
A.酸性变弱 B.酸性变强 C.酸性不变 D.碱性变弱
20.下表是部分农作物生长对土壤pH的要求.如果某地区经常降酸雨,则该地区最不适合种植的农作物是( )
农作物
大豆
茶
玉米
马铃薯
pH
6.0~7.0
5.0~5.5
7.0~8.1
4.8~5.5
A.大豆 B.茶 C.玉米 D.马铃薯
二.填空题(共5题)
21.某研究小组想探究某一温度下氯化钠饱和溶液的酸碱度。探究过程如下:
【猜想或假设】溶液的pH可能为①pH<7;② ;③ 。
【设计和实验】要测定溶液的酸碱度,除了正确的操作外,其中不能采用下列物质中
第11页(共11页)
的 来进行实验。(填序号)①pH试纸 ②紫色石蕊试液 ③酚酞试液
组内同学进行了如下实验:
甲同学:取pH试纸放在玻璃片上,用玻璃棒蘸取氯化钠溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,测得pH=7。
乙同学:取pH试纸放在玻璃片上,先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取氯化钠溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,测得pH=7。
丙同学:将pH试纸直接浸入氯化钠溶液中,把试纸显示的颜色与标准比色卡比较,测得pH=7。
【评价与反思】三位同学操作正确的是 同学。
指出其余同学的操作错误:
同学; ;
同学; 。
【结论与分析】丙同学得出“凡是盐溶液的pH都等于7”,你认为该同学结论 (填“正确”或“不正确”)。如不正确,请举一例说明 。
22.如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同。结合此图回答下列问题:
(1)稀硫酸中阳离子的符号是 ;
(2)反应①中石蕊溶液变为 色;
(3)反应⑤的化学方程式为 ;
(4)图中只生成盐和水的反应有 (填序号);
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、Na2CO3)中的 。
第11页(共11页)
23.甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如图所示的四组实验方案。
(1)其中能达到实验目的是
(2)在C组实验中发生的化学方程式为
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有 物质生成(填化学式),滴入酚酞后溶液呈红色。
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性。使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和 三种物质中的一种,或是三种物质两两混合组成的混合物。
(5)为了验证推测,甲同学查阅资料,获悉氯化钡溶液呈中性,并设计如下实验加以验证。请根据要求完成下列空白:
实验内容
预测现象
结论
①若有白色沉淀,溶液呈无色
物质是碳酸钠
第11页(共11页)
取少量容器中的上层溶液于试管中,加入过量的氯化钡溶液,静置
②若无沉淀生成,溶液呈红色
物质是氢氧化钙
③若有白色沉淀,溶液呈红色
(6)乙同学认为甲同学第②步验证的结论不严密,原因是 。
24.在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示。该反应的化学方程式为: ;该实验操作是将 滴加到另一种溶液 中。当加入溶液的质量为ag时,证明此时溶液呈 。性。所得溶液中的溶质为(写化学式) 。当加入溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈 色;此时溶液里所含有的溶质有(写化学式) 。
25.化学就在我们身边,从①H2SO4、②Ca(OH)2、③NaCl、④CaCO3、⑤CH4五种物质中学出与下列用途对应物质的序号填写在空白处:
欲除去溶液中含有的少量盐酸,在不用酸碱指示剂的条件下应加入的试剂是 .
三.实验探究题(共1题)
26.小红同学进行酸碱中和反应的实验(如图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液颜色没有变化。于是她对烧杯中的溶液进行了以下探究:
(1)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸过量。
小明同学却断定不可能“氢氧化钠有剩余”,他的理由是: ;
第11页(共11页)
(2)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写如表:
试验方法
可能观察到的现象
结论
将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中。
如果
则盐酸过量
如果
则盐酸与氢氧化钠恰好完全反应
(3)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的。你认为其中不正确的是 (填序号)。
A.生锈的铁钉 B.碳酸钠粉末 C.硫酸钠粉末 D.氢氧化铜
(4)如图曲线能够表示小红所做试验中溶液pH变化趋势的是 (填序号)。
四.解答题(共2小题)
27.某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A﹣H编号后,做如下实验。
第11页(共11页)
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 。
(2)写出实验中无明显现象产生的试管中发生的化学方程式 。
(3)实验后某试管中为红色溶液,当向其中加入过量的 后,溶液变为蓝色。由此推断,该试管中最初盛有的物质是 。
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是 。
28.已知,在水溶液中,乙醇(C2H5OH)不发生电离;溴化氢(HBr)电离产生氢离子(H+)和溴离子(Br﹣);氢氧化钠电离产生钠离子和氢氧根离子。请回答下列问题:
(1)根据这三种溶液的组成推断,医用酒精(含乙醇75%的水溶液)显 性,溴化氢的水溶液显 性。
(2)写出上述物质之间发生中和反应的化学方程式 。
(3)氢氧化钠溶液中存在的微粒有(用化学符号表示) 。
第11页(共11页)