- 249.64 KB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
初中化学·人教版·九年级下册——第十一单元 盐 化肥
第十一单元 盐 化肥
课题 1 生活中常见的盐
第 1 课时 常见的盐
测试时间:25 分钟
一、选择题
1.碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一,它的俗名是( )
A.小苏打 B.苛性钠 C.烧碱 D.苏打
2.(2019 云南大理二模)在蔬菜生长的过程中,常喷洒农药防治病虫害。据有关专家介绍,用碱性溶液
或清水浸泡,可使残留在蔬菜上的农药的毒性降低。浸泡买来的蔬菜时可以加入适量的( )
A.纯碱 B.白酒 C.烧碱 D.食醋
3.某同学将维生素 C 泡腾片放入水中,观察到有大量气泡冒出,根据泡腾片主要成分分析,该气体主要
是( )
A.O2 B.N2 C.CO2 D.水蒸气
4.现有下列试剂供选择:①石灰水、②食醋、③食盐水、④纯碱溶液、⑤烧碱溶液。为了检验贝壳的
主要成分是碳酸盐,应该用到的试剂是( )
A.①② B.①③ C.②⑤ D.③④
5.我国制碱工业的先驱——侯德榜先生,1921 年留美回国后,潜心研究制碱技术,发明了将制碱与制氨
结合起来的联合制碱法(又称侯氏制碱法),为纯碱和氮肥工业技术的发展做出了杰出贡献。 下列物质
中能与纯碱发生反应的是( )
A.NaOH B.NaHCO3 C.H2SO4 D.K2SO4
6.(2019 山东淄博博山一模)下列关于酸、碱、盐的用途不合理的是( )
A.用盐酸除铁锈
B.用氢氧化钠改良酸性土壤
C.用硫酸铜溶液与石灰乳混合配制农药波尔多液
D.用小苏打治疗胃酸过多
7.碳酸钠俗称“纯碱”。有关它的表述不正确的是( )
A.“纯碱”其实不是碱,它属于盐类
B.可用纯碱代替洗涤灵洗涤餐具表面的油污
C.用纯碱可除去面团发酵产生的酸
D.“冬天捞碱”可说明纯碱的溶解度受温度变化影响不大
8.(2019 山东济南历下三模)已知粉末 X 样品是下列四种物质中的一种,取三等份该粉末,分别加入足
量的氢氧化钙溶液、氯化钡溶液、稀盐酸中并振荡,产生的现象如下表。则该固体粉末 X 是( )
加入物质 氢氧化钙溶液 氯化钡溶液 稀盐酸
现象 产生白色沉淀 产生白色沉淀 固体溶解,产生无色气体
A.CuSO4 B.Na2SO4 C.K2CO3 D.Mg
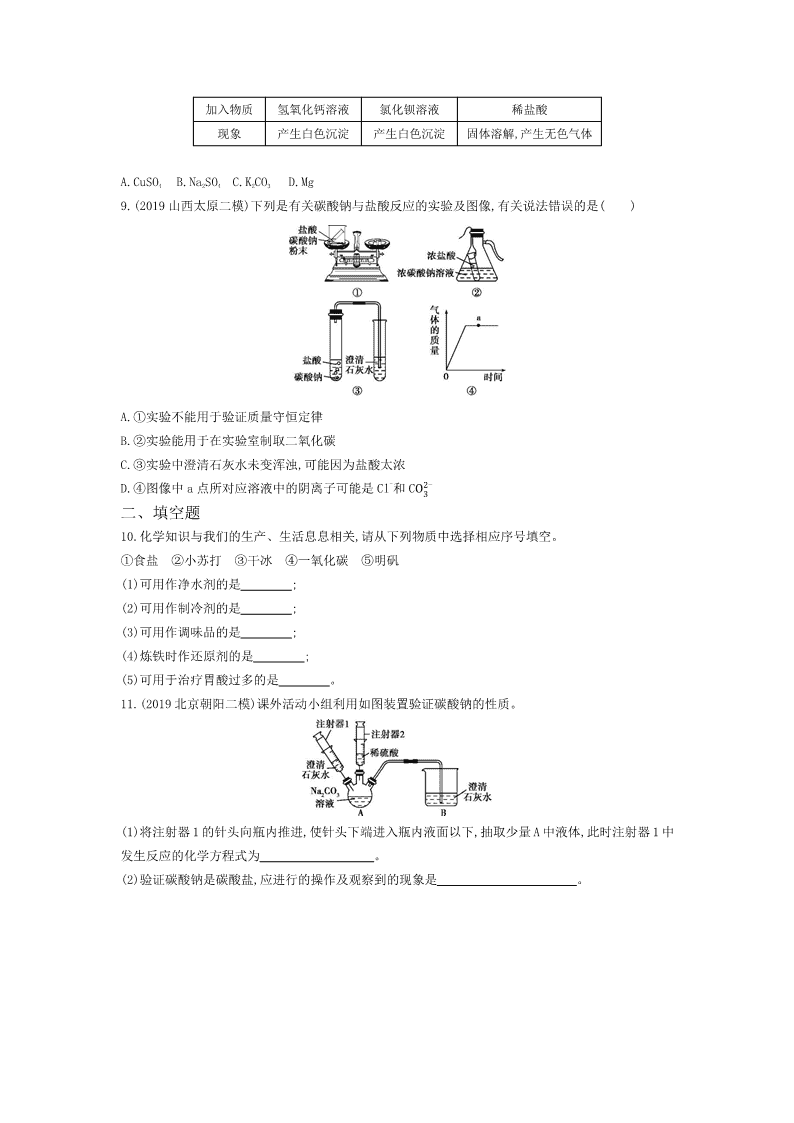
9.(2019 山西太原二模)下列是有关碳酸钠与盐酸反应的实验及图像,有关说法错误的是( )
A.①实验不能用于验证质量守恒定律
B.②实验能用于在实验室制取二氧化碳
C.③实验中澄清石灰水未变浑浊,可能因为盐酸太浓
D.④图像中 a 点所对应溶液中的阴离子可能是 Cl-和 C
O3
2
-
二、填空题
10.化学知识与我们的生产、生活息息相关,请从下列物质中选择相应序号填空。
①食盐 ②小苏打 ③干冰 ④一氧化碳 ⑤明矾
(1)可用作净水剂的是 ;
(2)可用作制冷剂的是 ;
(3)可用作调味品的是 ;
(4)炼铁时作还原剂的是 ;
(5)可用于治疗胃酸过多的是 。
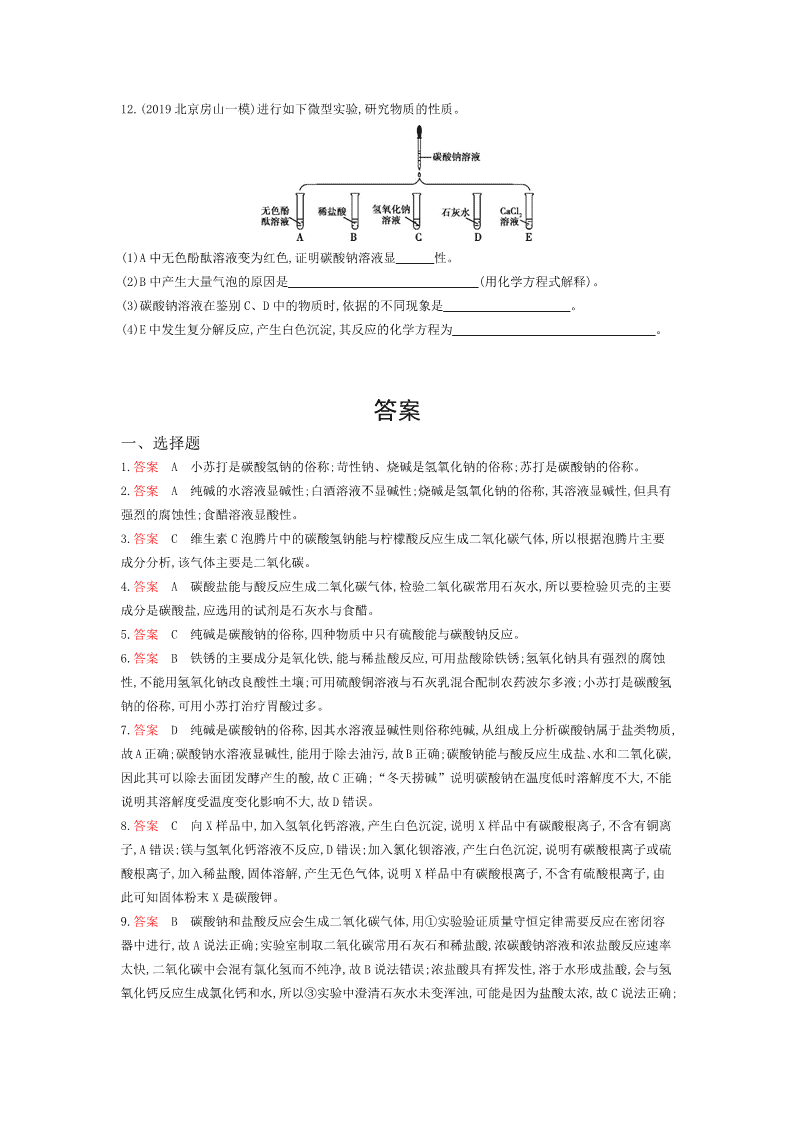
11.(2019 北京朝阳二模)课外活动小组利用如图装置验证碳酸钠的性质。
(1)将注射器 1 的针头向瓶内推进,使针头下端进入瓶内液面以下,抽取少量 A 中液体,此时注射器 1 中
发生反应的化学方程式为 。
(2)验证碳酸钠是碳酸盐,应进行的操作及观察到的现象是 。
12.(2019 北京房山一模)进行如下微型实验,研究物质的性质。
(1)A 中无色酚酞溶液变为红色,证明碳酸钠溶液显 性。
(2)B 中产生大量气泡的原因是 (用化学方程式解释)。
(3)碳酸钠溶液在鉴别 C、D 中的物质时,依据的不同现象是 。
(4)E 中发生复分解反应,产生白色沉淀,其反应的化学方程为 。
答案
一、选择题
1.答案 A 小苏打是碳酸氢钠的俗称;苛性钠、烧碱是氢氧化钠的俗称;苏打是碳酸钠的俗称。
2.答案 A 纯碱的水溶液显碱性;白酒溶液不显碱性;烧碱是氢氧化钠的俗称,其溶液显碱性,但具有
强烈的腐蚀性;食醋溶液显酸性。
3.答案 C 维生素 C 泡腾片中的碳酸氢钠能与柠檬酸反应生成二氧化碳气体,所以根据泡腾片主要
成分分析,该气体主要是二氧化碳。
4.答案 A 碳酸盐能与酸反应生成二氧化碳气体,检验二氧化碳常用石灰水,所以要检验贝壳的主要
成分是碳酸盐,应选用的试剂是石灰水与食醋。
5.答案 C 纯碱是碳酸钠的俗称,四种物质中只有硫酸能与碳酸钠反应。
6.答案 B 铁锈的主要成分是氧化铁,能与稀盐酸反应,可用盐酸除铁锈;氢氧化钠具有强烈的腐蚀
性,不能用氢氧化钠改良酸性土壤;可用硫酸铜溶液与石灰乳混合配制农药波尔多液;小苏打是碳酸氢
钠的俗称,可用小苏打治疗胃酸过多。
7.答案 D 纯碱是碳酸钠的俗称,因其水溶液显碱性则俗称纯碱,从组成上分析碳酸钠属于盐类物质,
故 A 正确;碳酸钠水溶液显碱性,能用于除去油污,故 B 正确;碳酸钠能与酸反应生成盐、水和二氧化碳,
因此其可以除去面团发酵产生的酸,故 C 正确;“冬天捞碱”说明碳酸钠在温度低时溶解度不大,不能
说明其溶解度受温度变化影响不大,故 D 错误。
8.答案 C 向 X 样品中,加入氢氧化钙溶液,产生白色沉淀,说明 X 样品中有碳酸根离子,不含有铜离
子,A 错误;镁与氢氧化钙溶液不反应,D 错误;加入氯化钡溶液,产生白色沉淀,说明有碳酸根离子或硫
酸根离子,加入稀盐酸,固体溶解,产生无色气体,说明 X 样品中有碳酸根离子,不含有硫酸根离子,由
此可知固体粉末 X 是碳酸钾。
9.答案 B 碳酸钠和盐酸反应会生成二氧化碳气体,用①实验验证质量守恒定律需要反应在密闭容
器中进行,故 A 说法正确;实验室制取二氧化碳常用石灰石和稀盐酸,浓碳酸钠溶液和浓盐酸反应速率
太快,二氧化碳中会混有氯化氢而不纯净,故 B 说法错误;浓盐酸具有挥发性,溶于水形成盐酸,会与氢
氧化钙反应生成氯化钙和水,所以③实验中澄清石灰水未变浑浊,可能是因为盐酸太浓,故 C 说法正确;
随着碳酸钠和盐酸反应的进行,生成二氧化碳质量逐渐增大,横坐标表示反应时间,a 点可能表示加入
的盐酸不足,碳酸钠没有完全反应,此时其中的阴离子为 Cl-和 C
O3
2
-,故 D 说法正确。
二、填空题
10.答案 (1)⑤ (2)③ (3)① (4)④ (5)②
解析 (1)明矾溶于水形成的胶状物质具有吸附性,能吸附水中的悬浮杂质,从而达到净水的目的;(2)
干冰是固态的二氧化碳,可用作制冷剂;(3)食盐是食物调味剂中不可缺少的物质,能增加食物的咸
味;(4)一氧化碳具有还原性,可以将氧化铁还原成铁单质;(5)小苏打是碳酸氢钠,其能与胃液中的盐
酸反应,可用于治疗胃酸过多。
11.答案 (1)Na2CO3+Ca(OH)2 2NaOH+CaCO3↓ (2)将注射器 2 中的稀硫酸推入瓶中,A 中有气泡产
生,B 中澄清石灰水变浑浊
解析 (1)将注射器 1 的针头向瓶内推进,使针头下端进入瓶内液面以下,抽取少量 A 中液体,此时注射
器 1 中碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠。(2)碳酸盐能与酸反应生成能使澄清石灰
水变浑浊的二氧化碳气体,检验碳酸盐最简单的方法是滴加酸,观察是否有能使澄清石灰水变浑浊的
气体产生,则验证碳酸钠是碳酸盐,将注射器 2 中的稀硫酸推入瓶中,A 中有气泡产生,B 中澄清石灰水
变浑浊,即可证明。
12.答案 (1)碱 (2)Na2CO3+2HCl 2NaCl+H2O+CO2↑ (3)C 中无明显现象,D 中出现白色沉淀
(4)Na2CO3+CaCl2 2NaCl+CaCO3↓
解析 (1)酚酞溶液遇碱性物质变红色,A 中无色酚酞溶液变为红色,证明碳酸钠溶液显碱性;(2)向稀
盐酸中滴加碳酸钠溶液,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;(3)氢氧化钠中加入碳酸钠
溶液不反应,无明显现象,石灰水中加入碳酸钠溶液,碳酸钠和氢氧化钙反应生成碳酸钙白色沉淀;
(4)氯化钙中加入碳酸钠,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠。
相关文档
- 九年级化学下册第十一单元盐化肥课2021-11-106页
- 人教版化学九年级下册第11单元盐化2021-11-106页
- 新课标RJ2020中考化学复习方案主题2021-11-1047页
- 九年级化学下册第十一单元盐化肥课2021-11-104页
- 人教版九年级化学下册盐化肥单元测2021-11-105页
- 九年级化学下册第十一单元盐化肥课2021-11-108页
- 九年级化学下册第十一单元盐化肥课2021-11-105页
- 河北专版2020中考化学复习方案主题2021-11-1047页
- 九年级化学下册[人教版]第11单元盐2021-11-109页
- 人教版化学九年级下册第11单元《盐2021-11-107页