- 302.50 KB
- 2021-11-11 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
1
专题三 身边的化学物质
一、气体的制取、收集和除杂
1.发生装置的选择
(1)选择原则
①反应物的状态;②反应是否需要条件。
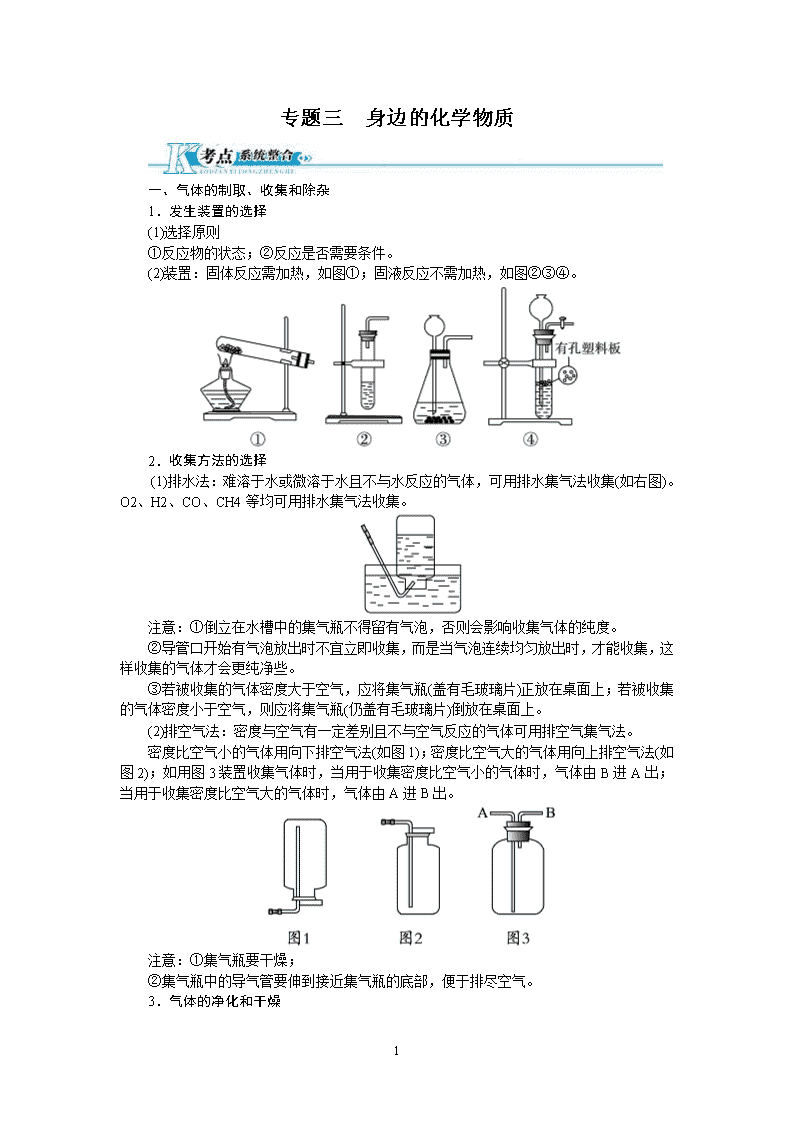
(2)装置:固体反应需加热,如图①;固液反应不需加热,如图②③④。
2.收集方法的选择
(1)排水法:难溶于水或微溶于水且不与水反应的气体,可用排水集气法收集(如右图)。
O2、H2、CO、CH4等均可用排水集气法收集。
注意:①倒立在水槽中的集气瓶不得留有气泡,否则会影响收集气体的纯度。
②导管口开始有气泡放出时不宜立即收集,而是当气泡连续均匀放出时,才能收集,这
样收集的气体才会更纯净些。
③若被收集的气体密度大于空气,应将集气瓶(盖有毛玻璃片)正放在桌面上;若被收集
的气体密度小于空气,则应将集气瓶(仍盖有毛玻璃片)倒放在桌面上。
(2)排空气法:密度与空气有一定差别且不与空气反应的气体可用排空气集气法。
密度比空气小的气体用向下排空气法(如图 1);密度比空气大的气体用向上排空气法(如
图 2);如用图 3装置收集气体时,当用于收集密度比空气小的气体时,气体由 B进 A出;
当用于收集密度比空气大的气体时,气体由 A进 B出。
注意:①集气瓶要干燥;
②集气瓶中的导气管要伸到接近集气瓶的底部,便于排尽空气。
3.气体的净化和干燥
2
(1)实验装置
(2)气体的干燥
选用干燥剂应根据气体的性质和干燥剂的性质而定,其原则是干燥剂只能吸收气体中的
水分,而不能与气体发生反应。如下表中常见气体的干燥剂:
干燥剂 可干燥的气体 不能干燥的气体
浓硫酸
H2、O2、CO、HCl等中性、
酸性气体
不能干燥碱性气体,如 NH3
无水硫酸铜
(CuSO4)、无水氯化
钙(CaCl2)
H2、O2、CO、CO2、HCl 无水氯化钙不能干燥 NH3
氢氧化钠固体或生
石灰或碱石灰
H2、O2、CO、NH3等中性、
碱性气体
不能干燥酸性气体,如 CO2、
SO2、HCl、H2S等
(3)气体的净化
选择气体吸收剂应根据气体的性质和要除去杂质的性质而定。
原则:①所用的吸收剂只能吸收气体中的杂质;②不能与被提纯的气体反应,也不能引
入新的杂质。
常见的气体及其吸收剂:
水蒸气:吸收剂为浓硫酸、无水硫酸铜、氢氧化钠固体、碱石灰(氢氧化钠与生石灰的
混合物)等。
HCl:吸收剂为氢氧化钠溶液、碱石灰等。
CO2:吸收剂为氢氧化钠溶液、澄清石灰水、碱石灰等。
气体的净化顺序:先除杂,后干燥;加热之前先除去水。
二、常见物质间的转化
1.CO2的重要性
围绕 CO2展开的一系列转化反应
2.金属及碱的重要性
(1)
3
(2)
3.盐的重要性
酸、碱、盐以及单质、氧化物的化学性质均与盐有密切的联系,盐将这些物质联系在一
起。
三、空气和水
空气是一种混合物,其组成是通过测定空气中各成分的体积分数来表示的,但各成分的
体积分数是相对的,并不是固定不变的。空气中氧气含量的测定方法很多,但原理基本是一
样的,即一般是先把氧气消耗掉,而后利用压强和体积的变化来确定。所以,在选择燃烧物
时一般选用红磷;不选用铁丝是因为铁丝在空气中不能燃烧;不选用硫或碳是因为硫或碳
燃烧后有二氧化硫、二氧化碳气体生成,如选用硫或碳,则瓶内可放一些 NaOH溶液来吸
收生成的气体。对实验误差的分析应重点放在燃烧物的用量(要充分消耗氧气)、装置的气密
性(装置气密性要好)、记录实验数据的时间(温度冷却到常温下)等。
四、溶液
1.溶液是均一、稳定的混合物。判断某物质是否是溶液,一般看以下两点:是否具有
均一、稳定的性质;是否是一种混合物。溶液是澄清、透明的,但不一定是无色的。当溶液
中有水存在时,不论水的量有多少,习惯上把水看做是溶剂,而且通常不指明溶剂的某溶液,
一般指的是其水溶液。
2.饱和溶液与不饱和溶液只有在“一定温度下”和“一定量的溶剂里”才有确定的意
义。在改变溶剂或温度的情况下,饱和溶液与不饱和溶液可以进行相互转化。溶液的饱和、
不饱和与浓、稀之间无必然联系,即饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶
液;但对于同一温度下、同一溶质的溶液,其饱和溶液溶质的质量分数比其不饱和溶液溶质
的质量分数大。
3.溶解度曲线的应用:①可以查出某种物质在某温度下的溶解度;②可以确定温度对
溶解度的影响状况;③可以比较不同物质在不同温度下的溶解度大小;④可以确定怎样制得
某温度时该物质的饱和溶液等。
五、溶液的酸碱性
1.溶液的酸碱性指的是溶液呈酸性、碱性还是中性,通常用酸碱指示剂来测定(定性)。
溶液的酸碱度是指溶液酸碱性的强弱程度,常用 pH表示(定量),测定 pH最简单的方法是
使用 pH试纸。
2.酸具有相似化学性质的原因是溶液中都含有 H+
;碱具有相似化学性质的原因是溶液
中都含有 OH-
。
4
3.NaOH和 Ca(OH)2同属碱类物质,由于金属阳离子不同,因而有各自的不同特性,
如 NaOH易溶于水,而 Ca(OH)2微溶于水。因此,要充分吸收混合气体中的 CO2应选用 NaOH
溶液,检验 CO2的存在时应选用 Ca(OH)2溶液。
4.“酸、碱、盐”这部分知识是初中化学的重点内容,其知识点多而琐碎。要想扎实
地学好这部分知识,就要认真分析、归纳好其中的重要知识点:会用酸碱指示剂检验溶液的
酸碱性;掌握常见酸、碱、盐的特性;会用 pH试纸测量溶液的酸碱性强弱;认识中和反应
的实质,知道中和反应在生产、生活中的应用;知道复分解反应及该反应发生的条件等。
考向一 气体的制取、收集和除杂
【例 1】 下图是实验室常用的一些装置。
(1)仪器 a的名称是__________;
(2)实验室制取并收集二氧化碳气体应选择的装置是________(填序号),检验二氧化碳是
否收集满的方法是__________________;
(3)用装置 A与 C连接制取并收集氧气,则装置 A中反应的化学方程式为___________,
当观察到装置 C中________时才开始收集;
(4 )SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到
空气中会形成酸雨。实验室用下图装置收集一瓶干燥的 SO2,装置的导管按气流方向连接的
顺序是________→________→________→________→e(填字母),装置中的 X是__________。
解析:(1)仪器 a为试管;(2)制取 CO2用大理石(或石灰石)与稀盐酸反应制取不需加热,
故选 B 作为发生装置;CO2密度比空气大,能溶于水,故选用向上排空气法收集;(3)用装
置 A与 C连接制取氧气时,制氧气药品是高锰酸钾,高锰酸钾在加热条件下,生成锰酸钾、
二氧化锰和氧气,用排水法收集时,当导管口有气泡连续均匀冒出时开始收集;(4)要收集
一瓶干燥的 SO2,用浓硫酸除去水蒸气,X为浓硫酸,长管进短管出,气体由 c进入,d出;
SO2的密度比空气大,故干燥后的 SO2由 b进入,a出;SO2有毒,故把 SO2溶于水。
答案:(1)试管
(2)B、D 将燃着的木条放在集气瓶口,若木条熄灭,则 CO2已集满
(3)2KMnO4=====
△
K2MnO4+MnO2+O2↑ 气泡连续均匀放出
(4)c d b a 浓硫酸
方法归纳 由反应物状态和反应条件确定发生装置;由气体的性质确定收集装置;除去
气体杂质先除去其他气体,最后除去水蒸气;有毒的、会污染空气的气体一定用尾气装置处
理。
考向二 空气和氧气
5
【例 2】 “减少污染,净化空气,还我一片蓝天”已成为城市居民共同的心声。
(1)洁净的空气中含量较多的气体有氧气和__________(填化学式)。
(2)汽车燃料燃烧不充分时,会产生炭粒和有毒的________(填化学式)气体,污染空气。
(3)汽车使用压缩天然气(CNG)作燃料,会减少对空气的污染。天然气所含主要成分的化
学式是__________。压缩天然气(CNG)加气站必须悬挂 图标,因为_______________。
解析:空气中含量较多的是氧气和氮气;汽车燃料燃烧不充分会产生炭粒和一氧化碳;
天然气的主要成分是甲烷;压缩天然气加气站必须禁止烟火,以防引燃加气站中空气里的天
然气,发生爆炸。
答案:(1)N2 (2)CO (3)CH4 加气站空气中含有天然气,遇到明火,可能发生爆炸
方法归纳 空气的污染包括气体污染和粉尘污染,气体污染包括 SO2、NO2和 CO的污
染等,在明确污染原因的前提下,分析防治措施是否可行,是否能起到防治污染的作用。
考向三 溶液
【例 3】 水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)“生命吸管”(如下图)是一种可以随身携带的小型水净化器,里面装有网丝、注入了
活性炭和碘的树脂等。其中活性炭起到________和过滤的作用。
(2)水常用来配制各种溶液,硝酸钾溶液中的溶质为____________________。
(3)农业生产常用溶质的质量分数为 10%~20%的 NaCl 溶液来选种。现将 300 g 25%的
NaCl溶液稀释为 15%的 NaCl溶液,需要加水的质量为________ g。
(4)根据下表回答问题。
温度/℃ 0 20 40 60 80 100
溶解度/g
NaCl 35.7 36.0 36.6 37.3 38.4 39.8
NH4Cl 29.4 37.2 45.8 55.2 65.6 77.3
①60℃时,向两个分别盛有 50 g NaCl和 NH4Cl的烧杯中,各加入 100 g的水,充分溶
解后,为饱和溶液的是__________溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。下列说法
正确的是________(填字母序号)。
A.溶质的质量不变 B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变 D.可升高温度或增加溶剂
解析:(1)活性炭具有吸附作用;(2)硝酸钾溶液是固体硝酸钾溶于水形成的,即溶质是
硝酸钾;(3)设需加水的质量为 x,则有:300 g×25%=(300 g+x)×15%,x=200 g;(4)①60℃
时,NaCl的溶解度为 37.3 g,即 100 g水中溶解 37.3 g NaCl恰好饱和,而 50 g NaCl在 100
g水中不能完全溶解,即得饱和溶液,同理,由60℃时NH4Cl的溶解度为 55.2 g知:50 g NH4Cl
能够完全溶解在 100 g水中,得到不饱和溶液;②因 NaCl的溶解度随温度的升高而增大,
可采用升温或增加溶剂的方法使饱和溶液变为不饱和溶液。
答案:(1)吸附 (2)硝酸钾 (3)200 (4)①NaCl ②D
方法归纳 溶液稀释的计算依据:稀释前后溶液中溶质质量不变;溶液在饱和溶液和不
饱和溶液之间相互转化条件:
6
饱和溶液 不饱和溶液[Ca(OH)2除外]。
考向四 碳和碳的化合物
【例 4】如图中的物质都是初中化学中所学的,其中 A、B为单质,B是可供动植物呼
吸的气体;甲、乙、丙为化合物,甲与过量的丙、乙与过量的丙两两反应的所有产物相同。
图中“—”表示两端的物质间能发生化学反应;“―→”表示物质间存在转化关系,部分反
应物或生成物已略去。
(1)写出 B的化学式______________;写出一种丙的名称__________。
(2)写出 A和甲反应的化学方程式:_________________________________________。
(3)写出乙―→甲的化学方程式:________________。
解析:B是可供动植物呼吸的气体,可知是 O2,由于单质 A能生成甲,并且 A与甲相
互之间还能反应,可推知 A为 C,甲为 CO2,又根据甲与过量的丙、乙与过量的丙反应的
产物相同,可知丙是碱溶液,乙是酸,因为碱与酸和碱与酸性氧化物反应都生成盐与水,乙
又能生成甲,则乙应是碳酸。
答案:(1)O2 氢氧化钠(或氢氧化钙等)
(2)C+CO2=====
高温
2CO
(3)H2CO3===CO2↑+H2O(合理答案均可)
方法归纳 解答此类推断题,首先要抓住突破口,然后顺藤摸瓜进行推理,若遇到多种
可能情况,则可用试探法,即假设某物质可能是什么,然后依据题中关系推理,若不合理则
排除,若合理则继续推理,直到推断出所有物质的名称,然后给出答案。
考向五 金属
【例 5】 向 AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,反应完成后过
滤,下列情况不可能存在的是( )。
A.滤纸上有 Ag、Cu、Fe,滤液中有 Zn2+、Fe2+
B.滤纸上有 Ag、Cu,滤液中有 Zn2+、Fe2+
C.滤纸上有 Ag、Cu,滤液中有 Cu2+、Zn2+、Fe2+
D.滤纸上有 Ag、Cu、Fe,滤液中有 Cu2+、Zn2+、Fe2+
解析:由于 D中滤纸上有 Fe,因此滤液中不会存在 Cu2+,因为 Fe 会将 Cu2+从溶液中
置换出来,选 D。
答案:D
方法归纳 如果盐溶液中有多种金属离子,金属先置换出较不活泼金属对应的离子,然
后再置换出较活泼的金属对应的离子。
考向六 酸 碱 盐
【例 6】 能大量共存且形成无色溶液的一组离子是( )。
A.Cu2+、SO、H+ B.Cl-、NH、OH-
C.Ba2+、SO、NO D.Na+、K+
、NO
7
解析:A中各离子共存,但 C u2+在溶液中呈蓝色溶液;B 中 NH、OH-
结合生成 NH3
和水,故不能共存;C中 Ba2+、SO结合生成难溶于水、也难溶于酸的白色沉淀,不能共存;
D中离子能大量共存,且形成无色溶液。
答案:D
方法归纳 溶液中物质共存问题的实质是物质溶于水发生电离,电离的各种离子两两结
合不能产生沉淀、气体或水。其基本类型有:①溶液若无色时则不存在有色离子:如 Fe3+(黄
色)、Fe2+(浅绿色)、Cu2+(蓝色);②在酸性溶液中,不能大量共存的离子:OH-
、CO、SO、
HCO 等;③在碱性溶液中,不能大量存在的离子:H+
、NH、Cu2+、Mg2+、Al3+、Fe3+、
Ag+
等;④彼此结合能生成沉淀的金属离子和酸根离子不能大量共存,Cl-和 Ag+
、Ba2+和
SO、Ca2+和 CO等。
1.下列关于 O2的说法不科学的是( )。
A.常用带火星的木条来检验空气中的 O2
B.硫在 O2里燃烧产生明亮的蓝紫色火焰
C.工业上将空气液化后再进行分离来制取 O2
D.加热 KClO3制 O2,可用MnO2作催化剂
2.下列有关碳及其氧化物的说法错误的是( )。
A.CO与 CO2可用澄清石灰水区分
B.CO具有还原性,可用于铁的冶炼
C.CO2的过多排放可导致酸雨的产生
D.金刚石和石墨结构中碳原子排列方式不同
3.下列有关铁的说法不正确的是( )。
A.生铁和钢都是铁合金
B.铁是地壳中含量最多的金属元素
C.工业炼铁的原理是:Fe2O3+3CO=====
高温
2Fe+3CO2
D.铁锅使用后及时洗净、干燥,以防生锈
4.除去下列物质中少量杂质(括号内的物质)的方法,合理的是( )。
A.CaO(CaCO3):加入足量的稀盐酸
B.CO2(CO):在氧气中点燃
C.H2(HCl、H2O):通过盛有足量生石灰和烧碱混合固体的干燥管
D.N2(O2、H2O):先通过加热的铜网,再通过盛有浓盐酸的洗气瓶
5.化学与我们的生活息息相关。现存:①氮气;②生石灰;③碳酸氢钠;④熟石灰;
⑤二氧化硫;⑥酒精。回答下列问题(均填序号):
(1)可作燃料的是__________。
(2)可作食品干燥剂的是__________。
(3)能形成酸雨的是__________。
(4)常用来改良酸性土壤的是__________。
(5)可作食品发酵粉的是__________。
(6)充入灯泡可延长灯泡使用寿命的是__________。
6.下列是初中化学部分重要的实验或实验装置。请按要求填空:
(1)A实验玻璃管②中产生的气体是__________;
(2)B实验如果实验数据小于 21%,可能原因是__________________(写出一点);
8
(3)C实验说明二氧化碳具有的性质是_______________________________________;
(4)写出用 D装置制取一种气体的化学方程式:______________________。
7.(1)下列三种金属被发现、使用的先后顺序为:铜、铁、铝。金属大规模被使用的先
后顺序跟(选填字母)________(A.地壳中金属元素的含量 B.金属的导电性 C.金属的活
动性)关系最大;目前世界上已有 50%以上的废钢铁得到回收利用,其目的是(选填字
母)____________(A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈);生锈的铁制品
放入盛有过量稀盐酸的洗槽中,观察到溶液变黄,有无色气泡逸出。写出其中一个反应的化
学方程式__________________,其反应类型是________。若要验证银、铁、锌的活动性顺序,
某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是________、________。
(2)A、B两种固体物质的溶解度曲线如下图所示。
①t1 ℃时,A和 B的溶解度大小关系是________。
②把 t1 ℃时 A 的饱和溶液变成不饱和溶液,除了升高温度外,还可以采取的方法有
________。
③t2 ℃时,A的溶解度为 25 g,在 t2 ℃时,向 50 g水中加入 20 g的 A物质,充分溶解
所得溶液的溶质质量分数为________。
④A中混有少量的杂质 B,若想得到较为纯净的 A,可以采用的方法是____________。
参考答案
专题提升演练
1.A 带火星的木条在空气中不复燃,不能检验空气中的氧气。
2.C CO2排放过多可引起温室效应;导致酸雨的气体是 SO2、NO2等。
3.B 铝是地壳中含量最多的金属元素。
4.C CaO和 CaCO3都能与盐酸反应,故无法除杂;因 CO2中有少量 CO不能被点燃,
不能用点燃的方法除去 CO;H2中混有 HCl、H2O,HCl能与生石灰、烧碱反应,H2O能与
9
生石灰反应,且能被烧碱吸收,能除去 HCl和 H2O;D项中通过加热的铜网,O2被除去,
通过盛有浓盐酸的洗气瓶无法除去 H2O,应通过浓硫酸的洗气瓶,可除去 H2O。
5.答案:(1)⑥ (2)② (3)⑤ (4)④ (5)③ (6)①
解析:酒精具有可燃性,可作燃料;生石灰能吸收水分,生成熟石灰,故可作食品干燥
剂;二氧化硫能与水反应生成酸,随水降落形成酸雨;熟石灰能中和酸,常用来改良酸性
土壤;碳酸氢钠受热易分解,放出 CO2气体,使食品松软可口,故可作发酵粉;氮气化学
性质稳定,不与灯丝反应,充入灯泡可延长灯泡使用寿命。
6.答案:(1)氢气(或 H2)
(2)装置漏气(或加热时间短,反应不充分;或铜的量太少,氧气没完全反应;或未
冷却至室温就读数等)
(3)不能燃烧,不支持燃烧,能灭火,密度比空气大
(4)CaCO3+2HCl===CaCl2+H2O+CO2↑(或 2H2O2=====
MnO22H2O+O2↑)
解析:(1)水的电解实验中与负极相连接产生的气体为氢气;(2)装置漏气、铜的量太
少,氧气没完全反应,未冷却至室温就读数等都能造成测定氧气的含量小于 21%;(3)由 C
中实验可知 CO2不能燃烧也不支持燃烧,能灭火,密度比空气大的性质;(4)用 D来制取
气体时,可用锌和稀硫酸反应制取氢气或可用大理石或石灰石反应制取 CO2,或用双氧水和
二氧化锰作催化剂制氧气。
7.答案:(1)C A Fe+2HCl===FeCl2+H2↑ 置换反应(或 Fe2O3+6HCl===2FeCl3
+3H2O,复分解反应) 硝酸银(AgNO3) 硫酸锌(ZnSO4或可溶性锌盐等)
(2)①AA) ②增加溶剂(或加水) ③20% ④降温结晶(或冷却热饱
和溶液法)
解析:(1)金属大规模使用的先后顺序与金属的活动性有关,金属的活动性越弱,使用
越早;回收利用废金属是为了节约金属资源;生锈的铁制品放入过量的稀盐酸中,发生的反
应有:铁和盐酸反应生成氯化亚铁和氢气,氧化铁和盐酸反应生成氯化铁和水,反应类型分
别为置换反应和复分解反应;验证银、铁、锌的活动性顺序,已使用铁丝,再选用可溶性锌
盐和硝酸银溶液。(2)t 1 ℃时 B的溶解度大于 A的溶解度;t1 ℃A的饱和溶液变成不饱和
溶液可采用升温或加溶剂。(3)t2 ℃时 A的溶解度为 25 g,50 g水中最多溶解 12.5 g的 A物
质,所得溶液已达到饱和,其溶质的质量分数为
12.5 g
50 g+12.5 g
×100%=20%;A的溶解度受
温度影响较大,B的溶解度受温度影响较小,A中混有少量 B,可采用降温结晶得到较纯净
的 A。
相关文档
- 中考化学总复习(人教版)精讲精练:第72021-11-1014页
- 中考化学总复习(人教版)精讲精练:专题2021-11-109页
- 中考化学总复习(人教版)精讲精练:专题2021-11-106页
- 中考化学总复习(人教版)综合模拟1(附2021-11-108页
- 中考化学总复习(人教版)阶段检测5(附2021-11-108页
- 中考化学总复习(人教版)精讲精练:第122021-11-1011页
- 中考化学总复习(人教版)精讲精练:专题2021-11-109页
- 中考化学总复习 专题检测题一(及答2021-11-1013页
- 中考化学总复习 练习题九(及答案)2021-11-1020页
- 中考化学总复习(人教版)精讲精练:第12021-11-1017页