- 230.13 KB
- 2021-11-12 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2020年山东省济宁市中考化学试卷
一、选择题(下列各题只有一个正确选项.其中,1~4小题各1分,5~10小题各2分,本大题共16分)
1. 下列物质的用途,一定涉及化学变化的是( )
A.金具有黄色金属光泽 制作饰品
B.活性炭具有吸附性 作除味剂
C.生石灰吸收空气中的水分 作干燥剂
D.干冰升华吸收大量的热 作制冷剂
2. 对下列物质构成的说法中,不正确的是( )
A.铜是由铜原子构成的金属单质
B.氧气是由氧分子构成的气体单质
C.水是由水分子构成的化合物
D.氯化钠是由氯化钠分子构成的化合物
3. 对CO2、C2H2、H2CO3、Ca(HCO3)2、Na2CO3五种物质的判断,正确的是( )
A.C2H2、H2CO3都是有机物
B.CO2、H2CO3都属于氧化物
C.Ca(HCO3)2、Na2CO3都属于盐
D.H2CO3、Na2CO3溶液都显酸性
4. 下列反应的化学方程式,书写正确的是( )
A.镁条在空气中长期放置发生氧化 Mg+O2=MgO2
B.高温煅烧石灰石制取生石灰 CaCO3=CaO+CO2↑
C.稀盐酸去除铁钉锈渍有气泡产生 2Fe+6HCl=2FeCl3+3H2↑
D.氢氧化钠溶液敞口放置发生变质 2NaOH+CO2=Na2CO3+H2O
5. 下列实验设计,不合理的是( )
选项
实验内容
实验过程
A
二氧化碳的溶解性
在充满二氧化碳气体的软塑料瓶中倒入13的水,拧紧瓶盖,振荡,塑料瓶迅速变瘪
B
浓盐酸的挥发性
打开盛有浓盐酸的细口瓶,瓶口有白雾产生
C
鉴定某溶液是氯化铁溶液
向溶液中滴加氢氧化钠溶液,有白色沉淀产生
D
硫酸铵是一种铵态氮肥
硫酸铵样品与熟石灰混合后研磨,有刺激性气味气体生成
A.A B.B C.C D.D
6. 通过一步化学反应,不能实现下列物质间转化的是( )
A.C→CO B.H2O2→O2
C.BaCl2→Ba(OH)2 D.NaCl→NaNO3
7. 10∘C时,将3g甲、乙两种可溶性固体分别放入盛有10mL水的试管中。两种物质的溶解情况(见图Ⅰ),两种物质的溶解度随温度的变化(见图Ⅱ)。下面对甲、乙两物质的判断,不正确的是( )
A.10∘C时,甲、乙两物质的溶液都是饱和溶液
B.温度升高至25∘C时,甲、乙两物质的溶液都是不饱和溶液
C.甲物质对应的溶解度曲线为a
D.可用降温结晶法分离甲、乙两种物质的混合物
8. 为鉴别氯化钠、氢氧化钠、碳酸钠和硫酸钠四种物质的溶液,设计如下实验:
5 / 5
下面对试剂①、试剂②和试剂③的选择,合理的是( )
A.①酚酞 ②稀盐酸 ③氯化钡
B.①酚酞 ②稀盐酸 ③稀盐酸
C.①石蕊 ②氯化钡 ③稀盐酸
D.①石蕊 ②氯化钡 ③碳酸钠
9. 在两只烧杯中分别放入相同质量的镁、锌两种金属,然后向两只烧杯中分别倒入相同质量、相同质量分数的稀硫酸,反应产生氢气的质量与消耗硫酸的质量关系见图。综合以上信息得到以下结论,合理的是( )
A.从图象可以看出,金属镁比金属锌的活动性强
B.若两种金属都有剩余,二者得到的氢气质量相同
C.若硫酸有剩余,二者得到氢气的质量相同
D.若两种金属完全溶解,二者消耗硫酸的质量相同
10. 向AgNO3、Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应,过滤。下面对反应结果的判断,不正确的是( )
A.若反应后溶液为蓝色,滤渣中一定不含有Zn
B.若反应后溶液为蓝色,滤渣中一定含有Ag,可能含有Cu
C.若反应后溶液为无色,滤渣中一定含有Ag和Cu
D.若反应后溶液为无色,滤渣中一定不含有Zn
二、填空与简答(共17分)
11. 按要求用符号回答下面问题:
(1)地壳中含量最多的金属元素________;
(2)空气中含量最多的气体单质________;
(3)天然气的主要成分________;
(4)硝酸钾溶液中的阴离子________。
12. 2019年碳家族再添新成员。某研究小组合成出第一个由18个碳原子构成的环状纯碳分子,其结构如图所示。回答:
(1)碳原子的结构示意图为,其最外层电子数是________;若碳元素在化合物中的化合价为+4价,写出一种符合要求的化合物的化学式________;
(2)尝试写出环状纯碳分子的化学式________。
13. 家庭或企业加工馒头、面包和饼干等食品时,常在面粉中加入膨松剂(如碳酸氢钠),蒸制或烘焙食品中产生大量气体,使面团疏松、多孔,制作的食品松软或酥脆,易于消化吸收。
阅读上面信息后,回答:
5 / 5
(1)信息中提供的膨松剂是________(填化学式);
(2)碳酸氢钠是一种________性的化合物(填“可溶”或“不溶”);
(3)碳酸氢钠能使蒸制或烘焙的食品疏松多孔,原理是________(用化学方程式解释)。
14. 镁及其合金是一种用途广泛的金属材料,大量的金属镁是从海水或卤水中提取的,其主要步骤见如图:
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用________;
(2)加入试剂①后,分离得到Mg(OH)2沉淀的方法是________;
(3)试剂②可以选用________;
(4)通电后,MgCl2分解生成Mg和Cl2的化学反应方程式________。
15. 某未知溶液,可能含有Na+、Cu2+、Ba2+、SO42-、Cl-中的几种。为确定溶液中含有的离子,实验如下:
①取未知溶液2∼3mL于试管中,滴加足量BaCl2溶液,有白色沉淀生成,静置;
②取①中上层清液,滴加AgNO3溶液,有白色沉淀生成;
③另取未知溶液2∼3mL于试管中,滴加NaOH溶液,有蓝色沉淀生成。
分析实验过程,回答:
(1)溶液中一定存在的离子是________;
(2)溶液中一定不存在的离子是________;
(3)溶液中可能存在的离子是________。
三、实验与探究(共11分)
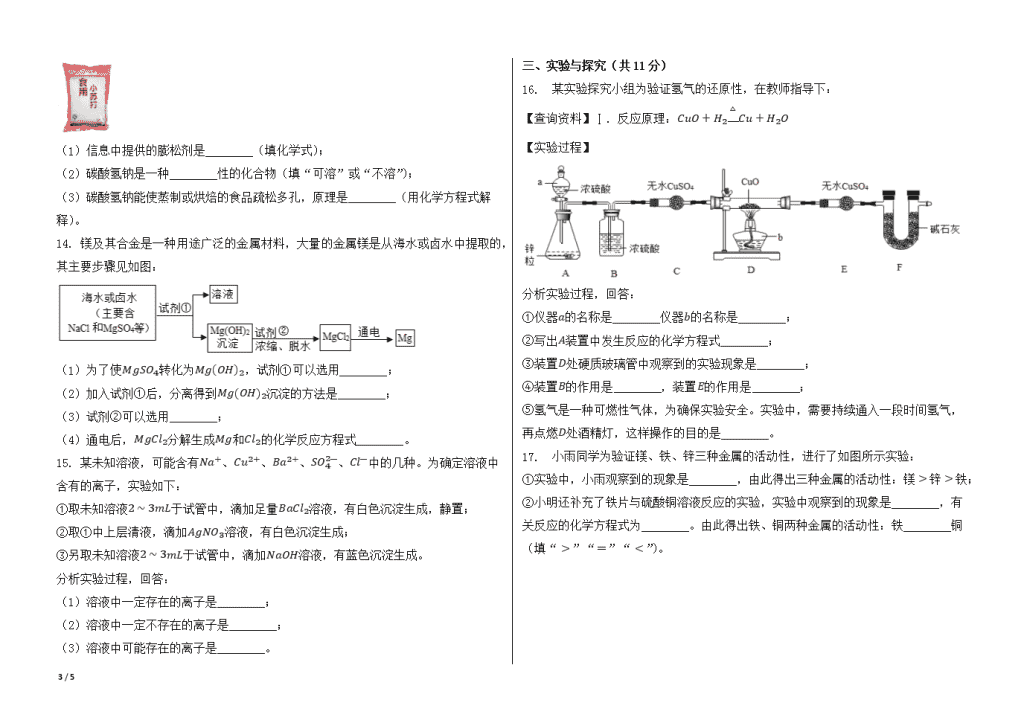
16. 某实验探究小组为验证氢气的还原性,在教师指导下:
【查询资料】Ⅰ.反应原理:CuO+H2△Cu+H2O
【实验过程】
分析实验过程,回答:
①仪器a的名称是________仪器b的名称是________;
②写出A装置中发生反应的化学方程式________;
③装置D处硬质玻璃管中观察到的实验现象是________;
④装置B的作用是________,装置E的作用是________;
⑤氢气是一种可燃性气体,为确保实验安全。实验中,需要持续通入一段时间氢气,再点燃D处酒精灯,这样操作的目的是________。
17. 小雨同学为验证镁、铁、锌三种金属的活动性,进行了如图所示实验:
①实验中,小雨观察到的现象是________,由此得出三种金属的活动性:镁>锌>铁;
②小明还补充了铁片与硫酸铜溶液反应的实验,实验中观察到的现象是________,有关反应的化学方程式为________。由此得出铁、铜两种金属的活动性:铁________铜(填“>”“=”“<”)。
5 / 5
四、分析与计算(共6分)
18. 人们在剧烈运动时,骨骼肌组织会供氧不足,导致产生的乳酸(化学式为C3H6O3)过度堆积,引起肌肉酸痛。回答:
(1)乳酸分子中,C、H、O三种原子的个数比为________;
(2)乳酸中,C、H、O三种元素的质量比为________。
19. 甲、乙、丙三个实验小组分别利用2g铜粉“测定空气中氧气的含量”,实验装置见图。课外兴趣小组为研究实验中铜粉的氧化情况,又进行以下实验:
①兴趣小组将甲、乙、丙三个实验小组硬质玻璃管中的残留固体全部取出,称量后,置于烧杯中;
②在烧杯中加入足量稀硫酸使之充分反应,将剩余固体过滤、洗涤、干燥、称量;相关数据见下表:
甲组
乙组
丙组
反应前固体质量
2.016g
2.016g
2.024g
反应后固体质量
1.936g
1.936g
1.904g
(1)烧杯中发生反应的化学方程式为________;
(2)甲、乙两组实验数据相同,残留固体中氧化铜的质量为________,丙组残留固体中氧化铜的质量为________。
(3)兴趣小组通过分析数据得出:甲、乙两组实验数据更接近实际空气中氧气的含量,丙组差异较大。你认为丙组在“测定空气中氧气的含量”实验中,可能存在的操作失误是________。
5 / 5
参考答案与试题解析
2020年山东省济宁市中考化学试卷
一、选择题(下列各题只有一个正确选项.其中,1~4小题各1分,5~10小题各2分,本大题共16分)
1.C
2.D
3.C
4.D
5.C
6.C
7.A
8.A
9.B
10.D
二、填空与简答(共17分)
11.Al
N2
CH4
NO3-
12.4,CO2
C18
13.NaHCO3
可溶
2NaHCO3△Na2CO3+H2O+CO2↑
14.氢氧化钠溶液
过滤
稀盐酸
MgCl2Mg+Cl2↑
15.Cu2+、SO42-
Ba2+
Na+、Cl-
三、实验与探究(共11分)
16.分液漏斗,酒精灯,Zn+H2SO4=ZnSO4+H2↑,黑色固体变为红色,玻璃管壁有水珠出现,去除水蒸气,检验水的生成,排出内部残留的空气
17.三种金属表面都有气泡冒出,冒出气泡的速率:镁>锌>铁,铁片表面有红色固体析出,溶液由蓝色逐渐变成浅绿色,Fe+CuSO4=FeSO4+Cu,>
四、分析与计算(共6分)
18.1:2:1
6:1:8
19.CuO+H2SO4=CuSO4+H2O
0.08g,0.12g
装置漏气
5 / 5
相关文档
- 中考化学第一轮复习考点分析:生活中2021-11-123页
- 江苏专版2020中考化学复习方案第一2021-11-125页
- 2019年湖南省怀化市中考化学试卷2021-11-1230页
- 北京专版2020中考化学复习方案实验2021-11-1211页
- 2013人教版初中化学实验操作考试试2021-11-1223页
- 2019年中考化学试题分类:考点9 氧气2021-11-121页
- 北京专版2020中考化学复习方案实验2021-11-129页
- 2019年中考化学试题分类:10粗盐和提2021-11-123页
- 2020中考化学复习方案主题一物质构2021-11-1214页
- 2019年全国各地中考化学试题-重庆2021-11-1210页