- 53.50 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
二氧化碳的制取
例1 实验室现有大理石、高锰酸钾、稀盐酸、稀硫酸和紫色石蕊溶液及相关的仪器和用品,小辉同学要通过实验验证二氧化碳能与水反应的性质。请结合右图回答下列问题:
(1)连接A和B并将实验装置图补充完整;
(2)A中发生反应的化学方程式为___________;
(3)B中观察到的实验现象是___________;
(4)在一般情况下仪器C的作用是___________。
解析 A和B装置要用导管连接起来,装置A中的导管不宜过长,稍微露出橡皮塞即可,装置B中的导管要伸入到液面以下;实验室里常用大理石或石灰石与稀盐酸反应来制取CO2;CO2能与水反应生成H2CO3,因此B瓶中的紫色石蕊试液会变红;试管在化学实验中常用作少量试剂的反应容器,能在常温或加热时使用。
答案 (1)略 (2)CaCO3+2HCl=CaCl2+CO2↑+H2O (3)紫色石蕊溶液变红(并且导管口有气泡冒出) (4)用作少量试剂的反应容器,在常温或加热时使用
例2 下图是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质的的实验装置图,试根据题目要求回答下列问题:
(1)仪器a的名称是_________;装置A中发生的化学方程式为______________________,装置C中观察到的现象是___________。
(2)装置D中观察到下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳的密度比空气大,它不能燃烧,也不能支持燃烧。由此可知,二氧化碳在生活中可用于___________。
(3)实验室用装置E来收集二氧化碳时,二氧化碳应从_______(填“c端”或“d端”)通入。
解析 本题综合考查了CO2的制取方法及相关性质实验。仪器a是长颈漏斗,实验室里常用大理石或石灰石与稀盐酸反应来制取CO2;CO2能与水反应生成H2CO3,因此C瓶中的紫色石蕊试液会变红;CO2不能燃烧,也不能支持燃烧,密度比空气大,生活中可用它来灭火;CO2的密度比空气大,因此若用装置E来收集时,CO2应该从c端通入。
答案 (1)长颈漏斗 CaCO3+2HCl=CaCl2+CO2↑+H2O 紫色的石蕊试液变红 (2)灭火 (3)c端
例3下列装置用于实验室里CO2的制备、净化、检验,最后收集一瓶干燥的CO2。请回答下列问题:
(1)对实验室制取二氧化碳药品选择的探究实验,记录如下:
组别
药品
实验现象
①
碳酸钠粉末和稀盐酸
产生气泡速率很快
②
块状石灰石和稀硫酸
产生气泡速率缓慢并逐渐停止
③
块状石灰石和稀盐酸
产生气泡速率适中
从制取和收集的角度分析,一般选择第_________(填序号)组药品,所发生反应的化学方程式为______________________。
(2)把C、D中的液体名称填入下表:
B(盐)
C(碱)
D(酸)
液体名称
碳酸氢钠溶液
(3)B中反应的化学方程式是______________________。
(4)C中反应的化学方程式是______________________。
(5)反应过程中将弹簧夹关闭,在A中看到的现象是______________________。
(6)E收集方法说明二氧化碳具有的物理性质是______________________。
解析 本题是一道关于实验室制取CO2的综合性实验
探究题,主要考查了药品的选择、化学方程式的书写、气体的净化、检验及收集等知识。实验室制取CO2一般用石灰石(或大理石)与稀盐酸来进行,不能用碳酸钠,因为反应速率太快,不易收集,也不能用稀硫酸,因为稀硫酸与CaCO3反应生成的微溶物CaSO4会阻碍反应的进一步进行;盐酸具有挥发性,会使制取的CO2气体中含有少量的HCl气体,应先将气体通过NaHCO3溶液;检验CO2应该选择澄清的石灰水,干燥CO2应选择浓硫酸;关闭弹簧夹,锥形瓶内压强增大,锥形瓶内的液面会下降、长颈漏斗内液面会上升;CO2的密度比空气大,可用向上排空气法来收集。
答案 (1)③ CaCO3+2HCl=CaCl2+H2O+CO2↑ (2)C:澄清石灰水 D:浓硫酸 (3)NaHCO3+HCl=NaCl+H2O+CO2↑ (4)CO2+Ca(OH)2=CaCO3↓+H2O (5)A中锥形瓶内液面下降、长颈漏斗内液面上升 (6)二氧化碳的密度比空气大
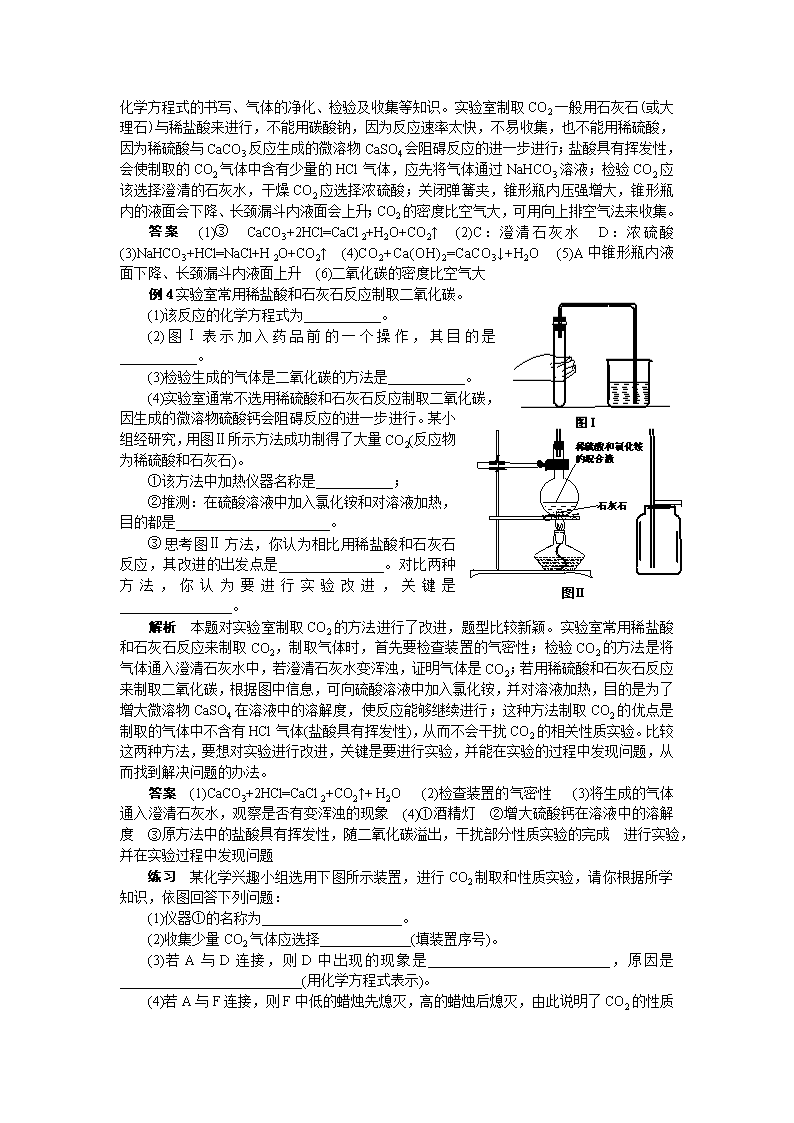
例4实验室常用稀盐酸和石灰石反应制取二氧化碳。
(1)该反应的化学方程式为___________。
(2)图Ⅰ表示加入药品前的一个操作,其目的是___________。
(3)检验生成的气体是二氧化碳的方法是___________。
(4)实验室通常不选用稀硫酸和石灰石反应制取二氧化碳,因生成的微溶物硫酸钙会阻碍反应的进一步进行。某小组经研究,用图Ⅱ所示方法成功制得了大量CO2(反应物为稀硫酸和石灰石)。
①该方法中加热仪器名称是___________;
②推测:在硫酸溶液中加入氯化铵和对溶液加热,目的都是______________________。
③思考图Ⅱ方法,你认为相比用稀盐酸和石灰石反应,其改进的出发点是_______________。对比两种方法,你认为要进行实验改进,关键是________________。
解析 本题对实验室制取CO2的方法进行了改进,题型比较新颖。实验室常用稀盐酸和石灰石反应来制取CO2,制取气体时,首先要检查装置的气密性;检验CO2的方法是将气体通入澄清石灰水中,若澄清石灰水变浑浊,证明气体是CO2;若用稀硫酸和石灰石反应来制取二氧化碳,根据图中信息,可向硫酸溶液中加入氯化铵,并对溶液加热,目的是为了增大微溶物CaSO4在溶液中的溶解度,使反应能够继续进行;这种方法制取CO2的优点是制取的气体中不含有HCl气体(盐酸具有挥发性),从而不会干扰CO2的相关性质实验。比较这两种方法,要想对实验进行改进,关键是要进行实验,并能在实验的过程中发现问题,从而找到解决问题的办法。
答案 (1)CaCO3+2HCl=CaCl2+CO2↑+ H2O (2)检查装置的气密性 (3)将生成的气体通入澄清石灰水,观察是否有变浑浊的现象 (4)①酒精灯 ②增大硫酸钙在溶液中的溶解度 ③原方法中的盐酸具有挥发性,随二氧化碳溢出,干扰部分性质实验的完成 进行实验,并在实验过程中发现问题
练习 某化学兴趣小组选用下图所示装置,进行CO2制取和性质实验,请你根据所学知识,依图回答下列问题:
(1)仪器①的名称为____________________。
(2)收集少量CO2气体应选择_____________(填装置序号)。
(3)若A与D连接,则D中出现的现象是__________________________,原因是__________________________(用化学方程式表示)。
(4)若A与F连接,则F中低的蜡烛先熄灭,高的蜡烛后熄灭,由此说明了CO2
的性质有__________________________、__________________________。
答案 ⑴长颈漏斗 ⑵B ⑶紫色石蕊变红 CO2+H2O=H2CO3 ⑷密度比空气大 不能燃烧,不能支持燃烧