- 2.06 MB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2017年各地中考化学真题分项解析汇编
专题9—1 溶液、溶液的组成及配制(原卷)
一、选择题
1.下列说法不正确的是
A.硝酸铵固体溶于水是吸热过程 B.乙醇与水混合可形成溶液
C.饱和溶液的质量分数一定大于不饱和溶液
D.氯化钠溶液能够导电是因为溶液中存在自由动的离子
2.【2017年重庆市B】下列物质不属于溶液的是( )
A.冰水 B.碘酒 C.食盐水 D.浓盐酸
3.【2017年重庆市B】下列相关实验方法能达到目的是( )
选项
实验目的
实验方法
A
鉴别稀硫酸和硫酸钠溶液
滴加酚酞
B
鉴别氢气和甲烷
点燃,火焰上罩一个冷而干燥的烧杯
C
除去KCl固体中的MnO2
溶解、过滤和蒸发
D
除去NaCl溶液中少量的Na2CO3
加入足量的石灰水,过滤
A.A B.B C.C D.D
4.【2017年重庆市A】餐桌上的饮品种类丰富,下列饮品中属于溶液的是( )
A.酸奶 B.玉米糊 C.冰水 D.可乐
5.【2017年重庆市A】两个烧杯中分别盛装X、Y的饱和溶液,两只试管中分别装有NaOH和NH4NO3固体,向两只试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( )
A.Y的溶解度曲线为b曲线 B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2℃降温到t1℃,溶质的质量分数变大
D.t3℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
6.【2017年山东省枣庄市】溶液的知识广泛用于生产、生活。下列说法正确的是( )
A.洗涤剂去油污的原理是溶解 B.植物油加入水可得溶液
C.氧化钠溶于水,温度明显上升 D.尿素施用过量会导致水污染
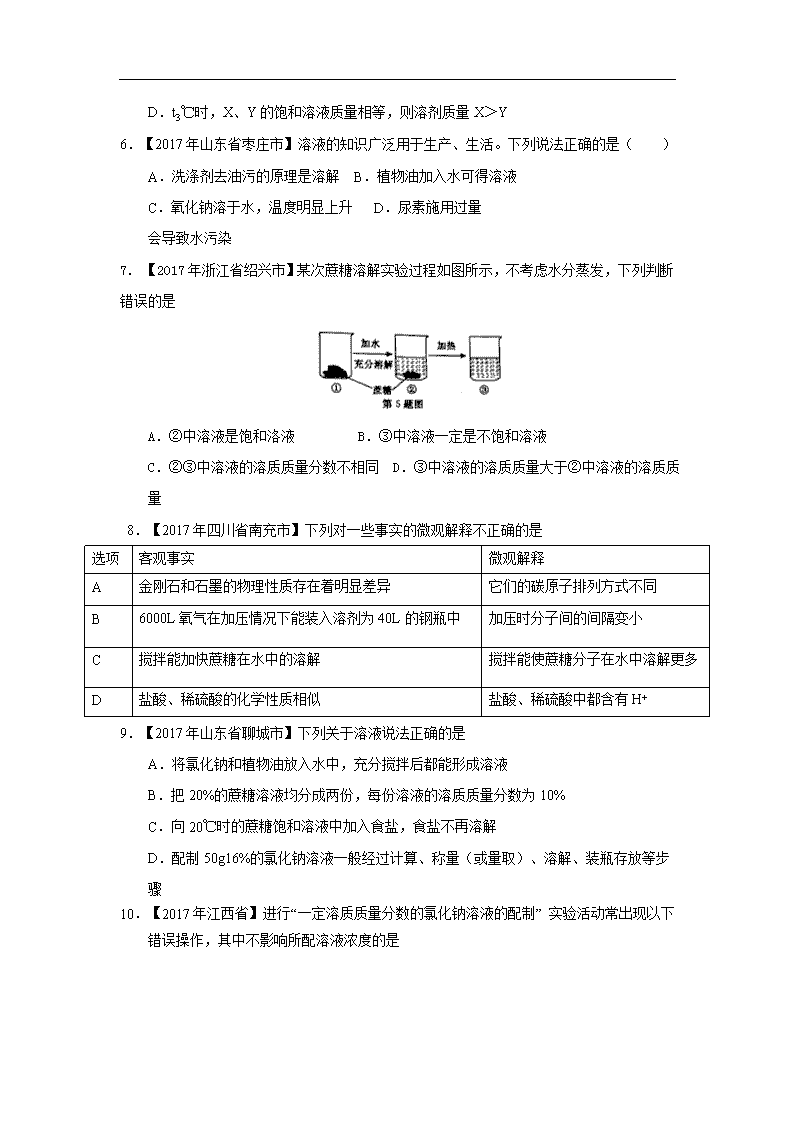
7.【2017年浙江省绍兴市】某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是
A.②中溶液是饱和洛液 B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同 D.③中溶液的溶质质量大于②中溶液的溶质质量
8.【2017年四川省南充市】下列对一些事实的微观解释不正确的是
选项
客观事实
微观解释
A
金刚石和石墨的物理性质存在着明显差异
它们的碳原子排列方式不同
B
6000L氧气在加压情况下能装入溶剂为40L的钢瓶中
加压时分子间的间隔变小
C
搅拌能加快蔗糖在水中的溶解
搅拌能使蔗糖分子在水中溶解更多
D
盐酸、稀硫酸的化学性质相似
盐酸、稀硫酸中都含有H+
9.【2017年山东省聊城市】下列关于溶液说法正确的是
A.将氯化钠和植物油放入水中,充分搅拌后都能形成溶液
B.把20%的蔗糖溶液均分成两份,每份溶液的溶质质量分数为10%
C.向20℃时的蔗糖饱和溶液中加入食盐,食盐不再溶解
D.配制50g16%的氯化钠溶液一般经过计算、称量(或量取)、溶解、装瓶存放等步骤
10.【2017年江西省】进行“一定溶质质量分数的氯化钠溶液的配制” 实验活动常出现以下错误操作,其中不影响所配溶液浓度的是
11.【2017年江苏省扬州市】下列物质溶于水,能使溶液温度降低的是
A.硝酸铵 B.氧化钙 C.氢氧化钠 D.浓硫酸
12.【2017年江苏省扬州市】下列说法正确的是
A.粉笔灰分散到水中形成溶液 B.自来水是纯净水
C.长期饮用硬水有益人体健康 D.水是宝贵的资源
13.【2017年江苏省苏州市】下列关于溶液的说法中,正确的是
A.泥土加入水中,振荡后可以形成溶液
B.蔗糖溶液上半部分溶液的甜度低于下半部分溶液的甜度
C.氢氧化钠溶液能导电,因为溶液中有较多自由移动的离子
D.氯化钠饱和溶液中不能再溶解少量硝酸钾晶体
14.【2017年湖南省长沙市】下列说法错误的是( )
A.饱和溶液一定是浓溶液 B.糖水、汽水都是溶液
C.洗洁精去油污是因为洗洁精具有乳化功能 D.溶液都是均一、稳定的混合物
二、非选择题
15.【2017年浙江省丽水市】用溶质质量分数为98%、密度为1.84克/厘米3的浓硫酸配制溶质质量分数为10%的稀硫酸100毫升,计算时必须查阅的数据是 。配制过程除使用量筒、玻璃棒和胶头滴管外,还需要的一种玻璃仪器是 。
16.【2017年浙江省金华市】在室温条件下,对100mL氯化钠饱和溶液进行如图所示操作:
(1)最终甲、乙两烧杯中溶液一定是饱和溶液的是 。
(2)乙溶液在加50mL水的过程中,下列这些量逐渐减小的是 。
①溶解度 ②溶质质量分数 ③溶剂的质量 ④溶液的密度
17.【2017年浙江省嘉兴市】实验室有一瓶由氯化钾和硝酸钾组成的化肥,但标注的质量分数己模糊不清,小明想通过实验重新标注,以下是他进行的实验步骤:
①取10克样品于烧杯中,加入蒸馏水充分溶解,配制成60克溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
⑧将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35克。
请根据上述实验回答:(相关反应的化学方程式为:KCl+AgNO3=AgCl↓+KNO3)
(1)在过滤操作中使用的玻璃仪器有:烧杯、______和玻璃棒。
(2)样品中氯化钾的质量分数为多少?(要求列式计算)
(3)完全反应后,混合液中的硝酸钾质量是多少克?
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小于计算得出的理论值。造成这种结果的原因可能是 ______。 (选填编号)
A.晶体没有干燥 B.蒸发时液体飞溅 C.硝酸钾残留在玻璃棒上
18.【2017年天津市】(7分)溶液与人们的生活息息相关。
(l)下列少量物质分别放入水中,充分搅拌,可以得到溶液的是______(填字母)。
A.高锰酸钾 B.汽油 C.面粉
(2)在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度升高。这种物质是______(填字母)。
A.烧碱 B.硝酸铵 C.氯化钠
(3)下表是三种物质在不同温度时的溶解度,根据表中信息回答问题。
温度/℃
0
20
40
60
80
100
溶解度/g
氯化钠
35.7
36.0
36.6
37.3
38.4
39.8网
硝酸钾
13.3
31.6
63.9
110
169
246
氢氧化钙
0.19
0.17
0.14
0.12
0.09
0.08
① 60℃时,氯化纳的溶解度_______硝酸钾的济解度(填“>”“=”或“<”)。
②表中某物质的饱和溶液随温度升高析出固体,该物质是_______(填化学式)。
③ 20℃时,氯化钠饱和溶液中溶质的质量分数为________(结果保留至0.1%)。
④ 向20℃的氢氧化钙饱和溶液中加入少量生石灰,再冷却至20℃,此时溶液中溶质的质量比加入生石灰前溶液中溶质的质量____(填“增大”“不变”或“减小”)。
⑤ 混有少量氯化钠的硝酸钾固体,加水配成80℃的硝酸钾饱和溶液,再冷却至20℃,析出晶体并得到溶液。下列有关说法中正确的是_______(填字母)。
A.析出的晶体中不一定含有硝酸钾
B.所得溶液一定是硝酸钾饱和溶液
C.上述方法可以将两种物质完全分离
19.【2017年天津市】(10分)酸、碱、盐在生产生活中具有广泛的用途。
(l)制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制50g质量分数为10%的氢氧化钠溶液。
① 若用氢氧化钠固体配制,需称量氢氧化钠的质量为________g。
② 用氢氧化钠固体配制10%的氢氧化钠溶液过程中需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要________。
③ 下列操作正确的是________(填字母)。
A.称量氢氧化钠固体时,左盘放祛码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为lg/cm3)配制50g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为________g;配制时应选用________mL的量筒量取水(填“10”或“50”)。
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如下实验:
回答下列问题:
① 反应I 的化学方程式为____________。
② 白色沉淀C是________(填化学式)。
③ 原固体粉末中一定不含________(填化学式)。
20.【2017年四川省内江市】(12分)仔细阅读下面的探究实验信息,回答相关问题。
I.[实验目的]探究溶解过程中,溶液温度的变化情况。
II.[查阅资料]
(1)物质溶解于水的过程包括吸收热量(Q吸)的扩散过程和放出热量(Q放)的水合过程。
(2)实验条件下,水的凝固点为0℃、沸点为100℃。
III.[提出猜想]物质溶解过程中,溶液的温度可能升高或降低或不变。
IV.[实验探究]某探究小组的同学设计了如下图所示的两种实验方案。在图2所示方案中,每次加入物质b之前,均使用温度计控制热水温度,使之保持在99℃。
V.[实验结论]
(1)图1所示实验中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度_____(填“升高”或“降低”或“不变”,下同)。
(2)图2所示实验中,若加入物质b后,热水会突然沸腾,说明溶液的温度__________。
VI.[拓展实验]按照图3所示进行实验。若物质c为NaOH,则U型管内的左边液面将_______(填“升高”或“低于”或“等于”)右边液面;若U型管内的液面位置变化与之相反,则物质c为______(填序号)。
①CaO ②NH4NO3 ③浓H2SO4
VII.[反思交流]
(1)该小组的同学进一步就物质溶解过程中溶液温度变化的原因展开了讨论,分析得出:若Q吸_____Q放(填“>”或“<”或“=”,下同),则溶液温度升高;若Q吸与Q放的相对大小与之相反,则溶液温度降低;若Q吸_____Q放,则溶液温度不变。
(2)在图2所示方案中,小张同学对实验现象很感兴趣,他继续向热水中加入相同质量的物质b,又看到沸腾现象,至烧杯中出现固体物质后,再继续加入相同质量的物质b,就看不到沸腾现象。请解释不再产生沸腾现象的原因________________________________。
21.【2017年四川省德阳市】(4分)某校化学课外活动小组的同学在实验室的一次探究性活动中,他们将50g氢氧化钠溶液与50g硫酸铜溶液混合恰好完全反应,得到9.8g沉淀。请你计算氢氧化钠溶液中溶质的质量分数。
22.【2017年山东省德州市】(3分)控制变量法是科学探究中常用的方法之一。
(1)在探究固体物质的溶解度时,需要考虑的因素有:①溶质的种类; ②溶剂的种类;③溶质最多被溶解的质量; ④溶剂的质量; ⑤温度。
如测定“某物质在不同温度下的溶解度”,研究的是_________ (填序号)受温度的影响,这就需要控制其他因素保持不变。
(2)右表是利用控制变量法测得的氯化钠、硝酸钾在不同温度时的溶解度,请根据表格内容及实验现象回答下列问题。
温度(℃)
20
40
50
溶解度/g
NaCl
36.0
36.6
37.0
KNO3
31.6
63.9
85.5
①从上表可知,两种物质的溶解度受温度变化影响较大的是____________;
②20℃时,将等质量的NaCl、KNO3分别放入盛有100
g水的两个烧杯中,充分溶解后如图1所示,升温到50℃时如图2所示。试判断:50℃时甲烧杯中的溶液一定是______(填“饱和溶液”、“不饱和溶液”或“不能确定”)。
23.【2017年山东省临沂市】工业上常用红锌矿(主要含ZnO)和18~25%的稀硫酸为原料制取硫酸锌。
(1)硫酸锌中硫元素和氧元素的质量比是_________ 。
(2)l00g溶质质量分数为98%的浓硫酸配制成溶质质量分数为20%稀硫酸。需要水的质量是___。
24.【2017年江苏省苏州市】(8分)为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验。(提示:本实验所川汽油与KMnO4、碘均不发生化学反应)
【实验l】KMnO4晶体在不同溶剂中的溶解实验
根据实验步骤、实验操作图示填写相关实验现象。
实验步骤
实验操作图示
实验操作及现象
步骤1
振荡后静置:
(1)A试管中晶体全部溶解,溶液呈________色;B试管中晶体不溶解,汽油不变色。
步骤2
将步骤1中A试管内溶液倒人B试管中,振荡后静置:(2)B试管中观察到的现象为__________。
【实验2]碘在不同溶剂中的溶解实验
根据实验操作图示回答相关问题。
实验操作图示
实验结论或解释
(3)由图2所示现象叮知:碘_____(选填“不”、“微”或“易”)溶于水
(4)图3所示试管中液体分层。上层紫红色溶液的名称是________。说明碘在汽油中的溶解性比在水中_____(选填“强”或“弱”)
【反思与应用】
(5)①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体______(选填“分层”或“小分层”)。
②“从稀碘水巾提取碘”是“海带提碘”工艺巾的一个重要步骤,其原理类似【实验2]中第二步操作。工业实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是________。
25.【2017年江苏省南京市】 (7分)溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是_________。
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为________,水的体积为________mL (水的密度近似看作1g/cm3)。
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如右下图.t1℃时,甲物质的溶解度是________。t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是________(填“甲”或“乙”)物质的饱和溶液。
选项
x
y
A
水
氧化钙
B
水
硝酸铵
C
浓硫酸
水
D
稀盐酸
镁
(4)按右上图所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是______。
26.【2017年湖南省邵阳市】化学源于生活,生活中蕴含着许多化学知识。
(1)用洗涤剂去除油污,是利用洗涤剂的__________作用。
(2)邵阳地区的生活用水多是硬水,生活中常用________的方法降低水的硬度。
(3)打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随______而减小。
(4)医生给胃酸过多的病人所开处方中,常包括含 Al(OH)3 的药物,试用化学方程式表示其治疗原理:______________ 。
27.【2017年湖南省邵阳市】某同学配制50g6%氯化钠溶液,整个操作过程如下图所示,回答下列问题:
(1)配制溶液的正确操作顺序为_______(填序号,下同),其中操作错误的是________。
(2)图② 中盛放氯化钠固体的仪器名称是 ______,需称取氯化钠 _______g。
(3)量水时选用的量筒的量程最合适的是______(填序号),读数时视线要与量筒内______保持水平。
A.10 ml B.25 ml C.50ml D.100ml
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是_______(填序号)。
A.氯化钠固体不纯 B.用生锈砝码称量
C.装瓶时有少量溶液洒出 D.溶解时烧杯内壁有水珠
28.【2017年广州市】(6分)某同学在实验室用6.5g粗锌(假设杂质不参与反应)和稀盐酸制取H2。
(1)配制100g 10%稀盐酸需要37%浓盐酸(密度1.19g/cm3)的体积为 mL(结果保留小数点后一位)。除了胶头滴管、烧杯外还需要的玻璃仪器是 、 。
(2)6.5g粗锌完全反应共产生H2的质量为0.16g,则该粗锌中锌的质量分数为 。
(3)验证后用装满水的10mL量筒代替小试管收集H2,装置如图所示。
①10mL量筒的最大刻度靠近 端。(填写“M”或“N”)
②当10mL量筒中的水全部被排尽后,实际收集到的H2体积V 10.0mL。(填写“>”、“=”或“<”)
29.【2017年湖南省长沙市】将适量二氧化碳通入100g氢氧化钠溶液中,恰好完全反应后,得到108.8g碳酸钠溶液。请计算:
(1)参加反应的二氧化碳的质量为_______g;
(2)氢氧化钠溶液的溶质质量分数_________.
2017年各地中考化学真题分项解析汇编
专题9—1 溶液、溶液的组成及配制(解析卷)
一、选择题
1.下列说法不正确的是
A.硝酸铵固体溶于水是吸热过程 B.乙醇与水混合可形成溶液
C.饱和溶液的质量分数一定大于不饱和溶液
D.氯化钠溶液能够导电是因为溶液中存在自由动的离子
【答案】C
2.【2017年重庆市B】下列物质不属于溶液的是( )
A.冰水 B.碘酒 C.食盐水 D.浓盐酸
【答案】A
【解析】溶液是均一稳定的混合物。A、冰水属于纯净物,不属于溶液;B、碘酒是碘溶于酒精形成的均一稳定的混合物,属溶液;C、食盐水是氯化钠溶于水形成的均一稳定的混合物,属溶液;D、浓盐酸是氯化氢气体溶于水形成的均一稳定的混合物,属溶液。故选A。
3.【2017年重庆市B】下列相关实验方法能达到目的是( )
选项
实验目的
实验方法
A
鉴别稀硫酸和硫酸钠溶液
滴加酚酞
B
鉴别氢气和甲烷
点燃,火焰上罩一个冷而干燥的烧杯
C
除去KCl固体中的MnO2
溶解、过滤和蒸发
D
除去NaCl溶液中少量的Na2CO3
加入足量的石灰水,过滤
A.A B.B C.C D.D
【答案】C
【解析】A、稀硫酸和硫酸钠溶液分别显酸性、中性,均能使酚酞溶液显无色,不能鉴别,错误;B、氢气和甲烷燃烧均能生成水蒸气,点燃,火焰上罩一个冷而干燥的烧杯,烧杯内壁上均出现水雾,不能鉴别,错误; C、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,正确; D、除杂质的要求是:要把杂质除去,但不能除去了需要的物质,更不能带入新的杂质。Na2CO3能与足量的石灰水反应生成碳酸钙沉淀和氢氧化钠,能除去杂质但引入了新的杂质氢氧化钠,不符合除杂原则,错误。故选C。
4.【2017年重庆市A】餐桌上的饮品种类丰富,下列饮品中属于溶液的是( )
A.酸奶 B.玉米糊 C.冰水 D.可乐
【答案】D
5.【2017年重庆市A】两个烧杯中分别盛装X、Y的饱和溶液,两只试管中分别装有NaOH和NH4NO3固体,向两只试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( )
A.Y的溶解度曲线为b曲线 B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2℃降温到t1℃,溶质的质量分数变大
D.t3℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
【答案】D
【解析】A、硝酸铵溶于水,溶液温度降低,Y的饱和溶液出现浑浊,所以Y的溶解度随温度的降低而减小,所以Y的溶解度曲线为a曲线,故A错误;B、通过推导可知,X物质的溶解度曲线是b,所以升温可使X的饱和溶液变浑浊,故B错误;C、X物质的溶解度随温度的降低而增大,所以X的饱和溶液从t2℃降温到t1℃,溶质的质量分数不变,故C错误;D、t3℃时,Y物质的溶解度大于X物质的溶解度,所以X、Y的饱和溶液质量相等,则溶剂质量X>Y,故D正确.故选:D.
6.【2017年山东省枣庄市】溶液的知识广泛用于生产、生活。下列说法正确的是( )
A.洗涤剂去油污的原理是溶解 B.植物油加入水可得溶液
C.氧化钠溶于水,温度明显上升 D.尿素施用过量会导致水污染
【答案】D
【解析】A.洗涤剂去油污的原理是乳化,说法错误;B.植物油加入水可得乳浊液,说法错误;C.氧化钠不溶于水,温度无明显变化,说法错误;D.尿素是氮肥,过量使用会造成水污染,说法正确。故选D。
7.【2017年浙江省绍兴市】某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是
A.②中溶液是饱和洛液 B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同 D.③中溶液的溶质质量大于②中溶液的溶质质量
【答案】B
8.【2017年四川省南充市】下列对一些事实的微观解释不正确的是
选项
客观事实
微观解释
A
金刚石和石墨的物理性质存在着明显差异
它们的碳原子排列方式不同
B
6000L氧气在加压情况下能装入溶剂为40L的钢瓶中
加压时分子间的间隔变小
C
搅拌能加快蔗糖在水中的溶解
搅拌能使蔗糖分子在水中溶解更多
D
盐酸、稀硫酸的化学性质相似
盐酸、稀硫酸中都含有H+
【答案】C
【解析】A决定物质性质的是物质的组成和结构,金刚石和石墨的组成元素相同,都是碳元素,但是两物质中碳原子的排列方式不同,即物质的结构不同,所以金刚石和石墨的物理性质存在着明显差异;B宏观物质是由微观粒子构成,微粒间是有间隔的,通常气体物质分子间的间隔较大,加压时分子间的间隔易变小,易被压缩;C搅拌能加快蔗糖在水中的溶解,是因为反应搅拌时加快了分子的运动,加快了蔗糖的溶解,但是由于搅拌不能改变物质的溶解度,所以搅拌不能使蔗糖分子在水中溶解更多;D溶液的化学性质是由溶质溶于水产生的离子决定的,酸性溶液中都有氢离子,所以酸的溶液有相似的化学性质。
9.【2017年山东省聊城市】下列关于溶液说法正确的是
A.将氯化钠和植物油放入水中,充分搅拌后都能形成溶液
B.把20%的蔗糖溶液均分成两份,每份溶液的溶质质量分数为10%
C.向20℃时的蔗糖饱和溶液中加入食盐,食盐不再溶解
D.配制50g16%的氯化钠溶液一般经过计算、称量(或量取)、溶解、装瓶存放等步骤
【答案】D
10.【2017年江西省】进行“一定溶质质量分数的氯化钠溶液的配制” 实验活动常出现以下错误操作,其中不影响所配溶液浓度的是
【答案】D
【解析】溶液是均一、稳定的混合物。故选D。
11.【2017年江苏省扬州市】下列物质溶于水,能使溶液温度降低的是
A.硝酸铵 B.氧化钙 C.氢氧化钠 D.浓硫酸
【答案】A
【解析】物质溶于水有三种现象如氧化钙、氢氧化钠、浓硫酸溶于水放热,使溶液的温度升高;硝酸铵溶于水吸热溶液的温度降低;绝大部分物质溶于水温度变化不大;故答案选择A
12.【2017年江苏省扬州市】下列说法正确的是
A.粉笔灰分散到水中形成溶液 B.自来水是纯净水
C.长期饮用硬水有益人体健康 D.水是宝贵的资源
【答案】D
【解析】A选项是错误的叙述,粉笔灰分散到水中形成悬浊液;B选项是错误的叙述,自来水中含有一些可溶性物质,属于混合物;C选项是错误的叙述,长期饮用硬水会造成结石等病;D选项水是宝贵的自然资源,是正确的叙述;故答案选择D
13.【2017年江苏省苏州市】下列关于溶液的说法中,正确的是
A.泥土加入水中,振荡后可以形成溶液
B.蔗糖溶液上半部分溶液的甜度低于下半部分溶液的甜度
C.氢氧化钠溶液能导电,因为溶液中有较多自由移动的离子
D.氯化钠饱和溶液中不能再溶解少量硝酸钾晶体
【答案】C
14.【2017年湖南省长沙市】下列说法错误的是( )
A.饱和溶液一定是浓溶液 B.糖水、汽水都是溶液
C.洗洁精去油污是因为洗洁精具有乳化功能 D.溶液都是均一、稳定的混合物
【答案】A
【解析】A饱和溶液是在一定温度下、一定量的溶剂里不能再溶解某物质的溶液叫该物质的饱和溶液,反之为不饱和溶液。因不同的物质溶解能力不同,且溶解能力受温度能因素影响,所以饱和溶液不一定是浓溶液 ;B.糖水、汽水都是均一稳定的混合物,是溶液;C.洗洁精去油污是因为洗洁精具有乳化功能,可以将油污分散成很小的油滴,相对均匀的分数于水中; D.溶液是均一稳定的混合物,在溶液中物质以分子或离子等微观粒子的的形式相互混合,因没有阻挡光线的微粒,所以溶液都是澄清透明的。选A
二、非选择题
15.【2017年浙江省丽水市】用溶质质量分数为98%、密度为1.84克/厘米3的浓硫酸配制溶质质量分数为10%的稀硫酸100毫升,计算时必须查阅的数据是 。配制过程除使用量筒、玻璃棒和胶头滴管外,还需要的一种玻璃仪器是 。
【答案】质量分数为10%的稀硫酸的密度 烧杯
【解析】配制前后溶质质量相等。已知10%的稀硫酸100毫升。还必须查阅的数据是质量分数为10%的稀硫酸的密度;配制过程除使用量筒、玻璃棒和胶头滴管外,还需要的一种玻璃仪器是烧杯作为配制容器。
16.【2017年浙江省金华市】在室温条件下,对100mL氯化钠饱和溶液进行如图所示操作:
(1)最终甲、乙两烧杯中溶液一定是饱和溶液的是 。
(2)乙溶液在加50mL水的过程中,下列这些量逐渐减小的是 。
①溶解度 ②溶质质量分数 ③溶剂的质量 ④溶液的密度
【答案】(1)甲 (2)②④
17.【2017年浙江省嘉兴市】实验室有一瓶由氯化钾和硝酸钾组成的化肥,但标注的质量分数己模糊不清,小明想通过实验重新标注,以下是他进行的实验步骤:
①取10克样品于烧杯中,加入蒸馏水充分溶解,配制成60克溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
⑧将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35克。
请根据上述实验回答:(相关反应的化学方程式为:KCl+AgNO3=AgCl↓+KNO3)
(1)在过滤操作中使用的玻璃仪器有:烧杯、______和玻璃棒。
(2)样品中氯化钾的质量分数为多少?(要求列式计算)
(3)完全反应后,混合液中的硝酸钾质量是多少克?
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小于计算得出的理论值。造成这种结果的原因可能是 ______。 (选填编号)
A.晶体没有干燥 B.蒸发时液体飞溅 C.硝酸钾残留在玻璃棒上
【答案】(1)漏斗;(2)74.5%;(3)12.65g;(4)BC
18.【2017年天津市】(7分)溶液与人们的生活息息相关。
(l)下列少量物质分别放入水中,充分搅拌,可以得到溶液的是______(填字母)。
A.高锰酸钾 B.汽油 C.面粉
(2)在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度升高。这种物质是______(填字母)。
A.烧碱 B.硝酸铵 C.氯化钠
(3)下表是三种物质在不同温度时的溶解度,根据表中信息回答问题。
温度/℃
0
20
40
60
80
100
溶解度/g
氯化钠
35.7
36.0
36.6
37.3
38.4
39.8
硝酸钾
13.3
31.6
63.9
110
169
246
氢氧化钙
0.19
0.17
0.14
0.12
0.09
0.08
① 60℃时,氯化纳的溶解度_______硝酸钾的济解度(填“>”“=”或“<”)。
②表中某物质的饱和溶液随温度升高析出固体,该物质是_______(填化学式)。
③ 20℃时,氯化钠饱和溶液中溶质的质量分数为________(结果保留至0.1%)。
④ 向20℃的氢氧化钙饱和溶液中加入少量生石灰,再冷却至20℃,此时溶液中溶质的质量比加入生石灰前溶液中溶质的质量____(填“增大”“不变”或“减小”)。
⑤ 混有少量氯化钠的硝酸钾固体,加水配成80℃的硝酸钾饱和溶液,再冷却至20℃,析出晶体并得到溶液。下列有关说法中正确的是_______(填字母)。
A.析出的晶体中不一定含有硝酸钾
B.所得溶液一定是硝酸钾饱和溶液
C.上述方法可以将两种物质完全分离
【答案】(1)A;(2)A;(3)①<;②Ca(OH)2;③26.5%;④减小;⑤B
19.【2017年天津市】(10分)酸、碱、盐在生产生活中具有广泛的用途。
(l)制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制50g质量分数为10%的氢氧化钠溶液。
① 若用氢氧化钠固体配制,需称量氢氧化钠的质量为________g。
② 用氢氧化钠固体配制10%的氢氧化钠溶液过程中需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要________。
③ 下列操作正确的是________(填字母)。
A.称量氢氧化钠固体时,左盘放祛码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为lg/cm3)配制50g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为________g;配制时应选用________mL的量筒量取水(填“10”或“50”)。
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如下实验:
回答下列问题:
① 反应I 的化学方程式为____________。
② 白色沉淀C是________(填化学式)。
③ 原固体粉末中一定不含________(填化学式)。
【答案】(1)①5;②玻璃棒;③D;④25、50;
(2)①CaCO3+2HCl=CaCl2+CO2↑+H2O;②BaSO4;③CuSO4、BaCl2.
20.【2017年四川省内江市】(12分)仔细阅读下面的探究实验信息,回答相关问题。
I.[实验目的]探究溶解过程中,溶液温度的变化情况。
II.[查阅资料]
(1)物质溶解于水的过程包括吸收热量(Q吸)的扩散过程和放出热量(Q放)的水合过程。
(2)实验条件下,水的凝固点为0℃、沸点为100℃。
III.[提出猜想]物质溶解过程中,溶液的温度可能升高或降低或不变。
IV.[实验探究]某探究小组的同学设计了如下图所示的两种实验方案。在图2所示方案中,每次加入物质b之前,均使用温度计控制热水温度,使之保持在99℃。
V.[实验结论]
(1)图1所示实验中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度_____(填“升高”或“降低”或“不变”,下同)。
(2)图2所示实验中,若加入物质b后,热水会突然沸腾,说明溶液的温度__________。
VI.[拓展实验]按照图3所示进行实验。若物质c为NaOH,则U型管内的左边液面将_______(填“升高”或“低于”或“等于”)右边液面;若U型管内的液面位置变化与之相反,则物质c为______(填序号)。
①CaO ②NH4NO3 ③浓H2SO4
VII.[反思交流]
(1)该小组的同学进一步就物质溶解过程中溶液温度变化的原因展开了讨论,分析得出:若Q吸_____Q放(填“>”或“<”或“=”,下同),则溶液温度升高;若Q吸与Q放的相对大小与之相反,则溶液温度降低;若Q吸_____Q放,则溶液温度不变。
(2)在图2所示方案中,小张同学对实验现象很感兴趣,他继续向热水中加入相同质量的物质b,又看到沸腾现象,至烧杯中出现固体物质后,再继续加入相同质量的物质b,就看不到沸腾现象。请解释不再产生沸腾现象的原因________________________________。
【答案】.[实验结论](1)吸热;(2)升高;[拓展实验]低于;②;[反思交流]<; =;(2)形成物质b的饱和溶液,物质形成溶液沸点升高,物质说放出的热达不到溶液的沸点而不能沸腾。
21.【2017年四川省德阳市】(4分)某校化学课外活动小组的同学在实验室的一次探究性活动中,他们将50g氢氧化钠溶液与50g硫酸铜溶液混合恰好完全反应,得到9.8g沉淀。请你计算氢氧化钠溶液中溶质的质量分数。
【答案】16%
【解析】设氢氧化钠的质量为x,
CuSO4+2NaOH==Na2 SO4+Cu(OH)2↓
80 98
X 9.8g
80/x=98/9.8g x=8g
氢氧化钠溶液中溶质的质量分数8g÷50g×100%=16%
答:略
22.【2017年山东省德州市】(3分)控制变量法是科学探究中常用的方法之一。
(1)在探究固体物质的溶解度时,需要考虑的因素有:①溶质的种类; ②溶剂的种类;③溶质最多被溶解的质量; ④溶剂的质量; ⑤温度。
如测定“某物质在不同温度下的溶解度”,研究的是_________ (填序号)受温度的影响,这就需要控制其他因素保持不变。
(2)右表是利用控制变量法测得的氯化钠、硝酸钾在不同温度时的溶解度,请根据表格内容及实验现象回答下列问题。
温度(℃)
20
40
50
溶解度/g
NaCl
36.0
36.6
37.0
KNO3
31.6
63.9
85.5
①从上表可知,两种物质的溶解度受温度变化影响较大的是____________;
②20℃时,将等质量的NaCl、KNO3分别放入盛有100 g水的两个烧杯中,充分溶解后如图1所示,升温到50℃时如图2所示。试判断:50℃时甲烧杯中的溶液一定是______(填“饱和溶液”、“不饱和溶液”或“不能确定”)。
【答案】(1)③ (2)①硝酸钾(或KNO3) ②不饱和溶液
23.【2017年山东省临沂市】工业上常用红锌矿(主要含ZnO)和18~25%的稀硫酸为原料制取硫酸锌。
(1)硫酸锌中硫元素和氧元素的质量比是_________ 。
(2)l00g溶质质量分数为98%的浓硫酸配制成溶质质量分数为20%稀硫酸。需要水的质量是___。
【答案】(1)1:2 (2)390
【解析】(1)硫酸锌(ZnSO4)中硫元素和氧元素的质量比是32:16×4=1:2; (2)l00g溶质质量分数为98%的浓硫酸配制成溶质质量分数为20%稀硫酸。需要水的质量是l00g×98%÷20%---100g=390g
24.【2017年江苏省苏州市】(8分)为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验。(提示:本实验所川汽油与KMnO4、碘均不发生化学反应)
【实验l】KMnO4晶体在不同溶剂中的溶解实验
根据实验步骤、实验操作图示填写相关实验现象。
实验步骤
实验操作图示
实验操作及现象
步骤1
振荡后静置:
(1)A试管中晶体全部溶解,溶液呈________色;B试管中晶体不溶解,汽油不变色。
步骤2
将步骤1中A试管内溶液倒人B试管中,振荡后静置:(2)B试管中观察到的现象为__________。
【实验2]碘在不同溶剂中的溶解实验
根据实验操作图示回答相关问题。
实验操作图示
实验结论或解释
(3)由图2所示现象叮知:碘_____(选填“不”、“微”或“易”)溶于水
(4)图3所示试管中液体分层。上层紫红色溶液的名称是________。说明碘在汽油中的溶解性比在水中_____(选填“强”或“弱”)
【反思与应用】
(5)①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体______(选填“分层”或“小分层”)。
②“从稀碘水巾提取碘”是“海带提碘”工艺巾的一个重要步骤,其原理类似【实验2]中第二步操作。工业实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是________。
【答案】(1)紫(紫红、红)(2)液体分层,上层为无色,下层为紫红色,试管底部无固体残留
(3)微(4)碘的汽油溶液强(5)①不分层 ②与水不互溶,碘在这种液体中的溶解度远大于在水中的溶解度
【解析】(1)高锰酸钾能溶解在水中形成紫红色的溶液;将高锰酸钾溶液倒入汽油中,B试管中的高锰酸钾会溶解在水中,且还会发生分层现象,即液体分层,上层为无色,下层为紫红色,试管底部无固体残留;(3)由图可知,加入水后变成了淡黄色,故碘微溶与水;(4)碘微溶于水,但能溶解在汽油中形成碘的汽油溶液;(5)①汽油和酒精均属有机溶剂,有机物能溶解在有机溶剂中,即碘能溶解在酒精中形成碘酒溶液,故若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体不分层;②“从稀碘水巾提取碘”,使用其他挥发性液体代替汽油,这种挥发性液体必须与水不互溶,碘在这种液体中的溶解度远大于在水中的溶解度。
25.【2017年江苏省南京市】 (7分)溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是_________。
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为________,水的体积为________mL (水的密度近似看作1g/cm3)。
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如右下图.t1℃时,甲物质的溶解度是________。t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是________(填“甲”或“乙”)物质的饱和溶液。
选项
x
y
A
水
氧化钙
B
水
硝酸铵
C
浓硫酸
水
D
稀盐酸
镁
(4)按右上图所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是______。
【答案】(1) D ;(2) 16g 84 (3)40g 乙 (4) AD
26.【2017年湖南省邵阳市】化学源于生活,生活中蕴含着许多化学知识。
(1)用洗涤剂去除油污,是利用洗涤剂的__________作用。
(2)邵阳地区的生活用水多是硬水,生活中常用________的方法降低水的硬度。
(3)打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随______而减小。
(4)医生给胃酸过多的病人所开处方中,常包括含 Al(OH)3 的药物,试用化学方程式表示其治疗原理:______________ 。
【答案】(1)乳化 (2)煮沸 (3)压强减小(或气压减小)(4) Al(OH)3 +3HCl=AlCl3+3H2O
【解析】(1)洗涤剂对油污有乳化作用,能将油污分散成很小的的液滴,而被洗掉; (2)煮沸可以将硬水中的钙镁化合物转化成沉淀而降低水的硬度。 (3)气体的溶解度随压强减小(或气压减小)而减小;(4)氢氧化铝和盐酸反应生成氯化铝和水, 化学方程式表示为Al(OH)3 +3HCl=AlCl3+3H2O
27.【2017年湖南省邵阳市】某同学配制50g6%氯化钠溶液,整个操作过程如下图所示,回答下列问题:
(1)配制溶液的正确操作顺序为_______(填序号,下同),其中操作错误的是________。
(2)图② 中盛放氯化钠固体的仪器名称是 ______,需称取氯化钠 _______g。
(3)量水时选用的量筒的量程最合适的是______(填序号),读数时视线要与量筒内______保持水平。
A.10 ml B.25 ml C.50ml D.100ml
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是_______(填序号)。
A.氯化钠固体不纯 B.用生锈砝码称量
C.装瓶时有少量溶液洒出 D.溶解时烧杯内壁有水珠
【答案】(1)②①⑤③④ ① (2)广口瓶3或3.0 (3)C 凹液面最低处 (4) AD
【解析】(1)配制溶液的正确操作顺序为计算、称量、溶解、装瓶存放,即②①⑤③④ ;称量固体时,应遵循左物右码的原则;(2)图②中盛放氯化钠固体的仪器名称是广口瓶,氯化钠的质量是50g×6%=3g (3)取水的量为47mL,所以应用50mL的量筒;量取液体视线应平视凹液面最低处 (4) 配制的溶液溶质质量分数偏小的原因是溶质偏少或者溶剂偏多。氯化钠固体不纯,导致氯化钠偏少;溶解时烧杯内壁有水珠,导致水的量偏多。
28.【2017年广州市】(6分)某同学在实验室用6.5g粗锌(假设杂质不参与反应)和稀盐酸制取H2。
(1)配制100g 10%稀盐酸需要37%浓盐酸(密度1.19g/cm3)的体积为 mL(结果保留小数点后一位)。除了胶头滴管、烧杯外还需要的玻璃仪器是 、 。
(2)6.5g粗锌完全反应共产生H2的质量为0.16g,则该粗锌中锌的质量分数为 。
(3)验证后用装满水的10mL量筒代替小试管收集H2,装置如图所示。
①10mL量筒的最大刻度靠近 端。(填写“M”或“N”)
②当10mL量筒中的水全部被排尽后,实际收集到的H2体积V 10.0mL。(填写“>”、“=”或“<”)
【答案】(1)22.7 量筒、玻璃棒(2)80%(3)N、=
29.【2017年湖南省长沙市】将适量二氧化碳通入100g氢氧化钠溶液中,恰好完全反应后,得到108.8g碳酸钠溶液。请计算:
(1)参加反应的二氧化碳的质量为_______g;
(2)氢氧化钠溶液的溶质质量分数_________.
【答案】(1) 8.8;(2)16% 。