- 183.00 KB
- 2021-08-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
杂化轨道理论 配合物理论
A篇 知识对点训练
知识点一 杂化轨道理论简介
1.下列有关杂化轨道的说法不正确的是( )
A.原子中能量相近的某些轨道,在成键时能重新组合成能量相等的新轨道
B.轨道数目杂化前后可以相等,也可以不等
C.杂化轨道成键时,要满足原子轨道最大重叠原理、最小排斥原理
D.杂化轨道只能用于形成σ键或容纳孤电子对
答案 B
解析 原子轨道形成杂化轨道前后,轨道数目不变化,用于形成杂化轨道的原子轨道的能量相近。杂化轨道只能用于形成σ键或容纳孤电子对,不能形成π键。
2.以下有关杂化轨道的说法中错误的是( )
A.第ⅠA族元素成键时不可能有杂化轨道
B.杂化轨道既可能形成σ键,也可能形成π键
C.孤电子对有可能进入杂化轨道
D.s轨道和p轨道杂化不可能有sp4出现
答案 B
解析 第ⅠA族元素的价电子排布式为ns1,由于只有1个ns电子,因此不可能形成杂化轨道;杂化轨道只用于形成σ键或者用来容纳未参与成键的孤电子对;由于np能级只有3个原子轨道,所以s轨道和p轨道杂化只有sp3、sp2、sp 3种,不可能出现sp4杂化。
3.在BrCH===CHBr分子中,C—Br键采用的成键轨道是( )
A.spp B.sp2s
C.sp2p D.sp3p
答案 C
解析 分子中的两个碳原子都是采用sp2杂化,溴原子的价电子排布式为4s24p5,4p轨道上有一个单电子,与碳原子的一个sp2杂化轨道成键。
4.如图是乙烯分子的模型,对乙烯分子中的化学键分析正确的是( )
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C、H之间是sp2杂化轨道形成的σ键,C、C之间是未能参加杂化的2p轨道形成的π键
D.C、C之间是sp2
- 5 -
杂化轨道形成的σ键,C、H之间是未能参加杂化的2p轨道形成的π键
答案 A
解析 乙烯分子中存在4个C—H键和1个C===C键,C原子上孤电子对数为0,σ键电子对数为3,则C原子采取sp2杂化,C、H之间是sp2杂化轨道形成的σ键,C、C之间有1个是sp2杂化轨道形成的σ键,还有1个是未参加杂化的2p轨道形成的π键。
5.甲烷分子(CH4)失去一个H+,形成甲基阴离子(CH),在这个过程中,下列描述不合理的是( )
A.碳原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的稳定性发生了改变
D.微粒中的键角发生了改变
答案 A
解析 CH4为正四面体结构,而CH为三角锥形结构,形状、键角、稳定性均发生改变,但杂化类型不变,仍是sp3杂化。
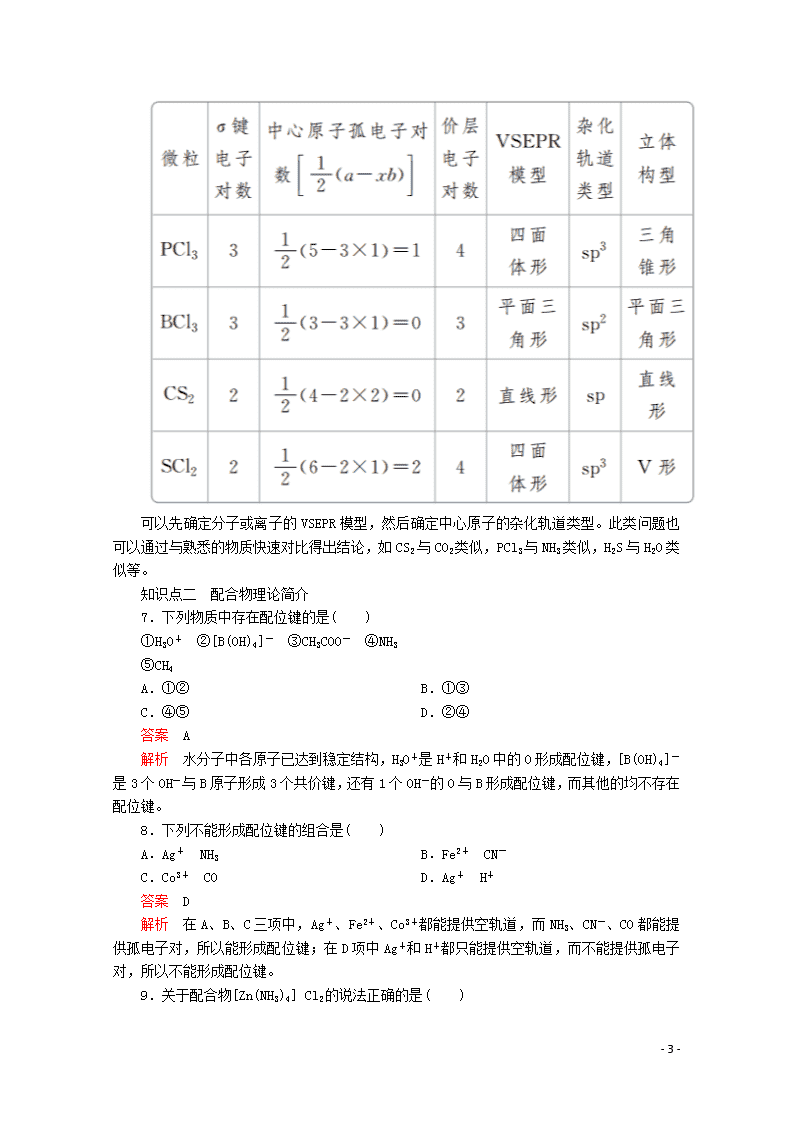
6.指出下列分子中,中心原子可能采取的杂化轨道类型,并预测分子的立体构型。
(1)PCl3________,________;
(2)BCl3________,________;
(3)CS2________,________;
(4)SCl2________,________。
答案 (1)sp3 三角锥形 (2)sp2 平面三角形
(3)sp 直线形
(4)sp3 V形
解析
- 5 -
可以先确定分子或离子的VSEPR模型,然后确定中心原子的杂化轨道类型。此类问题也可以通过与熟悉的物质快速对比得出结论,如CS2与CO2类似,PCl3与NH3类似,H2S与H2O类似等。
知识点二 配合物理论简介
7.下列物质中存在配位键的是( )
①H3O+ ②[B(OH)4]- ③CH3COO- ④NH3
⑤CH4
A.①② B.①③
C.④⑤ D.②④
答案 A
解析 水分子中各原子已达到稳定结构,H3O+是H+和H2O中的O形成配位键,[B(OH)4]-是3个OH-与B原子形成3个共价键,还有1个OH-的O与B形成配位键,而其他的均不存在配位键。
8.下列不能形成配位键的组合是( )
A.Ag+ NH3 B.Fe2+ CN-
C.Co3+ CO D.Ag+ H+
答案 D
解析 在A、B、C三项中,Ag+、Fe2+、Co3+都能提供空轨道,而NH3、CN-、CO都能提供孤电子对,所以能形成配位键;在D项中Ag+和H+都只能提供空轨道,而不能提供孤电子对,所以不能形成配位键。
9.关于配合物[Zn(NH3)4] Cl2的说法正确的是( )
- 5 -
A.配位数为6
B.配体为NH3和Cl-
C.[Zn(NH3)4]2+为内界
D.Zn2+和NH3以离子键结合
答案 C
解析 Zn2+的配位原子个数是4,所以其配位数是4,故A错误;该配合物中氮原子提供孤电子对,所以NH3是配体,故B错误;[Zn(NH3)4]Cl2中外界是Cl-,内界是[Zn(NH3)4]2+,故C正确;该配合物中,锌离子提供空轨道,氮原子提供孤电子对,所以Zn2+和NH3以配位键结合,属于特殊共价键,不属于离子键,故D错误。
10.水是生命之源,与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是__________。
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(2)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配离子。请写出生成此配离子的离子方程式:________________________________________。
答案 (1)A (2)Cu2++4H2O===[Cu(H2O)4]2+
解析 (1)水中氧原子以sp3杂化形成4个轨道,其中2个轨道是由孤电子对占据的,依据价层电子对互斥理论,孤电子对也参与互相排斥,水的空间构型为V形。在一定条件下水与氢离子结合形成配位键,这样氧原子与3个氢原子间的共用电子对和剩下的一对孤电子对相互排斥形成了三角锥形分子;同时其键角也发生改变,形成的微粒兼有水和氢离子的性质。故只有A不正确。
B篇 综合提升训练
11.下列说法正确的是( )
A.PCl3分子呈三角锥形,这是磷原子采取sp2杂化的结果
B.sp3杂化轨道是由任意的1个s轨道和3个p轨道混杂形成的4个新轨道
C.中心原子采取sp3杂化的分子,其立体构型可能是四面体形或三角锥形或V形
D.AB3型分子的立体构型必为平面三角形
答案 C
解析 PCl3分子的中心原子磷的价层电子对数=σ键电子对数+孤电子对数=3+=4,因此PCl3分子中磷原子采取sp3杂化,A项错误;sp3杂化轨道是原子最外电子层上的s轨道和3个p轨道混杂形成的4个新轨道,B项错误;采取sp3杂化的分子,中心原子若无孤电子对,其立体构型呈四面体形,若有,则分子的立体构型会发生变化,如NH3、PCl3分子呈三角锥形,H2O分子呈V形,D项错误,C项正确。
12.NF3分子中的中心原子采取sp3杂化,下列有关叙述正确的是( )
- 5 -
A.NF3分子的立体构型呈三角锥形
B.NF3分子的立体构型呈平面三角形
C.NF3分子中的N—F键间的夹角与CH4分子中的C—H键间的夹角相等
D.NF3分子不能与其他粒子形成配位键
答案 A
解析 氮原子采取sp3杂化,形成4个杂化轨道,其中1个轨道已填入孤电子对,另外3个则与F的2p轨道重叠形成共价键,所以NF3呈三角锥形。由于孤电子对对成键电子对的排斥作用,导致N—F键间的夹角小于CH4分子中的C—H键间的夹角。由于NF3中有孤电子对,所以NF3能与具有空轨道的原子或离子形成配位键。
13.下列现象与形成配合物无关的是( )
A.向FeCl3中滴入KSCN,出现红色
B.向Cu与Cl2反应后的集气瓶中加少量H2O,呈绿色,再加水,呈蓝色
C.Cu与浓HNO3反应后,溶液呈绿色;Cu与稀HNO3反应后,溶液呈蓝色
D.Fe在O2中燃烧产物为黑色
答案 D
解析 Fe3+与SCN-形成一系列配离子,都显红色;Cu2+在水溶液中形成配离子[Cu(H2O)2]2+显绿色;[Cu(H2O)4]2+显蓝色,故A、B、C项均与配合物有关。D项与配合物无关。
14.如图所示是甲醛分子的模型。根据该图和所学化学键知识回答下列问题:
(1)甲醛分子中碳原子的杂化方式是__________,做出该判断的主要理由是_____________。
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是__________(填序号)。
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角________(填“=”“>”或“<”)120°,出现该现象的主要原因是______________________。
答案 (1)sp2杂化 甲醛分子的立体结构为平面三角形 (2)②⑤ (3)< 碳氧双键中存在π键,它对C—H 键的排斥作用较强
- 5 -
相关文档
- 高中化学第二章分子结构与性质第二2021-08-0610页
- 高中化学第二章分子结构与性质3-22021-08-0616页
- 2019届一轮复习人教版分子结构与性2021-08-0610页
- 高中化学第二章分子结构与性质第三2021-08-065页
- 2020高中化学 第一章 原子结构与性2021-07-093页
- 高考化学第一轮复习课件第2讲 分2021-07-094页
- 高二化学第2章 分子结构与性质 章2021-07-098页
- 化学高考一轮复习课件:第13章 第2讲2021-07-0950页
- 备战2021 高考化学 加餐练34 分子2021-07-096页
- 2020届高考化学一轮复习分子结构与2021-07-0922页