- 1.74 MB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
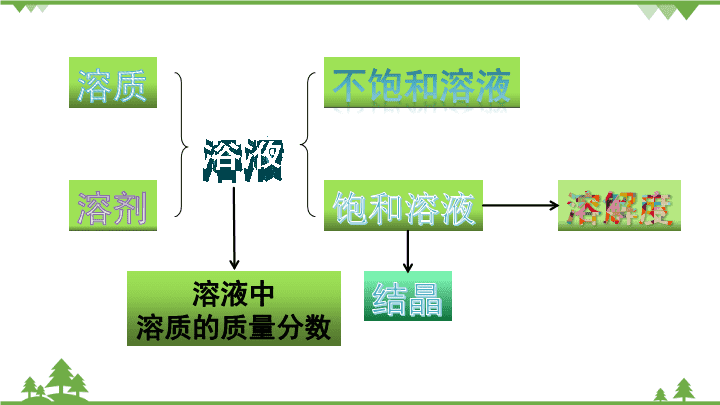
溶液中
溶质的质量分数
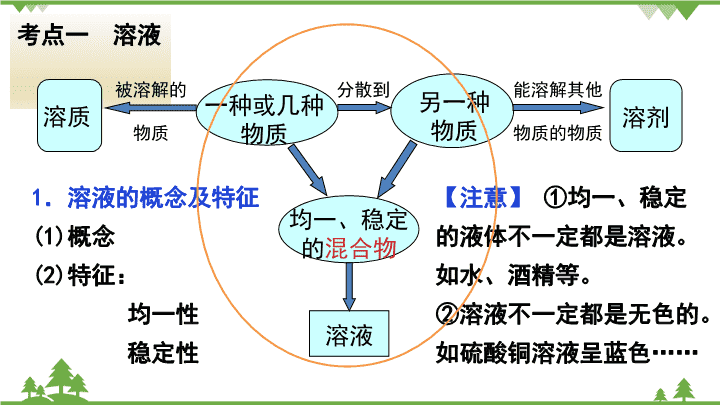
考点一 溶液
溶质
被溶解的
物质
一种或几种
物质
分散到 另一种
物质 溶剂
均一、稳定
的混合物
溶液
能溶解其他
物质的物质
1.溶液的概念及特征
(1)概念
(2)特征:
均一性
稳定性
【注意】 ①均一、稳定
的液体不一定都是溶液。
如水、酒精等。
②溶液不一定都是无色的。
如硫酸铜溶液呈蓝色……
③溶液中未溶解的部分不能视为溶质。
④与水发生反应的物质,放入水中时,生成物为该溶液的
溶质,如CaO放入水中时,溶质是Ca(OH)2,而不是CaO。
2.溶液的组成
溶液 溶质:
溶剂:
被溶解的物质
能溶解其他物质的物质
① m溶液= m溶质+ m溶剂
② V溶液≠V溶质+V溶剂
注意
因为在溶质分散到溶剂
的过程中,构成物质的
粒子不停运动,粒子的
间隔发生了变化。
物质在溶解时常伴随有吸热、放热现象。如________
溶解时会吸热,表现为溶液的温度降低;________溶
解时会放热,表现为溶液的温度升高;_________溶
于水时溶液的温度基本不变。
硝酸铵
氢氧化钠
3.溶解时的吸热、放热现象
氯化钠
注
意
①物质溶于水后,往往会使溶液的沸点、凝
固点、密度等发生变化。
②氧化钙遇水也会放出大量的热,但这一过程
并非溶解放热,而是氧化钙与水反应放出的热。
当在植物油中加入洗涤剂后振荡,植物油就被分散成
无数细小的油滴,而不能聚集成大的油珠,这种现象
被称为_________。肥皂、洗涤剂等都具有乳化作用。乳化现象
4.乳化作用
【注意】乳化与溶解的不同点在于,分散的物质在水中存在的
状态不同。植物油被乳化后变成无数细小的油滴分散在水中,
较稳定,但不是非常均匀;而溶质溶解在水中,是以分子或离
子的形式存在的,具有均一、稳定的特征。
【练习1】(海南中考)下列厨房用品在水中能形成
溶液的是( )
A.芝麻油 B.面粉 C.蔗糖 D.黄豆酱
【练习2】(湖北宜昌中考)下列物质溶于水的过程
中,溶液温度会明显降低的是( )
A.氯化钠 B.硝酸铵
C.浓硫酸 D.氢氧化钠
C
B
【练习3】(湖北天门中考)下列有关溶液的叙述错
误的是( )
A.长期放置后不会分层的液体一定是溶液
B.衣服上的油污用汽油或用加了洗涤剂的水可除去
C.一瓶合格的生理盐水密封一段时间,不会出现浑浊
D.实验室常将固体药品配制成溶液进行化学反应,以
提高反应速率
A
考点二 饱和溶液与不饱和溶液
溶液
饱和溶液---
不饱和溶液--
在一定
温度
在一定温度下,在一定量
的溶剂里,不能再继续溶
解某种溶质的溶液
在一定温度下,在一定量
的溶剂里,还能继续溶解
某种溶质的溶液
增加溶剂、升高温度
加入溶质、蒸发溶剂、降低温度
饱和溶液 不饱和溶液
相互
转化
①某物质的饱和溶液是指相应的溶质不能继续
溶解的溶液,但还可以溶解其他物质。如饱和食
盐水还可以继续溶解硝酸钾固体。
②通过降低温度实现由不饱和溶液向饱和溶液的转化,
只是针对多数固体溶质而言,对气体和少数固体(如
熟石灰)等不适用。
③对某饱和溶液进行降温或蒸发溶剂时,往往会有溶
质从溶液中以晶体形式析出。
注
意
4、浓、稀溶液与饱和不饱和溶液之间的关系
①饱和溶液不一定是浓溶液
②不饱和溶液不一定是稀溶液,如饱和的石灰水溶液就是稀溶液
③在一定温度时,同一种溶质的饱和溶液一定要比它的不饱和溶
液浓
5、混合物的分离
(1)过滤法:分离可溶物 + 难溶物
(2)结晶法:分离几种可溶性物质
结晶的两种方法
①蒸发结晶(蒸发溶剂):适用于得到溶解度受温度影响较小的
物质。如NaCl(海水晒盐)
②降温结晶(冷却热饱和溶液):适用于得到溶解度随温度升高
而升高的物质,如KNO3
【练习4】(浙江义乌中考)某次蔗糖溶解实验过程如图
所示,不考虑水分蒸发,下列判断错误的是( )
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
B
考点三 溶解度及溶解度曲线
1.固体物质的溶解度
(1)概念:在___________下,某固态物质在______g 溶剂里达到
______状态时所溶解的______,叫作这种物质在这种溶剂里的
溶解度。如果不指明溶剂,通常所说的溶解度是指物质在水中
的溶解度。
(2)影响因素
①内因:溶质和溶剂的性质;
②外因:主要是________。
一定温度 100
饱和 质量
温度
. . .
0.01g 1g 10g
易溶 可溶 微溶 难(不)溶
.
溶解度与溶解性(通常状态下)
2.气体的溶解度
(1)概念:是指在一定温度下,压强为________ 时,
某气体溶解在_____体积的水里达到________状态时
的气体________。
(2)影响因素:
①内因:气体的性质。
②外因:主要是温度和压强。温度越高,气体的溶解
度_______;压强越大,气体的溶解度______。
101 kPa
1 饱和
体积
越小 越大
3.溶解度曲线
(1)概念:指溶解度随温度变化的曲线。横坐标表示________,
纵坐标表示__________。
温度
溶解度
KNO3
NaCl
Ca(OH)2
(3)
规
律
大多数固体物质的溶解度随温度的升高而增大,如_______;
少数固体物质的溶解度受温度的影响很小,如________;
极少数固体物质的溶解度随温度的升高而减小,如________。
(2)含义:①曲线上的点表示某物质的饱和溶液;②曲线的走向
表示某物质的溶解度随温度的变化趋势;③两条曲线的交点表示
两种溶质在交点对应温度下的溶解度相同。
(4)溶解度曲线常见的考查形式(如图)
①t3℃时,a的溶解度为________g。
②P点的含义是_________________________。
50
t2℃时,a和c的溶解度相等
③N点对应的溶液为t3℃时a的__________溶
液,可通过
____________________________________等
方法使a的不饱和溶液变成饱和溶液。
④t1℃时,a、b、c三种物质的溶解度由大到
小的顺序为______________。
不饱和
加入a物质(或降温,或恒温蒸发溶剂)
c>b>a
⑤从a溶液中获取a晶体可采用__________________的方法。
⑥从b溶液中获取b晶体可采用__________________的方法。
冷却热饱和溶液
蒸发结晶
⑦t2℃时,a、b、c三种物质的饱和
溶液各w g,降温至t1℃会析出晶体
的是__________,此时所得溶液中
溶质的质量分数由小到大的顺序是
_________。
⑧分离a与少量b 的混合物,可采用
_____________的方法。
a和b
a<c<b
降温结晶
考点四 溶质的质量分数
1.定义:溶质质量与溶液质量之比
=溶液质量(溶质质量+溶剂质量)
溶质质量溶质的质量分数 ×100%
①质量单位要统一
②既适用于饱和溶液的计算,也适用于不饱和溶液的计算。
③溶质的质量分数一般用百分数来表示,不能用分数表示。
④未溶解的物质不能计入溶质质量。
注
意
2.一定温度下,某物质饱和溶液的溶质质量分数
= 100g + 溶解度
溶解度饱和溶液的
溶质质量分数 ×100%
点拨:一定温度下,某饱和溶液的溶质质量分数为定值。
3.关于溶液稀释问题的计算
溶液稀释前后,溶质的质量不变
点拨:溶质质量 = 溶液质量 × 溶质的质量分数
【例1】(新疆中考)某化学兴趣小组取12.5g的 大理
石样品(杂质不与盐酸反应)加入到一定量的稀盐酸
中,产生CO2的质量与稀盐酸的质量关系如图所示。
请计算:
(1)生成CO2的质量是_____g;
(2)该盐酸的溶质质量分数是多少?
(列式计算,计算结果保留到0.1%)
4.4
(2)解:设该盐酸中溶质的质量为x。
73 44
x 4.4g
盐酸的溶质质量分数 =
答:该盐酸的溶质质量分数是7.3%。
CaCO3+2HCl==CaCl2+H2O+CO2↑
= 4.4g
x
44
73
x = 7.3g
100g
7.3g ×100%
= 7.3%
考点五 一定溶质质量分数溶液的配制
配制50 g溶质质量分数为5%的氯化钠溶液
仪器:托盘天平(砝码盒)、量筒(10mL、50mL、100mL)、
___________、烧杯、________、________、擦拭纸、称量纸。
步骤:①计算:需氯化钠的质量为_____,需水的体积为_______
②称量:分别在托盘天平左右两盘放上相同的称量纸,调节托盘
天平平衡后,先将游码移动至______,然后逐渐往_____盘加氯化
钠固体至天平平衡。
玻璃棒 药匙 胶头滴管
2.5 g 47.5 mL
2.5 g 左
③量取:用________的量筒量取________的水。
④溶解:用玻璃棒搅拌的目的是________________,溶解时
________(填“能”或“不能”)在量筒中进行。
⑤装瓶贴标签。
50 mL 47.5 mL
加速溶解
不能
【练习5】(陕西中考)规范的实验操作是实验成功的
关键。下列配制20 g 10%的氯化钠溶液的操作中不规
范的是( )B
1.均一、稳定的混合物是溶液,溶液不一定是无色透明的,溶
液不一定是液体(某些合金、新鲜的空气也是溶液);溶液中被
溶解的物质才是溶质,一种溶剂可溶解多种溶质。
2.只有指明“一定的温度”和“一定量的溶剂”,溶液的“饱
和”与“不饱和”才有确定的意义。
3.物质溶于水时,如果发生了化学变化,则反应后的生成物是
被溶解的溶质。
4.汽油、洗洁精去油污的原理不同,前者为溶解,后者为乳化。
易错点归纳
相关文档
- 初中化学九年级上册第五单元化学方2021-11-1020页
- 北师大版(2012)九年级下册数学随堂小2021-11-108页
- 苏教版数学九年级上册课件3-1平均2021-11-1012页
- 2021化学中考模拟卷72021-11-104页
- 人教部编版九年级下册语文教学课件2021-11-1020页
- 苏科版江苏省九年级上学期期中联考2021-11-104页
- 人教版九年级物理下册-第二十一至2021-11-105页
- 九年级下册数学人教版知识要点汇总2021-11-108页
- 2019-2020学年江西省吉安市吉州区2021-11-1027页
- 九年级物理全册14-1电是什么课件(新2021-11-1015页