- 956.50 KB
- 2021-11-11 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第八单元 海水中的化学
可能用到的相对原子质量:H-1 C-12 O-16 Na-23
一、选择题
1.我国化学家侯德榜改进了一种化工产品的工业生产技术,其产品获得美国费城万国博览会金奖,这种生产技术用于( )
A.生产烧碱 B.生产纯碱 C.精制粗盐 D.生产尿素
2.下列过程发生化学变化的是( )
①海水晒盐 ②海水制碱 ③海水淡化 ④海水制镁
A.全部 B.只有② C.只有②④ D.②③④
3.如图是实验室里一瓶标签破损的白色粉末状固体。小明同学取出少量该固体放入一洁净试管中,加水振荡后固体溶解,形成无色透明溶液,继续加入少量盐酸,有无色、无味的气体产生。该固体可能是( )
A.Na2SO4 B.NaCl C.Na2CO3 D.NaOH
4.鱼胆弄破后会使鱼肉粘上一种叫胆汁酸(一种酸)的难溶于水的物质,使鱼肉变苦,要清除这种苦味,可用下列何种溶液冲洗最为适宜( )
A.食盐水 B.醋酸 C.纯碱溶液 D.烧碱溶液
5.下列有关海水晒盐的几种说法,错误的是( )
A.海水成为食盐的饱和溶液后才能析出晶体
B.盐场必须建在阳光充足、雨量少的地区
C.结晶池中析出盐后的母液没有用途,为防止污染须排入大海
D.盐场利用日晒、风吹晒盐,采取的是蒸发结晶的方法
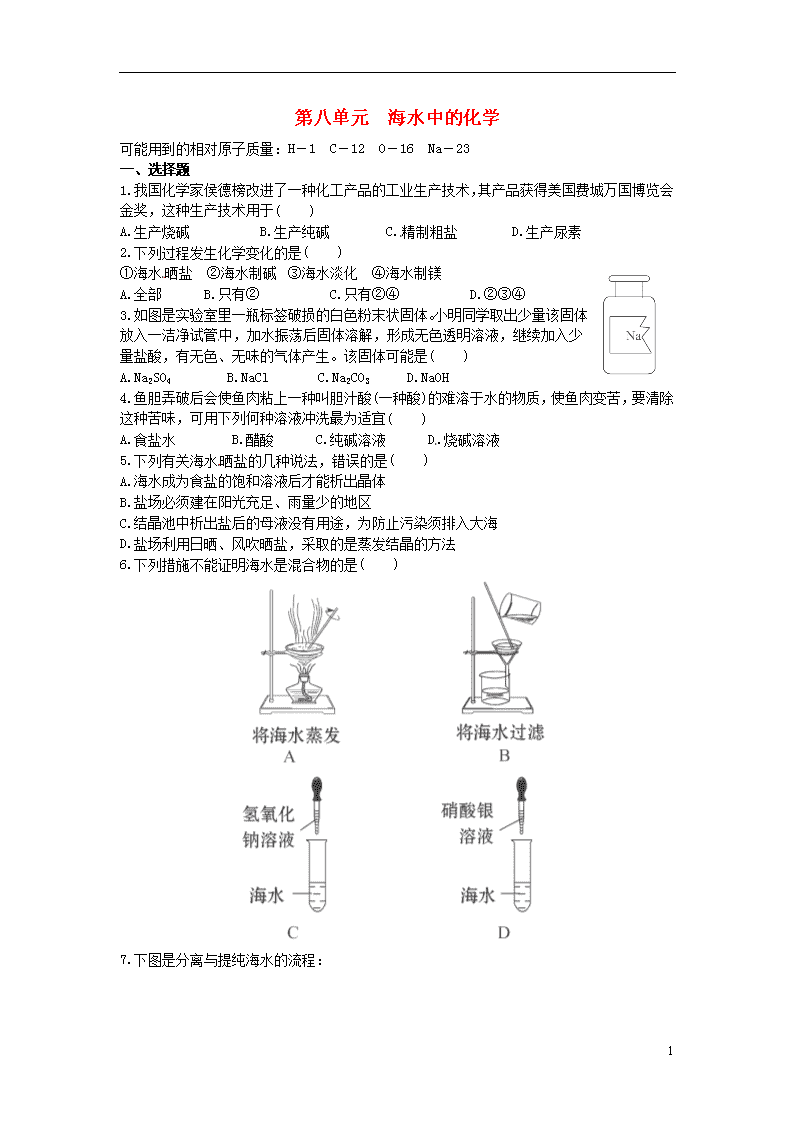
6.下列措施不能证明海水是混合物的是( )
7.下图是分离与提纯海水的流程:
4
下列有关认识错误的是( )
A.常用于淡化海水的方法有蒸馏法、过滤法等
B.粗盐提纯为较纯净的食盐晶体的操作为:溶解、过滤、蒸发
C.通常在苦卤中加入熟石灰制取氢氧化镁
D.海水中的食盐用途广泛,例如侯德榜利用食盐为原料制得了纯碱
8.下列物质中,与CO2、CuCl2溶液、Na2CO3溶液都能发生反应,且都有明显现象的是( )
A.NaOH B.Ca(OH)2 C.H2SO4 D.HCl
9.滴有酚酞的氢氧化钙溶液与下列物质恰好完全反应后仍显红色的是( )
A.稀硫酸 B.氯化铜溶液 C.碳酸钾溶液 D.二氧化碳
10.下列两种物质的溶液混合后,能发生反应,且溶液的总质量不会发生改变的是( )
A.氢氧化钠溶液和稀盐酸 B.碳酸钠溶液和稀盐酸
C.氯化钠溶液和稀硫酸 D.碳酸钠溶液和氯化钙溶液
11.在推断实验室无色废液的成分时,四位同学得出了四种结论,其中可能合理的是( )
A.NaCl、CuSO4、NaNO3 B.NaCl、K2SO4、NaOH
C.HCl、NaOH、CaCl2 D.K2CO3、KNO3、BaCl2
12.除去下列物质中含有的杂质所选用试剂或操作方法不正确的一组是( )
物质
所含杂质
除去杂质的试剂或方法
A
NaCl溶液
Na2CO3
过量盐酸,加热
B
CuO
Cu
灼烧
C
KCl
KClO3
MnO2,加热
D
O2
H2O
浓硫酸,干燥
13.如图所示,X溶液与AgNO3、Na2CO3、Na2SO4三种溶液发生反应均生成白色沉淀。则X可能是下列哪种物质的溶液( )
A.HNO3或KNO3 B.HCl或H2SO4
C.BaCl2或CaCl2 D.NaOH 或Ca(OH)2
二、填空与简答题
14.现有生活中的下列物质,请回答有关问题:
4
(1)纯碱属______类(填“酸”“碱”或“盐”),其水溶液的pH______7(填“大于”“小于”或“等于”);
(2)上述物质中含碳酸钙的是________(填序号);
(3)发酵粉的主要成分是(填化学式)__________;
(4)上述四种物质(或其中的主要成分)共同的化学性质是都能跟______反应;
(5)工业上可利用上述物质中的________溶液(填溶质化学名称)与石灰水反应制取氢氧化钠,有关反应的化学方程式为_____________________________。
15.如果以碳酸钙、碳酸钠、水为原料制取氢氧化钠,可设计如下反应过程:
请写出有关反应的化学方程式①_____________________________________;
②_______________________________________________________________;
③_______________________________________________________________。
三、实验与探究题
16.某兴趣小组进行粗盐提纯并配制NaCl溶液,请回答下列问题:
(1)操作①、②、③依次为下图中的(填字母)________。
4
(2)若NaCl的产率偏低(产率=100%),则可能的原因是(填字母)________。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含有泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制5% NaCl溶液50.0 g,需称取NaCl______g,配制时需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、________。
17.某兴趣小组发现一袋腌制松花蛋的泥料,配料表上的成分是氧化钙、纯碱和食盐。他们要探究在腌制松花蛋过程中都有哪些物质对鸭蛋起作用。于是取少量泥料在水中溶解,充分搅拌后过滤,取滤液探究其成分。
【猜想与假设】他们都认为滤液中一定有NaCl和NaOH。生成氢氧化钠的化学方程式为____________________________________________________________
__________________________________________________________________。
对其他成分他们分别做出了如下猜想:
小亮猜想:还可能有Na2CO3
小强猜想:还可能有Ca(OH)2和Na2CO3
你认为谁的猜想是错误的________,理由是_____________________________
__________________________________________________________________。
你还能做出的猜想是:还可能有_______________________________________
__________________________________________________________________。
【活动与探究】小亮取一定量的滤液于试管中,向其中滴加了几滴稀盐酸,振荡,没有气泡,于是他得出结论:没有Na2CO3。
请你选择CO2以外的物质,设计一个实验方案验证你的猜想。
实验步骤
现象及相应结论
【反思】小强认为小亮的结论不严密,理由是___________________________
__________________________________________________________________。
四、计算题
18.现有13.7 g由Na2CO3与NaHCO3组成的混合物,其中Na2CO3占5.3 g,请计算
(1)混合物中碳元素与氧元素的质量比为________;
(2)混合物中钠元素的质量分数为________。(精确至0.1%)
19.用“侯氏联合制碱法”制取的纯碱(Na2CO3)中常含有少量的氯化钠。化学实验小组同学为测定某厂生产的纯碱中碳酸钠的含量,称取12 g样品放入烧杯中并滴加稀盐酸,当盐酸滴加至73 g时,气泡不再冒出,此时称得烧杯内溶液的总质量为80.6 g。
试计算:
(1)产生二氧化碳气体的质量是________ g。
(2)该厂生产的纯碱中碳酸钠的质量分数。(计算结果精确到0.1%)
4
相关文档
- 2020九年级化学下册 第八单元 海水2021-11-113页
- 2020九年级化学下册 单元测试(二)海2021-11-115页
- 2019九年级化学全册 第三单元 海水2021-11-118页
- 2020九年级化学下册 第八单元 海水2021-11-114页
- 第八单元海水中的化学知识点2021-11-107页
- 2019九年级化学全册 第三单元 海水2021-11-1012页
- 2020九年级化学下册 第八单元 海水2021-11-066页
- 2020九年级化学下册 第八单元 海水2021-11-063页
- 2020高中化学 第三章 自然界中的元2021-08-063页
- 2020年高中化学 第三章 自然界中的2021-08-065页